基因工程与进化研究
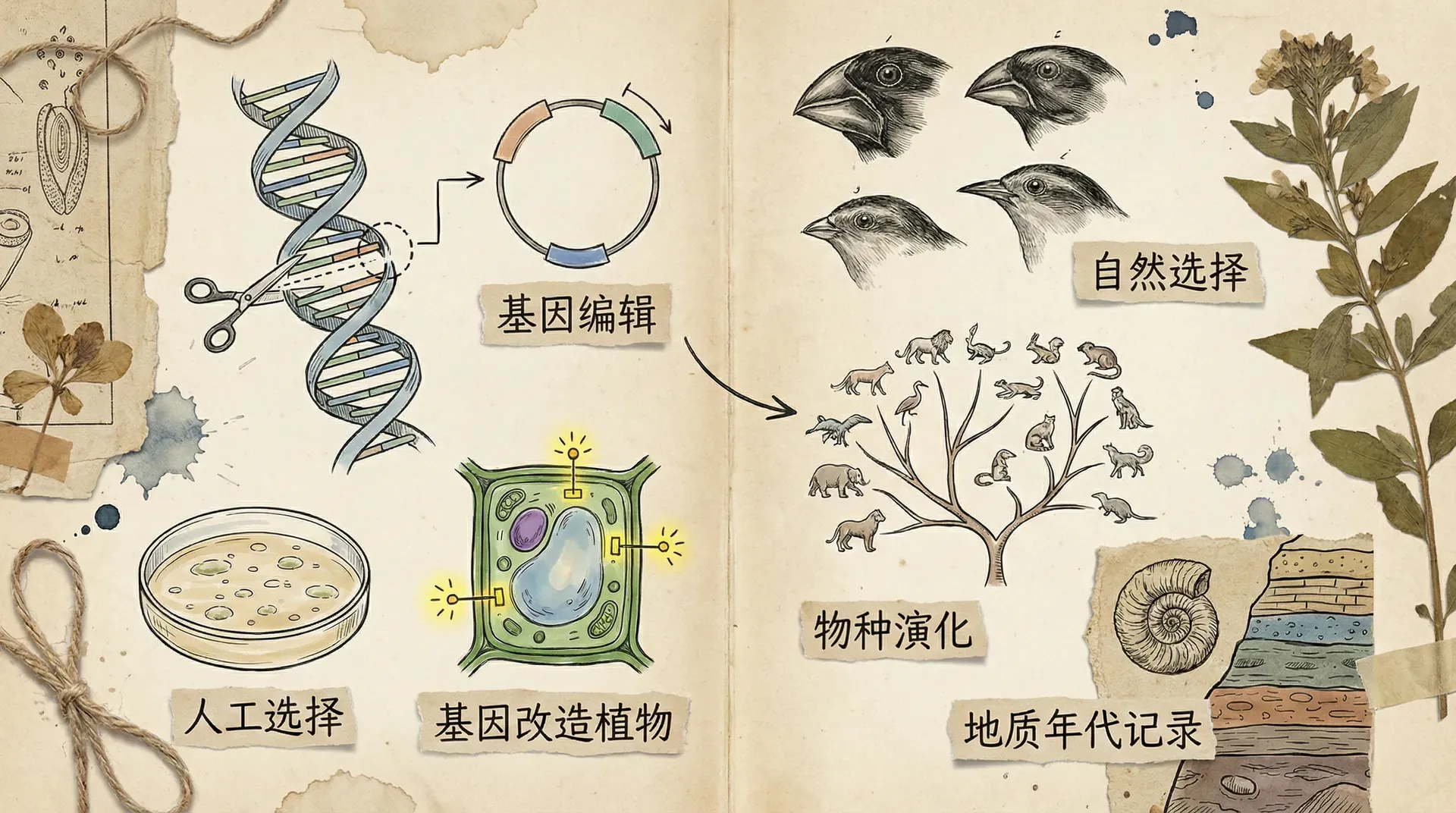
二十世纪八十年代,随着DNA分析技术的成熟,生物学研究掀开了新篇章。科学家们利用分子层面的“时光机器”——DNA序列比对,不仅能够追溯现存生物的演化轨迹,更颠覆了许多传统基于外形判断的生物分类。例如,在1984年前后,通过对不同物种DNA的比对,研究人员惊讶地发现人类与黑猩猩的基因差异竟然不到2%,远远小于此前预计。这一分子证据使我们对人类在生命之树上的位置有了全新认识。
同样,DNA技术也彻底改写了鸟类的进化史。许多外形相似的鸟类,在DNA层面却差异巨大;反之,一些看似完全不同的鸟类,其基因却显示高度相似。这说明,单凭外表很容易误判进化关系,DNA比对才是揭示生物亲缘的“族谱”。
DNA序列比对就像是阅读生物的“族谱”,序列越相似,说明共同祖先越近。通过比较差异,科学家甚至可以大致推算物种分化的大致年代。
八十年代初的一系列基因层面新发现,进一步揭示了生命发育的共通性。例如,1983年研究人员在哺乳动物和环节动物体内都发现了“同源异形盒”(homeobox)基因——这套通用的遗传“程序代码”主导了各类动物的身体结构发育。也就是说,从蠕虫到人类,复杂程度虽大不同,却都在沿用来自遥远祖先的遗产。
与此同时,基因组的动态性也成为一大突破。同一时期玉米研究中,科学家发现了能在染色体上“跳跃”的遗传元件,有效提升了作物育种效率,也展示了基因并非一成不变,而是充满流动与变迁,这为理解生物进化机制提供了关键线索。至1987年,法规完善推动了基因工程研究进入快车道。中国科学家在水稻等作物基因组、转基因技术等领域连获突破,像华大基因等机构在基因测序方面的进展,更为后续人类基因组计划作出了重要贡献。
基因技术服务医学
遗传疾病的基因突破
基因技术从实验室走向临床应用,最直接的体现就是对遗传疾病致病基因的发现。1990年,研究人员成功定位了导致神经纤维瘤病的基因。这种疾病会导致患者皮肤和神经系统出现大量良性肿瘤,严重影响患者的生活质量和外观。找到致病基因后,科学家进一步确定了这个基因负责生产的蛋白质,这为理解疾病机理和开发治疗方法奠定了基础。
类似的突破在各种遗传疾病研究中不断涌现。囊性纤维化是一种严重的遗传性疾病,患者的肺部和消化系统会分泌异常粘稠的黏液,导致反复感染和营养不良。经过多年研究,科学家在1989年终于找到了导致这种疾病的基因缺陷。这个基因位于特定染色体的一个狭窄区域内,研究人员通过分析大量家系的遗传数据,逐步缩小搜索范围,最终精确定位。
在中国,遗传疾病的基因研究同样取得了重要进展。地中海贫血是我国南方地区高发的遗传性血液病,广东、广西、海南等省份的发病率较高。通过基因筛查技术,医疗机构可以在婚前或产前检测夫妻双方是否携带致病基因,从而有效降低重症患儿的出生率。
基因治疗的开端
找到致病基因只是第一步,更关键的是能否利用基因技术来治疗疾病。1990年7月,世界上首例基因治疗正式获得批准。这次治疗针对的是腺苷脱氨酶缺乏症,这是一种罕见但致命的遗传性免疫缺陷疾病。患者由于缺乏特定的酶,导致免疫系统无法正常工作,极易受到各种感染的侵袭。
基因治疗的基本思路是:从患者体内取出免疫细胞,在实验室中将正常的基因导入这些细胞,然后将修复后的细胞回输到患者体内。这些携带正常基因的细胞能够生产缺失的酶,从而部分恢复患者的免疫功能。这种治疗方法虽然还不能完全治愈疾病,但显著改善了患者的生活质量。
基因治疗的核心理念是“缺什么补什么”——如果患者体内某个基因缺失或损坏,就通过技术手段补充正常的基因拷贝。这种治疗方式从根源上解决问题,而不仅仅是缓解症状。
在中国,基因治疗研究也在稳步推进。1990年代后期,中国科学家开始探索用基因治疗的方法治疗血友病、某些类型的癌症等疾病。虽然技术仍在不断完善,但基因治疗为许多过去无法治愈的疾病带来了新的希望。
生物伦理学的诞生
为什么需要生物伦理
随着生物技术的飞速发展,越来越多涉及人类健康、环境和社会价值观的伦理问题浮出水面。20世纪90年代,“生物伦理学”应运而生,成为一门集生物学、医学、哲学和法学等多学科于一体的新兴交叉领域。生物伦理学关注的不仅是单纯的技术问题,更重要的是思考技术进步给社会和人类带来的长远影响。
其实,生物伦理的萌芽远早于这个时代。1970年代,重组DNA技术刚刚面世,科学界已开始担忧其潜在风险。例如:
这些问题催生了1975年著名的阿西洛马会议(Asilomar Conference),成为现代生物伦理公共讨论的开端。随着70年代末环保理念的兴起,社会各界也对工业污染、核能安全、人口增长等问题产生了更深关注,为伦理反思注入新的动能。
到了1980年代,关注焦点进一步向基因工程倾斜:科学家激进推进基因操作,是否会导致未知的生物风险?转基因作物商品化,会不会影响食品安全和生态平衡?这些讨论推动伦理学者与科研人员建立更密切的合作机制。
在中国,自上世纪80年代末,随着现代生物医学研究的推进,伦理审查制度逐步建立。各大医院、科研单位纷纷设立伦理委员会,对涉及人体的医学研究进行严把“知情同意”“风险可控”等原则,为保障受试者利益和推动学科健康发展提供了坚实的制度支撑。
伦理关注的演变
生物伦理关注的议题随着时代演进不断扩展。下表列出部分典型关注点随年代的变迁:
动物实验伦理成为生物医学研究中不可回避的议题。研究离不开动物,但如何在推进科学进步的同时保护动物福利,是社会持续讨论的热点。例如,中国2006年出台《实验动物管理条例》,强制实验必须取得资质、保障动物饲养条件,并要求开展“3R原则”(减少Reduce、优化Refine、替代Replace)的研究设计。
关注重点的转移示例
生物伦理学的目标并非阻碍科技发展,而是促使科学家和社会公众共同评估风险和利益,确保科技应用尊重人权、照顾弱势群体以及保护未来的生态环境。
科研诚信也成为新的伦理关注重点。数据造假、剽窃、署名纠纷等学术不端行为频现,不仅损害科学公信力,也造成极大资源浪费。中国自2000年代起陆续出台了科研诚信建设系列文件,例如科研诚信档案、学术不端惩戒机制等,逐步完善学术“防线”。
医学实践中的伦理困境
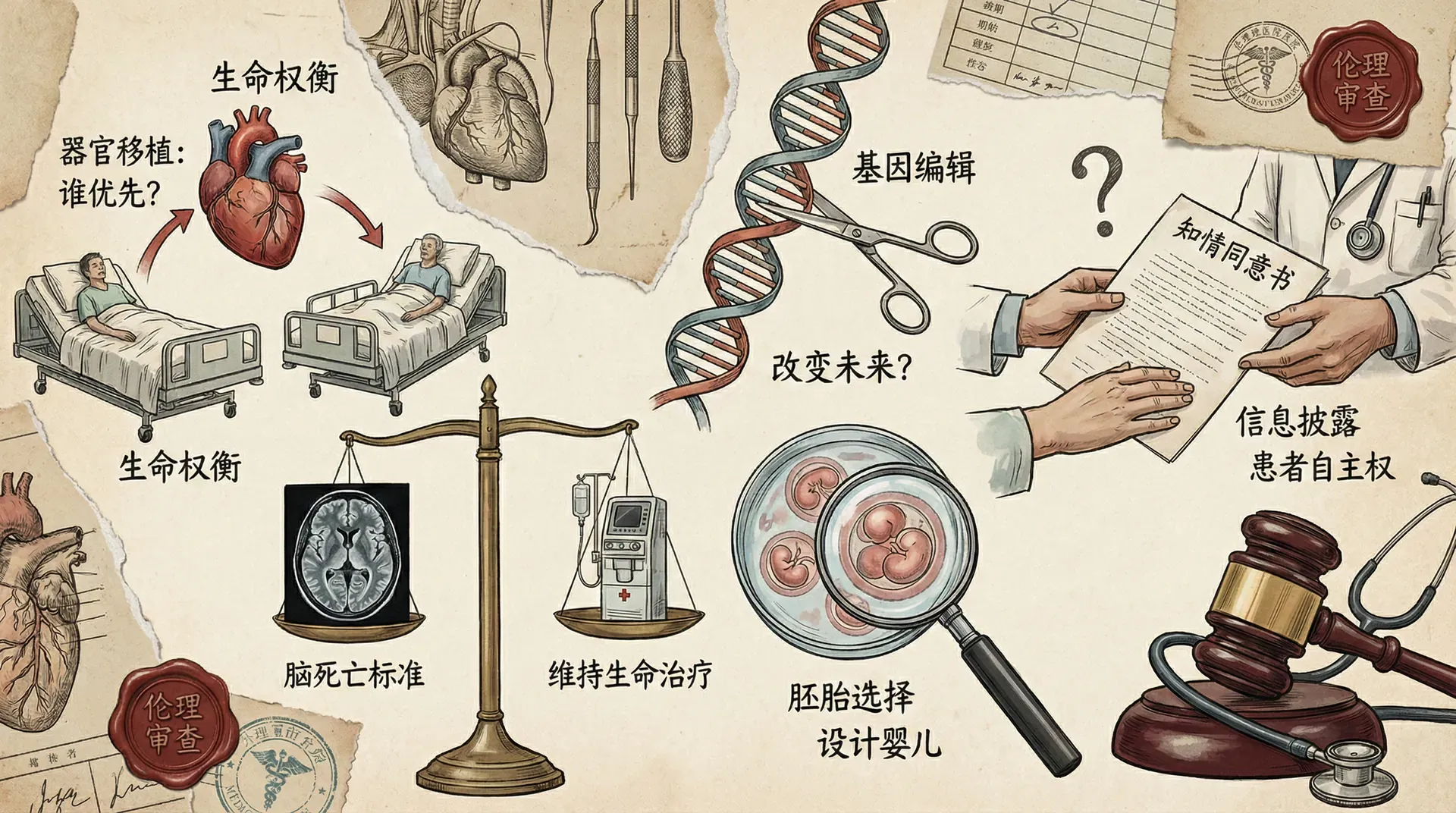
生殖技术的伦理问题
辅助生殖技术(如体外受精/IVF、人工授精)为数百万不孕症患者带来希望,但也带来一系列新的伦理难题。
- 案例一:试管婴儿胚胎归属
比如在夫妻离婚或一方去世的情况下,多余冷冻胚胎的“所有权”归谁?是否可以单方面决定胚胎植入或销毁? - 案例二:卵子/精子的匿名与知情权
捐献者信息应否告知新生儿?孩子有权了解其遗传来源吗?
胚胎研究亦高度敏感。科学界常用“14天规则”作底线,中国在2003年出台《人胚胎干细胞研究伦理指导原则》,规定人类胚胎体外培养不得超过14天,并严禁将人胚植入非人动物。该规则得到主流社会认可,平衡了科学探索和道德底限。
生命终结的定义
医疗进步促使“死亡”的标准变得复杂,尤其是脑死亡和持续性植物状态(PVS)。下表总结了生命终结关键问题及其聚焦点:
背景补充
医学伦理的核心,在于不断平衡技术可行性与人文关怀。并非所有“能做的”都“应该做”,只有在科学、法律与社会充分对话后,每一个生命相关的选择才能更有温度与尊严。
人类基因组计划
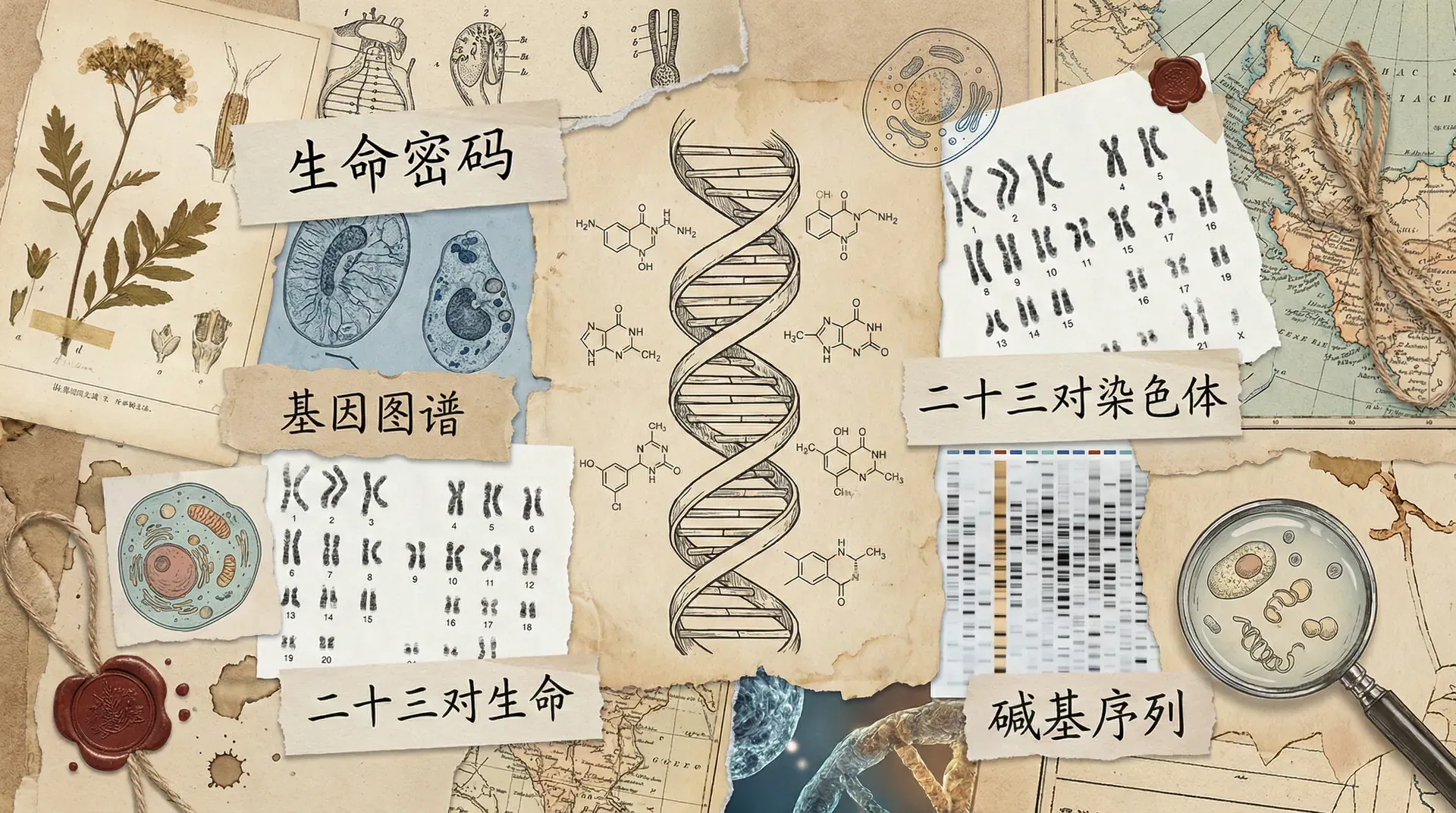
起源、目标与策略
20世纪80年代,科学界提出了“绘制完整人类基因组序列”的愿景——即破解人类约30亿碱基对的全部基因信息,希望把遗传病致病基因定位与医学研究推向全新高度。过去科学家定位单个致病基因需多年,而基因组图谱的建立可极大提升效率,就像有了全新地图查找“目的地”。
人类基因组计划(Human Genome Project, HGP)于1990年正式启动,最初由美国能源部和国立卫生研究院主导,目标是15年内完成测序。项目采用“分步法”策略——先建立覆盖全基因组的遗传标记地图(DNA短片段,每隔约200万碱基设一标记),再逐步精细测序,大大提升了工作速度。
项目主要阶段如下:
国际合作与中国角色
随着项目推进,HGP迅速发展为全球性的大协作平台,欧洲、日本等国家也加入分工测序。1999年中国团队正式加盟,承担了人类3号染色体短臂约3000万个碱基的测序任务,占总量1%。这不仅表明中国在基因组学有突破性进展,也为中国与国际生物科技合作积累了宝贵经验。中国科学家高效完成任务,获得业界高度评价。
从技术上看,自动化测序仪与计算机数据分析系统的引入是HGP加速的关键。例如,美国华盛顿大学分子生物技术系1992年成立后,推动了大规模自动测序能力,使原定15年计划2003年就基本完成。
主要成果与技术进步
HGP最核心的意义不仅在于获得了完整的人类基因组“蓝图”,更推动了测序技术的革命性降本。例如,测定100万碱基对的成本从1990年的1万美元,到2015年已降至1美元以下。基因测序由高端实验室走向大众应用,极大推动医学与生物学发展。
应用前景与伦理挑战
基因组计划带来了变革式影响:
- 医学方向:通过基因比对快速定位致病基因,如糖尿病、癌症、罕见病等的易感基因,促进了精准医疗——医生可按基因型制定个体化用药和治疗。
- 人类起源与演化:大量基因组数据支持“走出非洲”学说,证实现代人类的全球迁徙路线。
- 伦理思考:基因隐私保护、基因歧视与“定制婴儿”等新问题不断涌现。中国2019年已立法禁止人类生殖细胞的基因编辑,为技术应用划定红线。
化石研究的技术革新
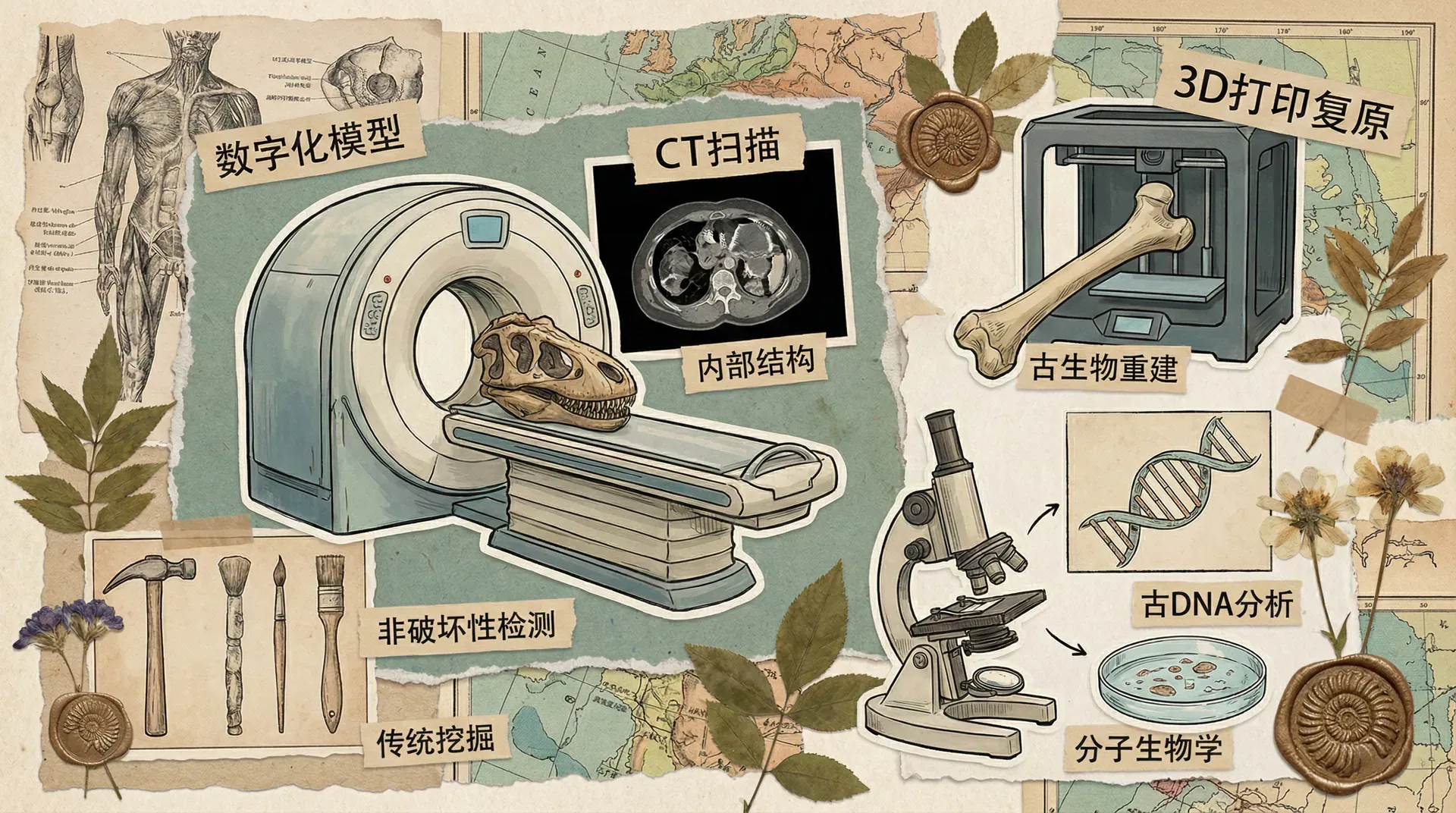
分子生物学飞速发展的同时,古生物学也因新技术焕发新生。以往化石研究主要聚焦“化石剥离与形态观察”,而今天,跨学科技术正让我们揭开地球生命的历史奥秘。
影像与成像技术的突破
医学影像技术,如CT(计算机断层扫描)、显微CT和同步辐射等,成为“无损化石解剖”利器。科学家可通过CT扫描得出完整骨骼或软组织的三维结构,避免传统机械剥离带来的损伤。例如:
- 恐龙骨骼空腔结构:1989年,研究人员用CT扫描恐龙化石,发现类似现代鸟类的中空骨骼,“鸟起源于恐龙”的假说获得重要新证据。
- 化石羽毛印痕:1996年中国辽宁北票市发现中华龙鸟化石,保存有清晰羽毛痕迹,为鸟类起源于恐龙提供了第一手证据;以后又陆续发现小盗龙等多种羽毛恐龙,甚至发现部分羽毛可能服务于保温或炫耀。
- 霸王龙前肢结构:精细CT扫描和力学分析显示霸王龙短小前肢拥有较强力量,颠覆了“霸王龙前肢无用”的印象。
- 鲸类“退化”腿骨:埃及发现5000万年前远古鲸化石,保留小型后肢,证实鲸祖先曾是陆生动物。
化石研究常见技术与举例
澄江生物群(云南,约5.2亿年前)保存有大量寒武纪软体化石,让我们窥见“生命大爆发”时期海洋生物的多样化。
新技术驱动下,古生物学正发展为集地质学、物理学、化学和生物学于一体的交叉学科。无损检测、数字成像和3D打印,让远古生命图景愈加真实。医学影像学与古生物学的结合,是典型的跨界创新范例。
科学进步表明,跨学科融合与技术创新是理解生命演化历程、推动生物科学长足发展的关键动力。
总结
生物学的进步离不开新技术的推动。从医学影像在化石研究中的应用,到胚胎发育调控机制的分子探究,跨学科手段让我们逐步揭开了生命复杂性的面纱。对恐龙骨骼结构和古鲸演化历程的发现,不仅丰富了我们对生物演化历史的认识,也展示了技术革新对科学研究的巨大推动力。在胚胎学方面,分子调控、组蛋白修饰、信号分子梯度等机制的阐明,则为理解生物体的发育规律和疾病防治提供了理论基础。
中国科学家在古生物、发育生物学等领域已取得了世界瞩目的成就,并在干细胞、再生医学等前沿方向积极探索。未来,伴随着多组学技术、人工智能和数据整合的不断发展,生物学研究将愈发精准和系统化,有望带来生命科学与医学的重大突破。综合来看,现代生物学的发展不仅改变了我们对自然与自我的认知,也为人类健康、医疗和可持续发展带来了广阔前景。