胚胎发育的分子机制
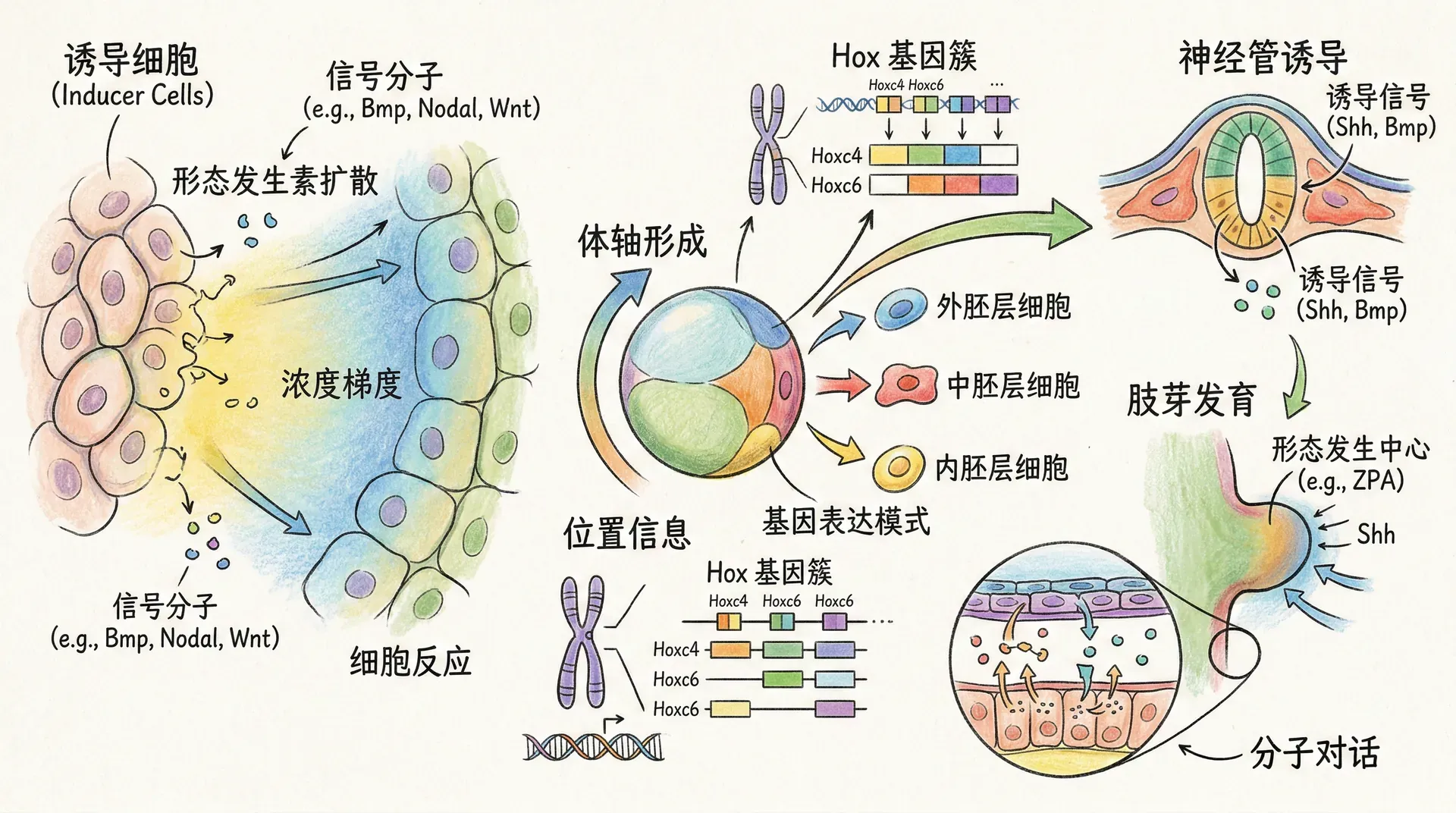
生命的起源一直以来都是生物学中极具魅力且富有挑战性的话题。一个微小的受精卵,如何在受精后的短短数天、数周内,经历细胞分裂、分化和空间重组,最终发育成包括各类组织和器官在内的高度复杂的多细胞生物体,这一过程蕴含着无数精细且动态的分子调控机制。
从最初的受精卵开始,细胞在数量上迅速扩增,同时通过信号传导通路(如Wnt、Notch、Hedgehog等)的调节,决定不同细胞的命运,实现胚层的分化,并逐步形成器官原基。此外,细胞间的相互作用、基因表达的时空调控、表观遗传修饰等环节共同保证了发育过程的精确性和有序性。
正是这些分子与细胞层面的协作,让一个简单的生命单元最终发育为功能完善、结构复杂的个体。本章将系统梳理胚胎发育过程中涉及的关键分子事件,深入介绍受精、早期胚胎发育、细胞命运决定和器官形成等环节,帮助我们全面理解生命初期发育的分子奥秘。
受精与早期胚胎发育过程
受精的分子机制
受精是生命开始的标志性事件,涉及精子与卵子的识别、融合及遗传物质的重组。这一过程包括多个高度特异的分子识别和调控事件,保障了物种的遗传纯度和生命的新起点。
当精子接近卵子时,需首先通过卵子的透明带。精子顶体中的多种水解酶(如透明质酸酶、蛋白水解酶)协助分解透明带使精子顺利穿越。在人类及大多数哺乳动物中,精子表面存在特异性结合蛋白(如ZP3结合蛋白),能够识别并结合卵子透明带上的ZP3糖蛋白,这种作用具有种属特异性,确保了不同物种之间不会互相受精。
精子与卵子质膜的融合是受精的关键环节。精子质膜上的融合蛋白(如IZUMO1)与卵子质膜上的受体蛋白(JUNO)相互作用,诱发两者膜的融合,为遗传物质的结合创造条件。这一机制虽然类似病毒入侵细胞,但调控更加严密。
受精后,卵子会迅速启动防止多精入卵的机制,包括膜电位的快速去极化(快速反应)及皮质颗粒释放(慢反应)等,确保仅有一个精子的遗传物质进入卵子,防止多倍体胚胎的产生。
受精后的细胞激活
精子进入卵子后,释放名为精子因子的蛋白(在哺乳动物为PLCζ),能够催化卵子胞质内的PIP2水解,产生IP3和DAG。IP3作用于内质网上的受体,导致钙离子的释放,形成反复的钙振荡。
钙振荡是卵子激活的核心事件。它持续数小时,每15-20分钟出现一次钙峰。这类周期性变化能够激活多种钙依赖性信号蛋白,如CaMKII,启动细胞周期、蛋白质合成,并降解细胞周期抑制因子,为胚胎后续发育打下基础。
上图展示了哺乳动物卵子受精后胞质内钙离子浓度的周期性变化。这种钙振荡是卵子激活的分子标志,对后续细胞分裂及胚胎发育至关重要。
原核形成与核融合
精子和卵子的细胞核在受精后发生显著变化:精子核高浓缩染色质解凝,重新形成核膜,成为雄原核;卵子完成第二次减数分裂后形成雌原核。两者在胞质中借助微管系统相向移动,靠近但不彻底融合,直到第一次有丝分裂,核膜共同解体,染色体在同一纺锤体上排列,实现遗传物质的真正结合。
近年来,中国科学家利用斑马鱼和小鼠模型深入研究发现,原核的移动速度和相遇位置均受卵子内母源因子控制,这些因子的储备为胚胎早期发育提供坚实物质基础。
卵裂,囊胚形成与着床
卵裂的特点与分子调控
受精后,合子开始一系列快速的细胞分裂——卵裂。卵裂特征为几乎不增长总体积,仅持续分割胞质以增殖细胞数,所需蛋白和RNA主要依赖卵母细胞阶段储备的母源性物质。
哺乳动物卵裂为全裂且不完全规律,第一次分裂产生两枚等大卵裂球,此后分裂的时间和方向则常不同步。有的动物如鸟类、爬行动物,则由于卵黄丰富而采用盘裂模式——分裂仅限于一个细胞极端。
早期卵裂周期由母源性细胞周期蛋白和依赖性激酶(如Cyclin、CDK)驱动。这些调控因子在卵子成熟中已提前储备,用于支持分裂的高速度。
卵裂阶段细胞周期极度缩短或缺失G1、G2期,仅保留DNA复制和有丝分裂阶段,如果蝇早期胚胎细胞周期仅需8-10分钟,非洲爪蟾约30分钟。
桑椹胚与致密化
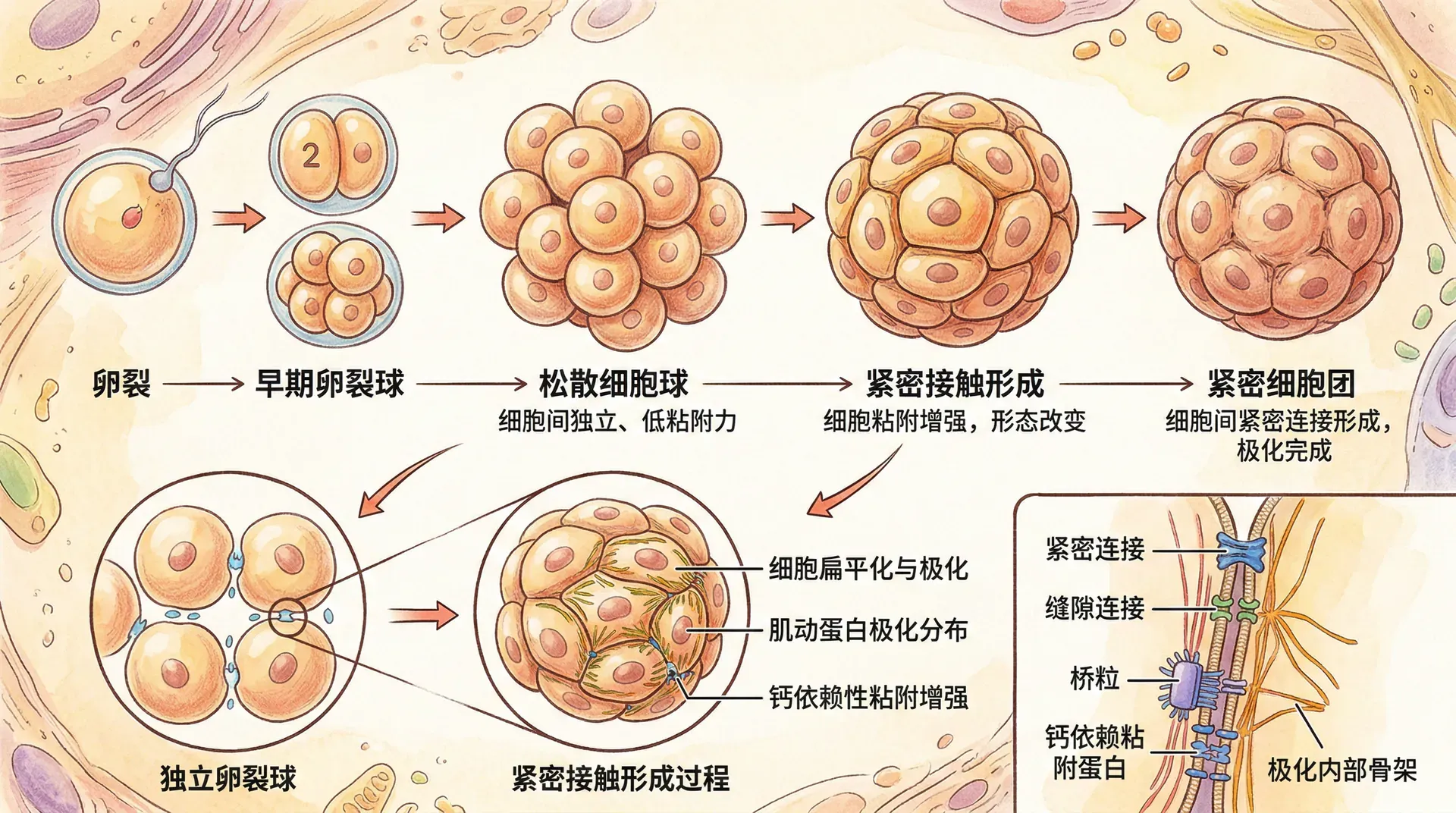
随着卵裂进行,胚胎达到16-32细胞期时外观类似桑椹果实,称为桑椹胚。此时,胚胎细胞之间由松散转为紧密聚集,称为致密化。
致密化依赖细胞间连接蛋白(如E-钙黏蛋白)的表达和局部化。E-钙黏蛋白在细胞接触处高度富集,通过钙离子依赖的同源相互作用牢固连接细胞。致密化的同时,外层细胞开始展现顶-基底极性,为后续囊胚腔的形成奠定基础。
囊胚形成与细胞分化
桑椹胚发育后,外层细胞通过主动转运将钠离子泵入胚胎中央,水分随之渗透形成囊胚腔,使胚胎进入囊胚阶段。这一阶段首次发生明显的细胞命运分化:
- 囊胚外层:滋养层细胞(将发育为胎盘等支持结构)
- 囊胚一侧内部:内细胞团(将发育为胎体及部分胚外组织)
调控上述命运分化的主要转录因子有:
胚胎着床
囊胚需在子宫内膜完成着床后方可继续发育。着床大致分为三个阶段:定位、黏附、侵入。
中国学者近年来发现,子宫内膜在“着床窗口期”会特异性表达多种microRNA,这些小分子通过调控靶基因影响子宫容受性,为解决不明原因的不孕及反复着床失败提供新思路。
原肠胚形成与三胚层分化
原肠胚形成的意义
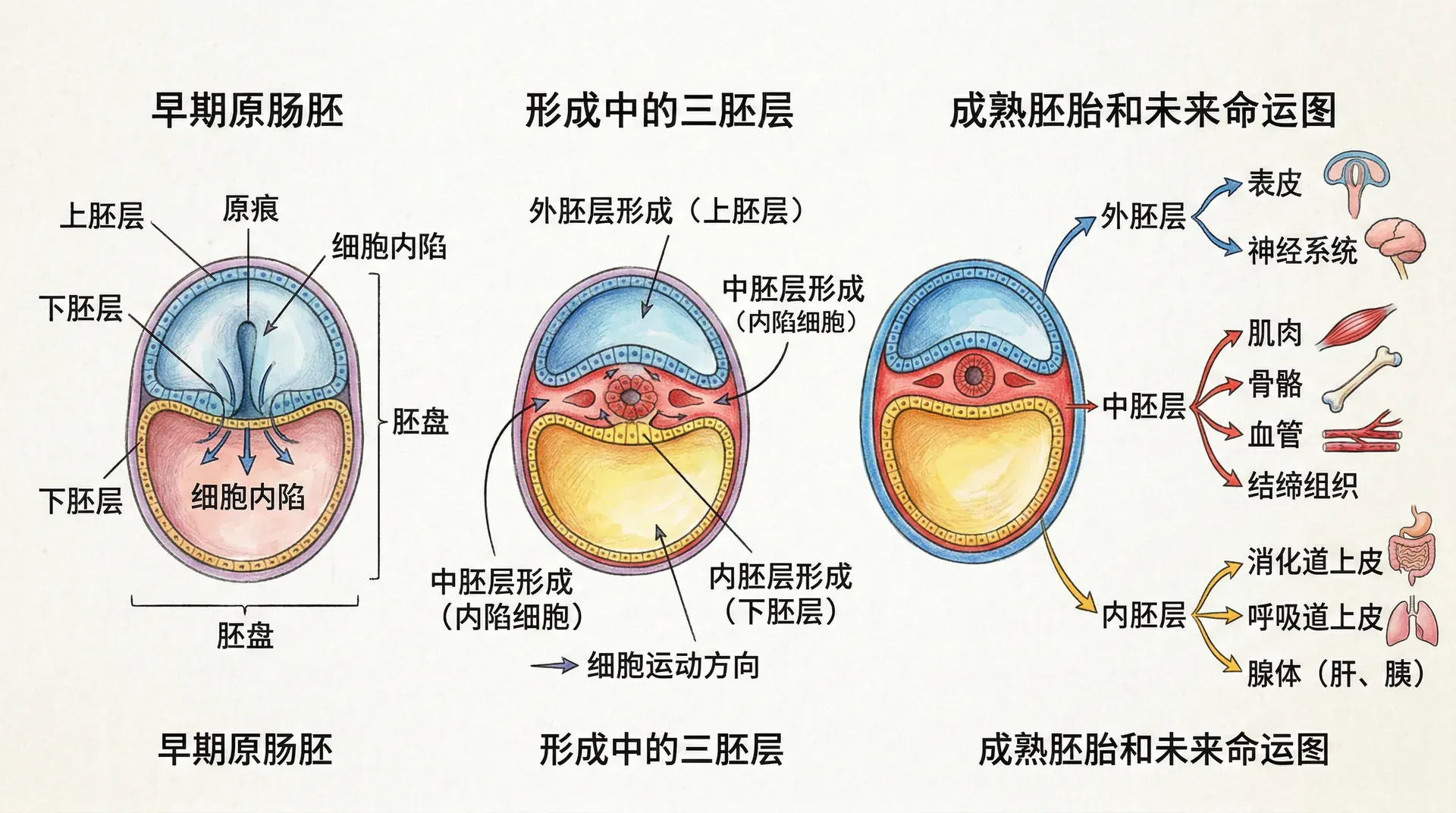
原肠胚形成(gastrulation)是胚胎发育的关键事件。刘易斯·沃尔珀特曾说:“人一生中最重要的时刻不是出生、结婚或死亡,而是原肠胚形成。”该阶段单层细胞转变为三层胚盘(外、中、内胚层),为后续器官形成奠定基础。原肠胚形成伴随细胞大规模迁移、变形与重排,需要复杂分子信号网络精确调控。
原肠胚形成的过程
在哺乳动物中,原肠胚形成始于着床后。内细胞团先分化为上胚层和下胚层,上胚层将发育成胚胎主体。随后,上胚层一侧形成原条,标志着前后轴建立。细胞向原条迁移、内陷,最早进入的细胞取代下胚层,形成真内胚层;后续内陷细胞形成中胚层,留在表面的为外胚层。
原肠胚形成期间的异常可能导致神经管闭合不全、脊柱裂等严重先天缺陷,因此该阶段极其敏感,极易受药物、辐射等外界不良因素影响。
三胚层的命运
三胚层各具命运,未来发育成不同系统与器官:
外胚层主要形成神经系统与表皮。中胚层形成脊柱骨骼、骨骼肌、泌尿生殖、心血管等系统。内胚层则内衬消化及呼吸道,衍生肝脏、胰腺、甲状腺等器官。中胚层与内胚层间常存互相诱导与支持的分化合作。
原肠胚形成的分子调控
原肠胚形成依赖多条信号通路精密调控,主要包括Wnt、Nodal及BMP路径:
- Wnt信号主导原条形成与中胚层分化,在胚胎后侧高表达,激活关键基因(如Brachyury)。
- Nodal信号(TGF-β家族成员)调控前后轴与原条形成,其浓度梯度决定内-中胚层命运:高浓度诱导内胚层,中等诱导中胚层。
- BMP信号主控背腹轴—背侧信号被抑制,神经组织分化;腹侧BMP高表达则促使表皮、血液等分化。
这些信号相互作用、反馈环环相扣。例如,Wnt促进Nodal表达;Nodal又可诱导Wnt抑制因子等,形成自限负反馈网络,实现空间-时序的精准调控。
胚胎极性与体轴建立
体轴的概念
多细胞生物体具有明确的空间组织,不同的身体结构在特定的位置有序排列,这一空间模式依赖体轴的建立。脊椎动物胚胎拥有三大主要体轴:
体轴的建立始于早期胚胎,部分物种甚至在卵子形成时就为体轴铺垫了分子基础。体轴建立的核心机制包括分子的非对称分布、局部信号中心定位及空间化的基因表达等。
前后轴的建立
前后轴决定胚胎头部与尾部。哺乳动物中,原条(primitive streak)的出现位置界定后端,而相对区域则为前端。其分子基础简要梳理如下表:
Wnt信号在后侧高表达,相关拮抗剂(如Dkk1、Sfrp)前侧表达,形成“前低后高”的梯度。同理,Nodal信号及其拮抗剂沿前后轴分布,协同决定原条位置与轴性。
前后轴确立之后,胚胎中会出现一系列转录因子的空间梯度表达,其中最具代表性的是HOX基因。HOX基因在染色体上的排列顺序与其在前后轴上的表达顺序高度一致,这种现象被称为“共线性”。不同的HOX基因组合决定了胚胎各体节区段的发育命运,例如颈椎、胸椎和腰椎等结构的特异性由各自的HOX表达谱共同确定。
背腹轴的建立
背腹轴决定神经系统(背)与血液表皮系统(腹)的区分。这一轴的确立主要依赖BMP信号梯度:
两栖类中,“组织者”如施佩曼组织者区域分泌Chordin、Noggin、Follistatin等BMP拮抗剂,BMP信号被抑制促进神经诱导。腹侧无拮抗剂,BMP活跃,促腹侧结构生成。哺乳动物虽无典型“组织者”,但前侧内胚层(AVE)分泌Wnt/Nodal拮抗剂,依旧调控轴性。
左右轴的建立
左右轴的建立打破了身体的对称性,使如心脏、肝脏等器官产生明确的左右区分。
左右不对称的分子机制如下:
- 节点(node)中的纤毛细胞自发旋转,形成“节点流”(nodal flow),将Nodal蛋白等信号定向推向左侧。
- 左侧中胚层激活Nodal、Lefty2、Pitx2等信号/转录因子,启动左侧器官发育程序。
- 右侧则有Nodal抑制剂,维持右侧信息。
例如,Pitx2为左侧发育关键调控因子。纤毛结构异常可造成内脏镜像(situs inversus)。如DNAH5、DNAH11基因突变影响纤毛运动,即可导致此类罕见现象。
发育过程中的基因表达调控
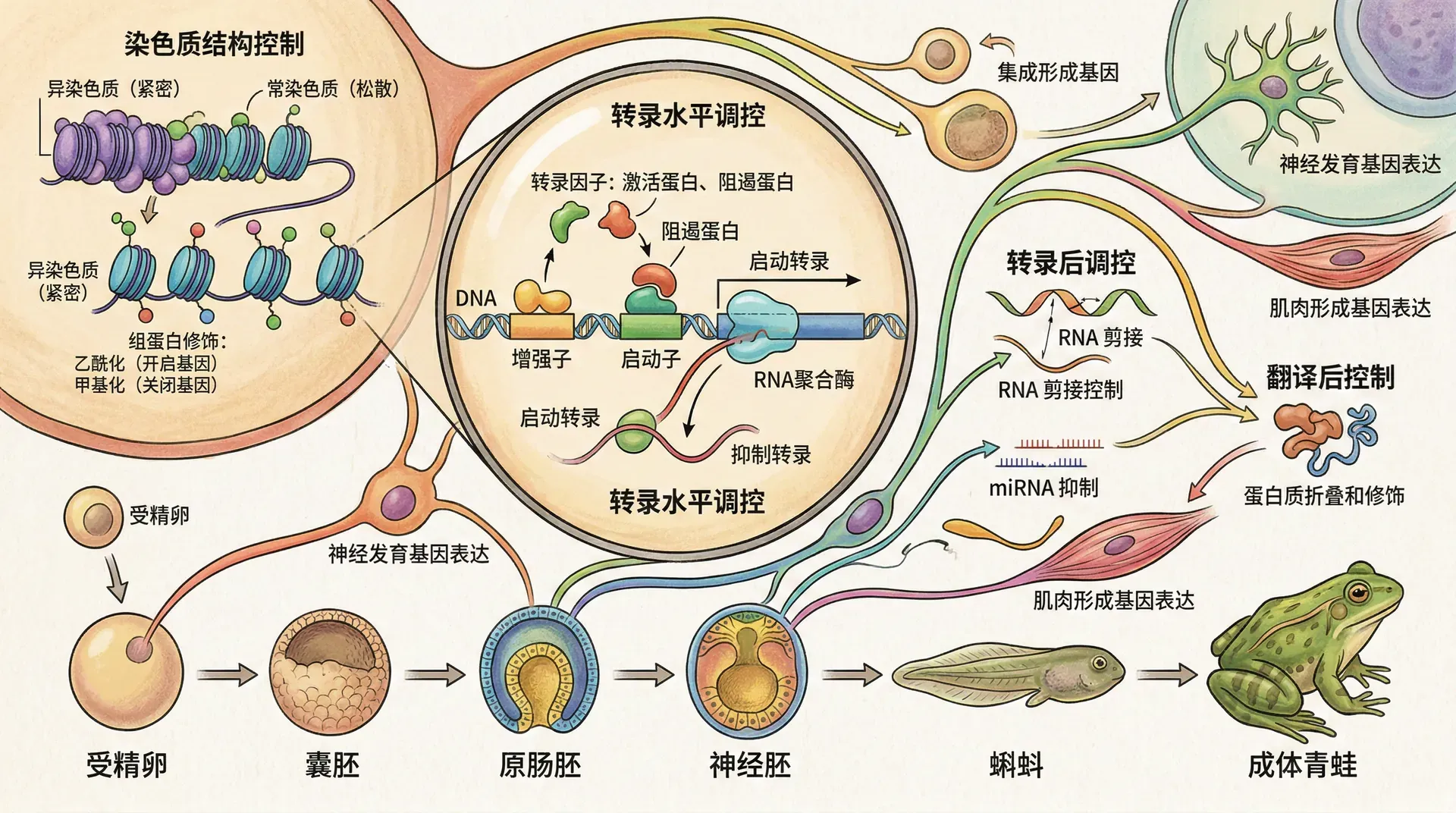
母源性向合子性转换(MZT)
早期胚胎先依赖母源性mRNA/蛋白储备,随着卵裂,母源性逐步耗竭,之后合子基因组被激活(ZGA):
- 小鼠:2细胞期ZGA
- 人类:4-8细胞期ZGA
- 斑马鱼:受精后约3小时ZGA
ZGA过程中,发生染色质重塑和母源mRNA的降解。表观遗传机制(如染色质开放、组蛋白修饰、DNA甲基化变化)极为关键。例如,清华大学团队运用单细胞转录组,绘制人类胚胎ZGA时刻的表达图谱,识别数百个特异激活基因。
转录调控网络
发育调控依赖复杂网络,一些核心转录因子起“主调控因子”作用:
例如,实验中将MyoD导入成纤维细胞,可直接将其诱导为肌细胞,体现主调控因子的决定性力量。
调控网络常见以下环路结构:
- 正反馈:维持细胞状态的稳定性
- 负反馈:产生周期性/振荡(如体节发育)
- 前馈环路:响应信号时过滤“噪音”
信号转导与形态发生素梯度
细胞如何“感知”自身空间位点?答案是形态发生素梯度。
常见形态发生素比较:
以Shh为例,沿神经管背腹轴形成浓度递减梯度,不同浓度激活互斥的转录因子组合,从而指定区域特别的神经元亚型。现代成像技术提升了对梯度形成/解读的实时分析,揭示其调控的动态变化。
表观遗传调控
DNA序列之外,表观遗传层级调控基因激活/沉默。代表修饰有:
DNA甲基化:启动/沉默基因表达,两轮重编程分别发生在受精后与原始生殖细胞发育期
组蛋白修饰(甲基化、乙酰化等):形成组蛋白密码,决定染色质活性
- H3K4me3 :活跃转录标记
- H3K27me3:基因沉默标记
染色质重塑:调节DNA结构及可及性
蛋白复合体:
- Polycomb复合体:维持沉默状态,调控HOX等基因
- Trithorax复合体:维持激活状态,两者拮抗协调
上图比较了不同调控机制在发育不同阶段的重要性。可见,信号通路(如形态发生素)在早期胚胎占主导,随着发育,表观遗传和转录因子调控地位提升,器官形成期则细胞间互作更为关键。
非编码RNA的调控作用
非编码RNA在发育调控中的作用不可忽视,典型代表如下:
miRNA主要通过与mRNA的3'UTR结合,抑制其翻译或促进降解。例如,miR-430在斑马鱼的ZGA(基因组激活)阶段高表达,能够有效促进母源mRNA的清除;而miR-1和miR-133则参与心脏和骨骼肌的分化调控,敲除这些miRNA会导致严重的发育缺陷。
lncRNA的作用机制多以“招募效应”为主,即通过吸引表观遗传修饰蛋白(例如Polycomb复合体)到特定基因位点,从而调控目标基因的状态。典型的例子是Xist lncRNA,它可以促使雌性哺乳动物的X染色体失活,是发育调控中的经典案例。除此之外,piRNA、circRNA等也被逐步证实调控发育过程,未来有望揭示更多分子层面新机制。
总结
我们探讨了胚胎发育的分子机制,从单个受精卵到三胚层胚盘的形成,这个过程体现了生命发育的精密性和复杂性。受精启动了一系列的发育程序,卵裂将庞大的合子分割为多个细胞,囊胚形成标志着第一次细胞分化,原肠胚形成建立了三胚层和体轴系统。这些形态学变化的背后是分子水平的精确调控,包括信号转导、转录调控、表观遗传修饰等多个层面。
理解胚胎发育的分子机制不仅具有理论意义,也有重要的应用价值。在临床上,许多出生缺陷源于胚胎发育早期的异常,了解这些机制有助于出生缺陷的预防和诊断。在再生医学领域,胚胎发育的原理被应用于干细胞分化和组织工程。在进化生物学中,比较不同物种的发育过程揭示了生命演化的历史。随着技术的进步,我们对胚胎发育的理解将更加深入,为人类健康和生命科学的发展做出更大贡献。
本节练习
1. 关于受精过程,下列哪一项说法是正确的?
A. 精子表面的ZP3结合蛋白识别卵子透明带上的ZP3糖蛋白,实现种属特异性结合。
B. 受精后卵子无任何机制防止多精入卵。
C. 精子与卵子的结合只需穿越卵黄膜,无需穿越透明带。
D. 防止多精入卵的唯一机制是卵子质膜去极化。
答案:A
解析:
- 精子通过表面的ZP3结合蛋白特异性识别并结合卵子的ZP3糖蛋白。
- 受精后,卵子先发生膜去极化(快反应),紧接着皮质颗粒反应导致透明带硬化(慢反应),共同防止多精入卵。
- 精子必须穿越透明带后才能与卵细胞膜融合。
知识点: 受精的分子机制、防止多精入卵的机制
2. 囊胚包含两种主要细胞类型:滋养层细胞和内细胞团。请完成下表,填写这两种细胞类型的关键转录因子和发育命运。
答案:
这些转录因子之间存在相互抑制关系:CDX2抑制OCT4的表达,而OCT4也抑制CDX2,确保两种细胞命运的清晰分离。
知识点: 囊胚的细胞分化、转录因子在细胞命运决定中的作用
3. 下列哪一组组织/器官全部起源于外胚层?
A. 心脏、骨骼肌、肾脏
B. 肝脏、肺上皮、胰腺
C. 脑和脊髓、皮肤表皮、神经嵴细胞
D. 肺上皮、皮肤表皮、骨骼肌
答案:
C. 脑和脊髓、皮肤表皮、神经嵴细胞
解析:
- 外胚层主要形成神经系统和表皮。神经嵴细胞虽然来源于外胚层,但可进一步分化成许多组织。
- 中胚层主要生成心脏、骨骼肌、肾脏等。
- 内胚层主要生成肝脏、肺上皮、胰腺等。
知识点: 三胚层的发育命运、器官的胚层来源
4. 形态发生素通过形成浓度梯度来传递位置信息。请举例说明BMP信号在背腹轴建立中的作用,并解释为什么背侧能够形成神经组织。
答案:
BMP(骨形态发生蛋白)信号在背腹轴建立中起关键作用,其活性梯度决定了背侧和腹侧组织的分化:
- 背侧(低BMP活性): 组织者区域分泌BMP拮抗剂(Chordin、Noggin、Follistatin),抑制BMP信号活性。在BMP信号被抑制的情况下,外胚层细胞默认分化为神经组织,这个过程称为神经诱导。
- 腹侧(高BMP活性): 缺乏BMP拮抗剂,BMP信号保持活跃,促进腹侧组织(如表皮和血细胞)的形成。
- 中间区域(中等BMP活性): 形成中间性质的组织。
神经组织形成的原理: 外胚层细胞的"默认命运"是神经,只有在BMP信号存在时才会转变为表皮。因此,背侧组织者通过抑制BMP信号,"解除"了对神经分化的抑制,使得背侧外胚层能够形成神经板,进而发育为神经系统。
知识点: 形态发生素梯度、BMP信号在背腹轴建立中的作用、神经诱导机制
5. 请解释什么是母源-合子转换(MZT),这个过程在不同物种中发生的时间有何差异?为什么这个转换对胚胎发育至关重要?
答案:
母源-合子转换(Maternal-to-Zygotic Transition, MZT) 是指早期胚胎从依赖母源性(卵子中储备的)mRNA和蛋白质转变为依赖胚胎自身基因组转录的发育过程。
不同物种MZT发生时间:
- 小鼠:2-细胞阶段(受精后约24-30小时)
- 人类:4-8细胞阶段(受精后约2-3天)
- 斑马鱼:受精后约3小时
- 果蝇:受精后约2-3小时
MZT的重要性:
- 基因组激活: 标志着胚胎自身基因组开始大量转录,摆脱对母源因子的完全依赖。
- 母源mRNA清除: 许多母源mRNA在此期间被降解,为新转录的mRNA腾出空间,确保发育程序的精确执行。
- 染色质重塑: 伴随表观遗传重编程,建立胚胎特异的染色质状态。
- 发育控制权转移: 从母体控制转向胚胎自主控制,是胚胎发育的关键转折点。
如果MZT不能正常进行,胚胎通常会在此阶段停止发育,这也是为什么许多胚胎在体外培养中会在这个阶段发育停滞。
知识点: 母源-合子转换、合子基因组激活、早期胚胎的转录调控
6. 原肠胚形成被认为是胚胎发育过程中最为关键的事件之一。请从细胞行为、组织层次变化和发育意义三个方面,阐述原肠胚形成的重要性。并结合实例说明,为什么这一时期被称为发育的“敏感期”。
答案:
原肠胚形成(gastrulation)是胚胎发育的核心事件,其重要性可以从以下三个方面理解:
一、细胞行为的复杂性
原肠胚形成涉及大规模、高度协调的细胞运动和重排,包括:
- 细胞内陷: 上胚层细胞通过原条向胚胎内部迁移,改变形状从柱状变为瓶状。
- 细胞迁移: 内陷后的细胞在胚层之间定向迁移,找到目的位置。
- 细胞间黏附变化: 细胞通过改变黏附分子(如钙黏蛋白)的表达,与旧邻居分离,与新邻居建立联系。
- 细胞极性重建: 迁移过程中细胞建立新的极性,适应新的组织环境。
这些细胞行为需要精确的时空调控,任何环节出错都可能导致发育异常。
二、组织层次的转变
原肠胚形成使胚胎从单层或双层结构转变为三胚层结构:
- 外胚层: 将来形成神经系统和表皮
- 中胚层: 形成肌肉、骨骼、循环系统等
- 内胚层: 形成消化道和呼吸道内衬及其衍生器官
三胚层的建立为后续的器官发生奠定了基础。每个胚层都有特定的发育命运和基因表达程序,这种组织层次的建立是复杂生物体形成的前提。
三、发育意义
原肠胚形成不仅建立了胚层,还确立了:
- 体轴系统: 原条的出现明确了前后轴,为后续的背腹轴和左右轴建立创造条件。
- 组织相互作用: 三个胚层建立后,彼此之间开始复杂的信号交流,这种组织间诱导是器官发生的驱动力。
- 细胞命运决定: 细胞的最终位置决定了它接收的信号环境,从而决定了分化方向。
为什么是“敏感期”?
原肠胚形成期被称为发育的“敏感期”或“致畸敏感期”,原因包括:
-
快速的细胞分裂和分化: 细胞处于高度活跃状态,DNA复制频繁,更容易受到化学物质和辐射的损伤。
-
关键发育事件集中: 体轴建立、胚层分化、器官原基形成都在此期间进行,任何干扰都可能产生广泛影响。
-
缺乏修复机制: 此时期的细胞检查点机制尚不完善,异常细胞可能继续分裂,导致大范围的发育缺陷。
实例说明:
- 神经管缺陷: 如果原肠胚形成期间叶酸缺乏或受到某些药物(如抗癫痫药)影响,神经管可能无法正常闭合,导致脊柱裂或无脑畸形。
- 先天性心脏病: 心脏原基在原肠胚期开始形成,此时暴露于致畸因子(如风疹病毒、酒精)可能导致心脏发育异常。
- 肢体畸形: 反应停(沙利度胺)在上世纪60年代造成大量肢体缺陷婴儿的悲剧,正是因为该药物在胚胎器官形成早期(包括原肠胚期)干扰了正常的细胞增殖和分化。
因此,孕早期(特别是妊娠第3-8周,对应胚胎的原肠胚期和器官形成期)应特别注意避免接触有害物质,补充叶酸等营养素,以降低出生缺陷的风险。
知识点: 原肠胚形成的过程、三胚层的建立、胚胎发育的敏感期、致畸因素对早期胚胎的影响