身体如何保持内在平衡
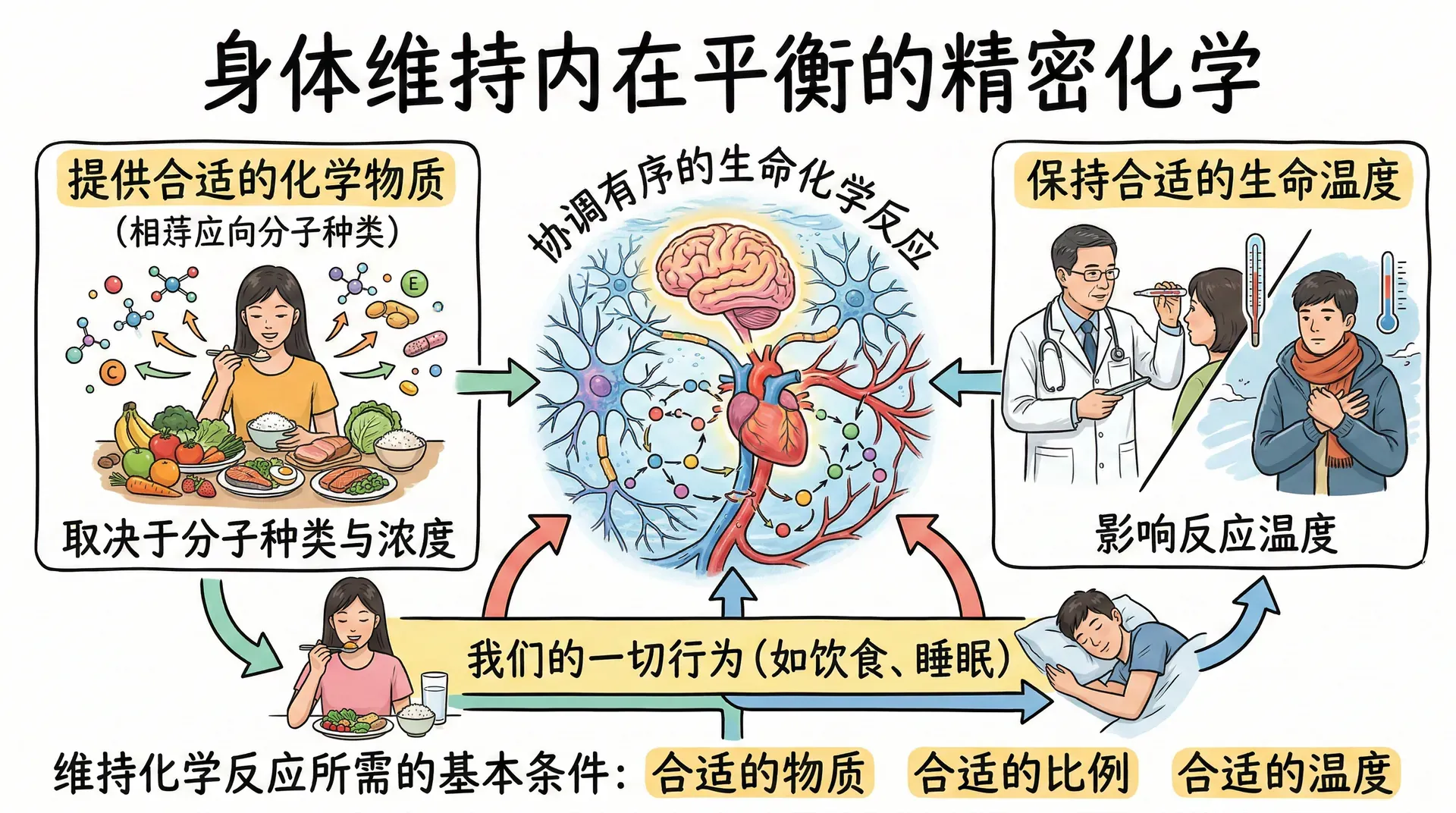
生命是什么?从医学、法律、哲学还是诗歌的角度,我们都可以给出不同的定义。但从生物学的角度来看,生命的必要条件是一系列协调有序的化学反应。并非所有的化学反应都代表着生命,但所有的生命活动都依赖于精密调控的化学反应。每一个活体内的化学反应都发生在水溶液中,其速度取决于水中分子的种类、浓度以及溶液的温度。我们的一切行为,从饮食到睡眠,都是在维持这些化学反应所需的基本条件——合适的化学物质、合适的比例,以及合适的温度。
地球上所有的生命都离不开水,动物会在任何能找到水的地方饮用它。这种对水的依赖不仅仅是生存需要,更是生命化学反应得以持续进行的根本基础。
温度调节与生存策略
温度是影响化学反应速率最直接的因素之一。对动物而言,体温的维持不是一件被动的事,而是一套精密的主动调控系统。从行为层面的选择,到生理层面的自动响应,不同物种在漫长的进化历程中形成了各自独特的体温管理方式。理解这些策略,也是理解行为背后生理驱动力的起点。
恒温动物与变温动物
动物界存在两种主要的温度调节策略。两栖动物、爬行动物和大多数鱼类是变温动物,体温随环境温度变化而波动。少数大型鱼类,如鲨鱼和金枪鱼,是例外,它们能将核心体温长期维持在高于周围水温的水平。
变温动物缺乏颤抖、出汗等生理调温机制,但这并不意味着它们对体温毫无控制。“冷血动物”这个说法其实有些误导,沙漠蜥蜴会在阳光区域、阴影区域和洞穴之间不断移动,通过行为选择来维持相当稳定的体温。哺乳动物和鸟类是恒温动物,通过生理机制维持近乎恒定的体温。部分物种在冬眠期间会暂时转为变温状态,这是一种节能适应。
维持恒温的代价对小动物而言尤为高昂。动物产生的热量与其总质量成正比,而散失的热量与其体表面积成正比。老鼠、蜂鸟等小型恒温动物的表面积与体积比很高,散热极快,因此每天必须消耗大量食物才能维持体温。
体温调节的行为与生理机制
体温调节包含两个层面:行为调节和生理调节。行为调节更为古老,变温动物完全依赖它;恒温动物则在此基础上叠加了精密的生理机制。
观察鸟类的日常行为,可以发现许多有趣的体温调节细节。海鸥和鸭子在寒冷天气中习惯单腿站立,将另一条腿收入腹部羽毛之间以减少散热。鸟类还会通过张嘴喘气来散热,原理与狗的喘气一致——加速水分蒸发带走热量。冬季,许多鸟类会将羽毛蓬松,在羽毛间形成隔热的静止空气层;夏季则将羽毛贴紧身体,便于散热。
在生理层面,当气温高于体温时,蒸发散热是唯一有效的降温途径。人类通过出汗将水分暴露在皮肤表面,蒸发时带走大量热量。不会出汗的动物则通过舔舐皮毛或持续喘气来达到同样效果。值得注意的是,当空气既热又潮湿时,水分蒸发受阻,这一机制的效率会大幅下降,这也是湿热天气比干热天气更令人难受的原因。
在寒冷环境中,身体会启动多种机制来增加产热、减少散热。
-
颤抖是最直接的产热方式。肌肉不停收缩,代谢产生的热量迅速积累,这是身体应对突发寒冷的第一道防线。
-
皮肤血管收缩,减少流向体表的血流,使血液集中在核心器官周围,降低体表散热速率。
-
对大多数哺乳动物而言,寒冷时竖起毛发能在皮肤表面形成隔热层。人类保留了这一反射,寒冷时皮肤上的细小毛发会竖起,这便是俗称的“鸡皮疙瘩”现象。在远古祖先毛发浓密的年代,这一机制有实际的保温效果。
《黄帝内经》中提到“春夏养阳,秋冬养阴”,古人凭借长期观察总结出人体需要随季节调整生活方式。现代研究印证了这一直觉:许多动物和人类在秋季会增加体脂储备,春季则消耗减少。即便室温保持恒定,人体在白天维持的核心温度也高于夜晚,这种随情境变化的设定点调整,正是适应性调节的体现。
恒温的代价与体温的进化边界
维持恒定体温是一项代价高昂的进化投资。哺乳动物大约三分之二的总能量用于维持体温,也就是常说的基础代谢。变温动物的基础代谢水平远低于此,所需食物也少得多。既然成本如此之高,恒温必然提供了某种不可或缺的生存优势,否则自然选择早就将它淘汰。
高体温的生存优势
随着水温降低,变温鱼类必须调动越来越多的快肌纤维才能维持正常游速,而快肌纤维疲劳速度远比慢肌纤维快。在同等寒冷的环境下,鱼的运动能力已经大打折扣,而哺乳动物的肌肉始终处于最适温度,随时可以全力爆发。这在逃脱天敌或追捕猎物时意味着决定性的优势。
简单来说,恒温动物用大量的食物换来了在任何气候条件下都能高效运动的能力。这是一场以能量换时机的进化博弈,而哺乳动物和鸟类选择了“随时在线”的策略。
37°C的由来
为什么哺乳动物进化出37°C,而不是更高或更低的温度?
-
温度越高,化学反应速率越快,肌肉运动效率越高,但维持所需的能量消耗也同步增加。
-
超过40°C至41°C,蛋白质开始变性,失去正常功能。蛋白质的酶活性依赖其三维构象的灵活性,温度过高会使其结构崩解,就像煮熟的鸡蛋白再也无法还原一样。鸟类的体温约为41°C,已处于临界边缘。
虽然理论上可以进化出耐高温蛋白质——某些嗜热菌确实能在沸水中存活——但这类蛋白质需要大量额外的化学键来维持结构稳定,结构过于僵硬后反而失去了催化活性。37°C是在运动效率和蛋白质稳定性之间找到的最优平衡点。
生殖细胞的温度需求是一个有趣的例外。鸟类将卵产在体外孵化,而非留在体内,原因之一就是体内温度对早期胚胎过高。雄性哺乳动物的阴囊悬挂在体外,也是出于同样的原因——精子的产生需要比核心体温低约2°C的环境。
大脑对体温的调控
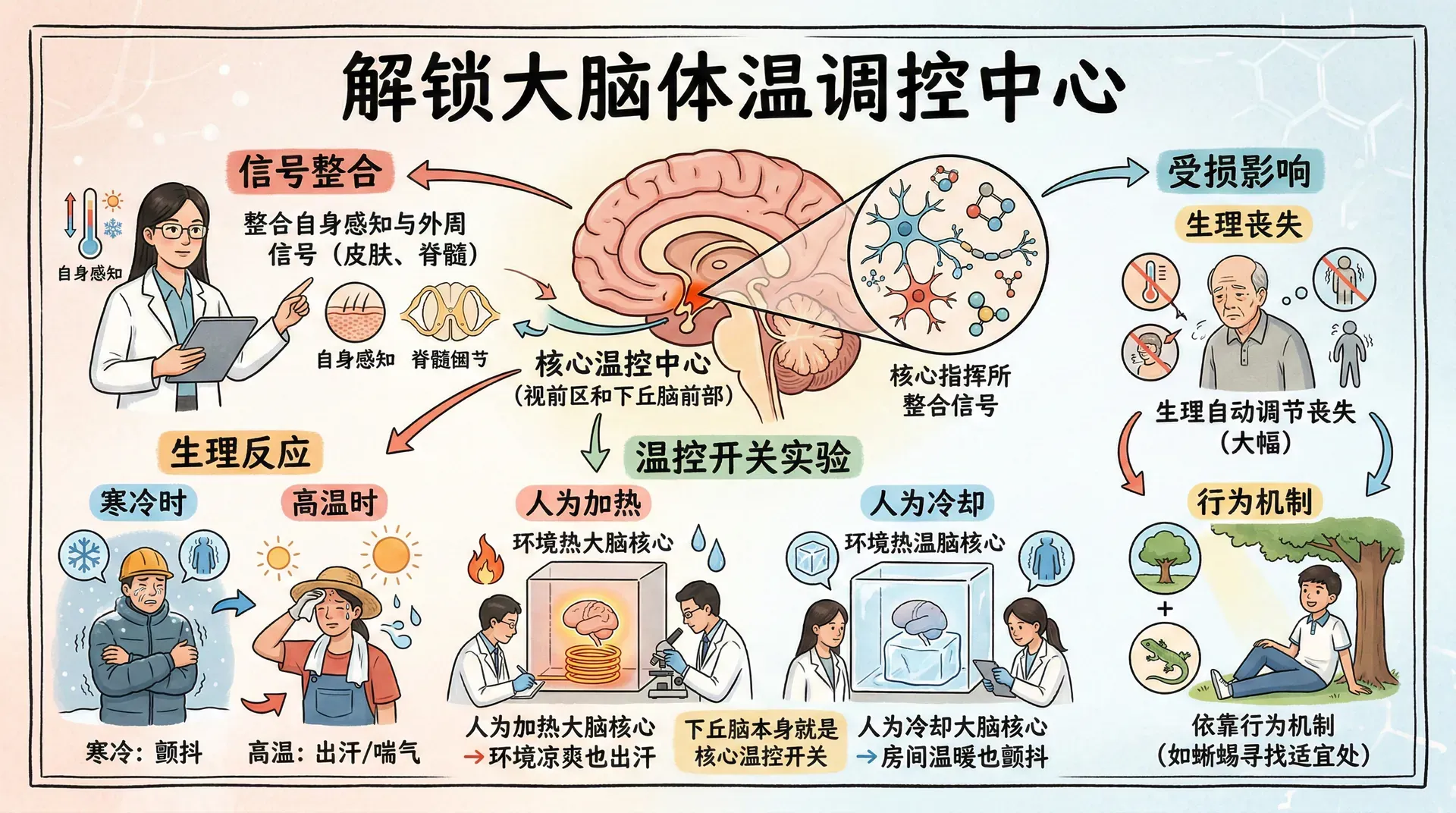
调节体温的生理变化,如颤抖、出汗和皮肤血流改变,都受控于下丘脑内及附近的区域,主要是视前区和下丘脑前部。由于两者关系密切,研究人员通常将它们视为一个功能单元共同讨论。
视前区和下丘脑前部不仅通过感知自身温度来监测体温,还整合来自皮肤和脊髓温度感受器的信号。当该区域和外周感受器同时检测到寒冷时,颤抖反应最为剧烈;当两者都检测到高温时,出汗或喘气反应最为明显。如果该区域受到人为加热,即便环境凉爽,动物也会出汗;反之,人为冷却该区域,动物即便身处温暖的房间也会颤抖,这说明下丘脑本身就是体温的核心“温控开关”。
即便这一区域受损,哺乳动物仍能依靠行为机制调节体温,就像蜥蜴那样寻找更温暖或更凉爽的地方。但生理层面的自动调节能力会大幅丧失。
发热的防御意义
细菌和病毒感染通常会引起发热,即体温的整体升高。发热并非疾病本身,而是身体主动启动的防御手段。当病原体入侵时,白细胞被动员起来,释放细胞因子攻击入侵者。细胞因子还会刺激迷走神经,向下丘脑发送信号,促使前列腺素大量释放。下丘脑特定核团的前列腺素受体一旦被激活,体温设定点便会上调,发热随之产生。
发热代表的是体温设定点的整体上移,而非简单的体温失控。当设定点升至39°C时,身体会主动将体温维持在这一水平,低于时颤抖产热,高于时出汗散热。走进凉爽的房间并不会退烧,因为大脑仍在努力维持那个更高的温度目标。
发热对某些类型的细菌确实有抑制作用,高温环境下细菌的繁殖速度会明显下降。同时,发热还能增强免疫细胞的活性,在细菌感染中提高个体的存活概率。但这种防御收益有明确的上限:超过39°C的发热弊大于利,超过41°C则具有生命危险。
身体在体温调节上采取了多重保障机制。生理机制与行为机制并行运作,某一环节失效时,其他机制会立即补偿。这种冗余设计,是生命系统在漫长进化中形成的稳健性策略。
渴觉与水分调控
水分约占哺乳动物体重的70%。体液中溶质的浓度直接决定了每一个细胞内化学反应的速率,因此水分含量必须被严格维持在一个狭窄的范围内。此外,循环系统需要足够的液体来维持正常血压,保证营养物质和氧气的运输。人在缺乏食物的情况下可以存活数周,但缺水数天便会威胁生命。
不同物种形成了截然不同的水分管理策略。生活在长江流域的河马和水牛大量饮水,吃水分充足的食物,排出稀释的尿液;生活在西北沙漠的跳鼠和沙狐则几乎不需要主动饮水,完全靠食物中的水分维持,并通过排出极干燥的粪便、高度浓缩的尿液以及减少皮肤蒸发来节约每一滴水。
人类在水分管理上具备相当的弹性。当饮水不足时,脑下垂体后叶会分泌加压素,肾脏随即从尿液中大量回收水分,排出更浓缩的尿液,汗液分泌也同步减少。睡眠期间加压素分泌增加,正是为了在无法饮水的数小时内尽量保存体内水分。加压素还能收缩血管,帮助维持血压。
在正常情况下,多数人的饮水行为发生在进餐或社交场合,并不依赖强烈的渴觉驱动。大量饮水之后,多余的水分会通过尿液排出。身体更倾向于处于轻度水分过剩的状态,因为这比脱水更安全,代价也更低。
渗透性渴觉与低血容量性渴觉
渴觉并非一种单一的感受,而是由两种机制分别触发,分别对应不同的身体状态。
渗透性渴觉由体液浓度升高触发。进食咸味食物后,钠离子迅速扩散至血液和细胞外液,但无法直接穿越细胞膜进入细胞内部。这导致细胞外液浓度高于细胞内液,形成渗透压差,水分从细胞内向细胞外渗透,细胞因此脱水。位于第三脑室附近的渗透压感受器检测到这一变化,触发渴觉,驱使人主动寻水。
低血容量性渴觉则由血容量下降触发。因出血、腹泻或大量出汗而失去大量体液时,体液渗透压不一定改变,但循环血量减少,心脏向头部泵血的能力下降,营养物质运输受阻。此时,肾脏释放肾素,经一系列酶反应生成血管紧张素二型,收缩血管以维持血压,并与静脉血压感受器协同,触发对含盐液体的渴望。这种渴觉的本质是机体既需要水分,也需要补充流失的电解质,单纯饮用大量淡水反而会进一步稀释体液。
大脑如何感知水分状态
大脑通过第三脑室周围的特殊区域来监测血液中的渗透压和盐分含量。这些区域的血脑屏障相对薄弱,使得血液中的化学物质能够较为直接地影响此处的神经元。其中,血管器官和穹窿下器官是检测渗透压的关键结构,它们将信号传至下丘脑,既影响加压素的分泌速率,也调控饮水行为。
一个有趣的细节是,渴觉触发后,身体并不会等到吸收的水分真正进入大脑才停止饮水。水分从口腔到被血液吸收大约需要15分钟,如果一直等到渗透压正常化才停止,早就喝多了。身体通过监测吞咽次数和胃部扩张程度来估算已摄入的水量,在水分真正被吸收之前就发出“够了”的信号,这是一种预期性控制机制。
钠特异性饥饿
当身体因出血或大量出汗而丢失体液时,需要补充的不仅是水,还有盐。此时,动物对含盐液体的偏好会自动增强,这种现象被称为钠特异性饥饿。它不需要经过学习,是一种由身体状态直接驱动的本能偏好。
这一机制的生理基础在于肾上腺分泌的醛固酮。当血钠水平下降时,醛固酮分泌增加,促使肾脏、唾液腺和汗腺保留盐分。醛固酮和血管紧张素二型还会改变舌头上味觉感受器以及脑干味觉回路的敏感性,使咸味的感知更为强烈,进而推动个体主动补充钠盐。
月经期间的女性,以及在炎热天气中大量出汗的人,常常会发现咸味食物格外诱人,这并非偶然,而是体内低血容量状态正在通过改变味觉偏好来驱动补盐行为。钠特异性饥饿是少数几种不需要通过经验学习便能自动产生的特异性食欲之一,这与对其他维生素、矿物质的渴求形成鲜明对比——后者通常需要反复的试错学习才能建立。
饥饿与能量调节
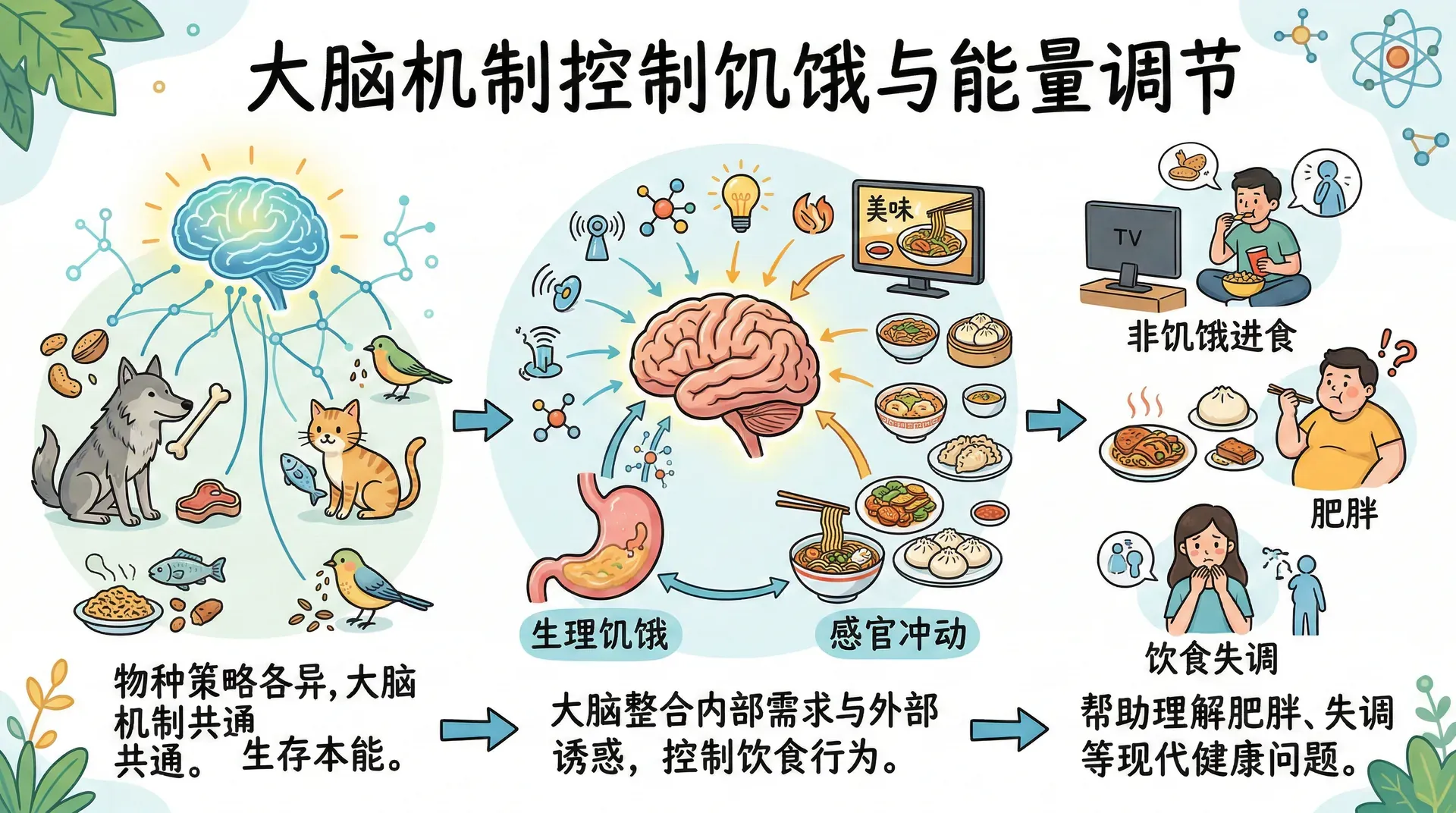
进食是动物最基本的生存行为之一。不同物种因生态位和生理特点的差异,形成了截然不同的进食策略,而这些策略背后的大脑机制,与人类的饮食行为有着深刻的共通之处。理解饥饿的产生与调节,有助于解释为什么人们有时会在不饿的情况下进食,也有助于理解肥胖、饮食失调等现代健康问题的根源。
不同物种的进食策略
蛇和鳄鱼可以一次大量进食,然后数月不再进食。这种策略在变温动物中行得通,因为它们不需要消耗大量能量维持体温,新陈代谢可以长期保持在极低水平。熊则采取相反的策略,在水果和坚果集中成熟的短暂季节里拼命进食,积累脂肪以度过漫长冬季,“最胖者生存”是对这一策略的生动概括。
在中国东北的严冬,麻雀和山雀面临的挑战更为极端。它们体型极小,表面积与体积比很高,散热速度惊人,夜间必须持续颤抖才能防止体温降至致命水平。为此,这些小鸟每天进食到体重增加约10%,再在夜间通过颤抖将这些能量全部消耗。换算到人身上,相当于一个50公斤的人每天白天增重5公斤,夜间再通过颤抖将这些重量消耗殆尽,其代谢强度令人叹为观止。
消化系统的工作流程
消化系统的核心任务是将食物分解为细胞可以直接利用的小分子。这一过程从口腔开始,唾液中的淀粉酶负责分解碳水化合物。食物经食道进入胃部,与盐酸和蛋白酶混合,进行初步消化。胃将食物暂时储存,再通过幽门括约肌的定量开放,将食糜分批送入小肠。
小肠是消化吸收的主要场所,肠壁细胞分泌的酶协同胰腺和胆汁,分解蛋白质、脂肪和碳水化合物,产生的小分子经肠壁吸收进入血液,随后被输送至全身细胞使用或储存。大肠主要负责吸收水分和电解质,并将剩余废物润滑成型,最终排出体外。
食物选择与大脑的关系
食物成分会影响大脑的化学状态,进而对行为产生微妙的影响。一个典型的案例与色氨酸有关。色氨酸是合成褪黑激素的前体物质,而褪黑激素能诱导困倦和睡眠。色氨酸进入大脑需要借助一种载体蛋白,但这种载体同样被苯丙氨酸等其他大型氨基酸竞争使用。
当摄入高碳水化合物的食物时,胰岛素分泌增加,胰岛素会将苯丙氨酸等氨基酸转入肌肉储存,降低它们在血液中的浓度,从而减少了与色氨酸的竞争,使色氨酸更顺利地进入大脑,催生困倦感。这也解释了为什么丰盛的宴席之后人们容易犯困——那种困倦主要来自席间的米饭、馒头和甜点,而非蛋白质食物本身。
民间常有“吃糖让孩子变多动”的说法,但经过严格控制的双盲研究始终无法证实这一点。这类研究让孩子在不同日期分别食用含糖和不含糖的零食,孩子、家长和教师都不知道当天吃的是哪种,结果显示糖对儿童的活动水平、游戏行为或学业表现均无显著影响。
饥饿的短期信号
进食的开始与结束受到多套短期信号的精密调控。口腔的感受是其中不可忽视的一环。人不仅因为营养需求而进食,口腔的咀嚼和味觉体验本身就是强烈的正向刺激。当营养液通过静脉直接注入绕过口腔时,人虽然能维持正常体重,却会对进食的感官体验产生强烈渴望;反之,让动物品尝食物但阻止其进入消化系统,动物会几乎不间断地进食而永远无法满足。这说明口腔感受和消化系统的信号共同构成了饱足感的基础,缺少任何一方都无法产生真正的满足感。
胃扩张是终止一餐的主要信号。胃壁感受器通过迷走神经向大脑传递扩张信息,当胃部充盈到一定程度,饱足感便随之产生。十二指肠在这一过程中也发挥着重要作用:食物进入十二指肠后,肠壁释放胆囊收缩素,一方面收紧胃与十二指肠之间的括约肌,使胃保持充盈状态,另一方面通过迷走神经向下丘脑传递饱足信号,提前终止进食。
血糖、胰岛素与瘦素的长期调节
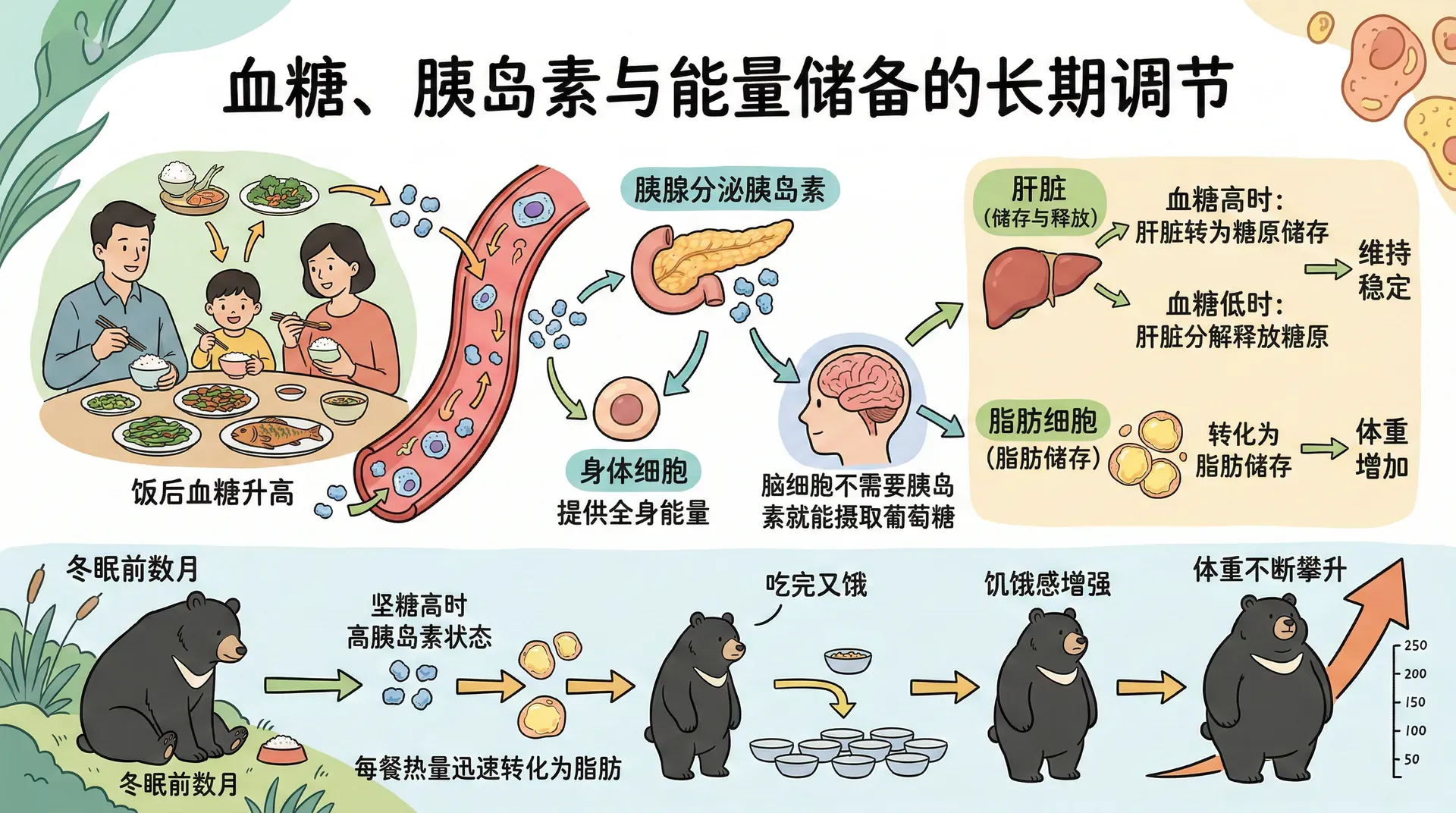
大部分消化后的食物以葡萄糖形式进入血液。葡萄糖是全身细胞的能量来源,也几乎是大脑唯一可以直接使用的燃料。血糖水平升高时,肝脏将多余的葡萄糖转化为糖原储存,脂肪细胞则将更多葡萄糖转化为脂肪;血糖下降时,肝脏再将糖原分解为葡萄糖释放入血,维持血糖相对稳定。
胰岛素是这套系统的关键调节因子。饭后血糖升高时,胰腺分泌胰岛素,帮助葡萄糖进入各类细胞(脑细胞是例外,它不需要胰岛素就能摄取葡萄糖)。若胰岛素分泌持续过高,血糖会被快速转入细胞和脂肪储存,血糖反而下降,饥饿感随之增强。准备冬眠的动物正是利用这一机制,在冬眠前的数月内维持持续高胰岛素状态,每餐摄入的热量迅速转化为脂肪,吃完又饿,体重不断攀升。
若胰岛素长期不足,如一型糖尿病患者,血糖水平可能达到正常值的三倍以上,但由于葡萄糖无法进入细胞,细胞实际上处于“饥饿”状态。患者食欲旺盛却持续消瘦,多余的葡萄糖最终通过尿液大量排出,这也是糖尿病早期诊断指标之一。
短期的进食调节虽然精密,但难以做到长期精确。如果每天的摄入量略多或略少于消耗,误差会日积月累,最终体重大幅偏离正常水平。瘦素是身体用于长期校准的激素。脂肪细胞储存越多,释放的瘦素越多;储存减少,瘦素水平下降。下丘脑感知到高瘦素水平时,饥饿感降低、活动量增加;瘦素水平低时,则反向调节,推动机体多吃少动、积累能量。
在青春期启动的问题上,瘦素也扮演着重要角色。脂肪储备达到一定水平,瘦素信号足够强时,青春期才会启动。若体脂过低,瘦素信号不足,青春期延迟。这一机制的生物学逻辑是:只有当身体储备充足,才具备支撑生殖和哺育后代的能量基础。体形偏瘦的人普遍比同龄人进入青春期晚,这一现象与瘦素机制高度吻合。
几乎所有超重者的血液中都含有大量瘦素,问题不在于瘦素缺乏,而在于大脑对瘦素的敏感性下降,即瘦素抵抗。这与胰岛素抵抗的逻辑相似,长期处于高水平激素环境中,受体的响应能力逐渐钝化。
下丘脑的饥饿控制网络
大脑通过整合来自全身的多种信号来决定何时进食、吃多少。饥饿感不仅取决于胃肠状态和血糖水平,还受到体温、健康状况以及视觉、社交等非生理因素的影响。看到摆盘精致的食物会刺激食欲,和家人朋友共桌而食往往吃得更多,这些都是大脑对环境信息的整合反应。
控制饥饿的核心脑区是下丘脑的弓状核,其中存在两类功能相反的神经元:一类对饥饿信号敏感,另一类对饱足信号敏感。
饥饿敏感神经元接收来自味觉通路的输入,也接收胃饥饿素的刺激。胃在空腹状态下分泌胃饥饿素,该激素传至下丘脑后,既诱发胃收缩,也强化学习与觅食动机。饱足敏感神经元则受胆囊收缩素、血糖、胰岛素和瘦素等多种信号的驱动,在进食后逐步积累足够的抑制信号,最终终止进食行为。
弓状核的输出主要流向室旁核,后者抑制下丘脑外侧区的进食促进作用。下丘脑外侧区一旦被激活,会通过向脑干、皮质和脊髓的多条通路,全面促进食物摄取行为;若该区域受损,动物会拒绝进食,可能饿死。相反,下丘脑腹内侧核的输出抑制进食,该区域受损则会导致持续过量进食和体重迅速增加。
肥胖、基因与现代环境
肥胖是当代中国面临的重要公共卫生问题之一。近40年间,中国成人肥胖率持续攀升,与经济发展带来的饮食结构改变和体力活动减少密切相关。
体重受到基因的显著影响。一项针对540名收养儿童的长期追踪研究发现,这些孩子的体重与其生物学亲属的相关性,远高于与养父母的相关性,说明遗传因素在体重调节中占有重要地位。其中,黑皮质素受体基因的突变是较为常见的单基因肥胖原因,携带该突变的人从幼年起就表现出过量进食和快速增重的倾向。
以中国西北部分高原民族为例,他们中许多人天生容易积累脂肪。这一倾向在传统游牧生活方式下具有明显的生存价值——高热量食物只在特定季节集中出现,进化压力使这些群体形成了“有食即储”的代谢模式,以应对漫长冬季和食物匮乏期。然而,当现代高热量食物全年可得时,这种储能倾向反而成了负担。体重问题的根源从来不是单一的基因或单一的环境,而是两者共同作用的结果。
饮食成瘾与暴食症
暴食症是一种在大量进食与严格节食之间循环的饮食障碍,相当比例的患者同时伴有抑郁、焦虑或其他情绪问题。暴食症患者常见胃饥饿素分泌异常升高,但这往往是行为模式的结果,而非原因,经有效干预后多可恢复正常。
暴食行为与药物成瘾有深刻的神经生物学共性。美味食物和成瘾物质激活的是大脑中相同的奖赏回路,主要是伏隔核的多巴胺系统。戒毒者常常以过量进食来填补原本由毒品满足的奖赏需求,饥饿状态也会提高个体对奖赏刺激的敏感性,使成瘾行为更容易建立。
以大鼠研究为例,每日禁食12小时后给予糖浆,持续数周后,大鼠出现了典型的成瘾特征:每日摄入量递增,进食时释放大量多巴胺和内源性阿片类物质,一旦断供则出现摇头、牙关颤抖等戒断反应。这一发现提示,对高糖食物的强迫性摄取,在神经机制层面与物质成瘾具有相当的相似性。
进食调节的大脑网络高度复杂,整合着血糖、胃扩张、十二指肠激素、体脂水平、社会信号等多维度信息。这种复杂性意味着系统在多个节点都可能出现失调,但同时也赋予了整个系统极强的冗余保障能力。绝大多数人能够在如此复杂的调节网络下长期维持相对稳定的体重,这本身就是一件值得关注的事。
稳态调节的整体视角
温度、水分、能量,这三套调节系统表面上各自独立,实际上在神经和激素层面深度交织。下丘脑是贯穿这三套系统的核心枢纽,它持续整合来自体内外的信号,协调颤抖与出汗、渴觉与排尿、饥饿与饱足,在动态变化中维持着身体的内部平衡。
中国古代医学将人体视为一个与外界环境相互应答的整体,主张顺应时令、平衡阴阳,这种朴素的系统观与现代生理学所揭示的稳态调节逻辑有着相通之处。每一次进食、每一次出汗、每一次感染后的发热,都是身体在环境压力下主动维持内部秩序的具体表现。
这些调节系统的另一个共同特点是冗余性。无论是体温调节还是水分调节,身体都同时保有行为机制和生理机制两条通路,每条通路内部又包含多个环节。某一机制失效时,其他机制会迅速介入补偿。正是这种多层次的冗余设计,使生命系统在面对各种干扰时表现出相当的稳健性。
在快节奏的现代生活中,高热量食物唾手可得,久坐少动的生活方式已成常态,人工照明打乱了自然光周期,慢性压力持续拉高皮质醇水平。这些因素都在不同程度上干扰着进化塑造的稳态调节机制,使肥胖、睡眠障碍、代谢综合征等问题日益普遍。了解这些调节机制的工作原理,不仅是生物心理学的学术课题,也是每个人在现代环境中保持健康的实践基础。