细胞培养基础
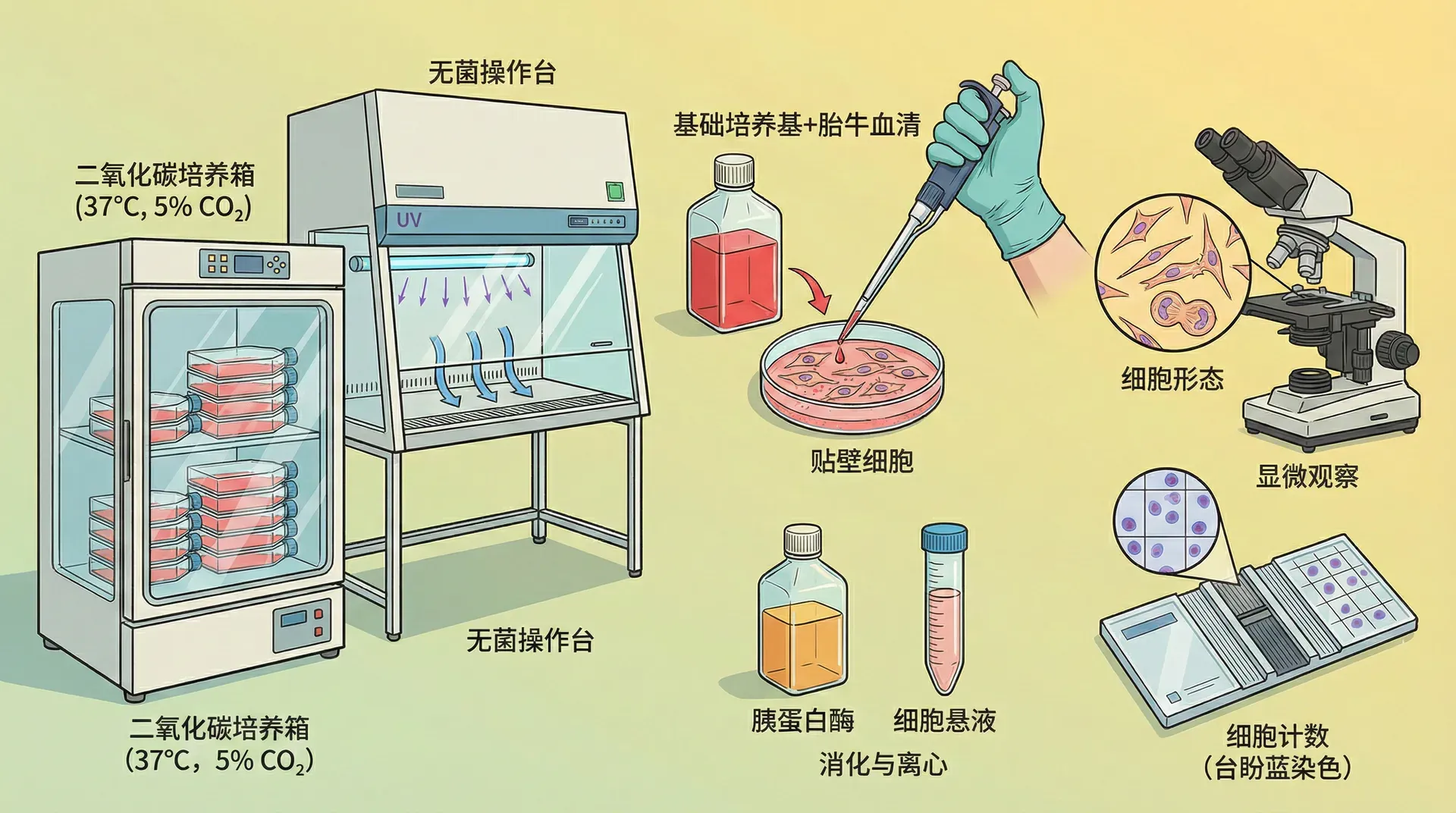
细胞培养技术是现代生物技术研究中不可或缺的一项基本技能,也是开展生命科学各类实验的基础。通过在实验室中对细胞进行体外培养,我们能够模拟生命活动的基本过程,探索细胞的生长、分化、凋亡等机制,从而为药物开发、疾病病理研究、再生医学和组织工程等多个领域搭建坚实的平台。细胞培养不仅仅是让细胞在容器中存活下来,更要保证细胞的状态与体内环境相似,以便获得可靠的实验结果。
为此,掌握细胞培养的基础知识格外重要,这既包括对细胞类型、生长特性、培养条件的深入理解,也离不开严谨的无菌观念和规范的操作流程。每一个细节——从培养用具的消毒、培养基的配置,到细胞的传代和冻存——都直接影响着实验的可靠性与科学性。只有通过系统的学习和反复实践,才能真正掌握细胞培养这项既具挑战性又极具意义的科学技能。
原核细胞与真核细胞的差异
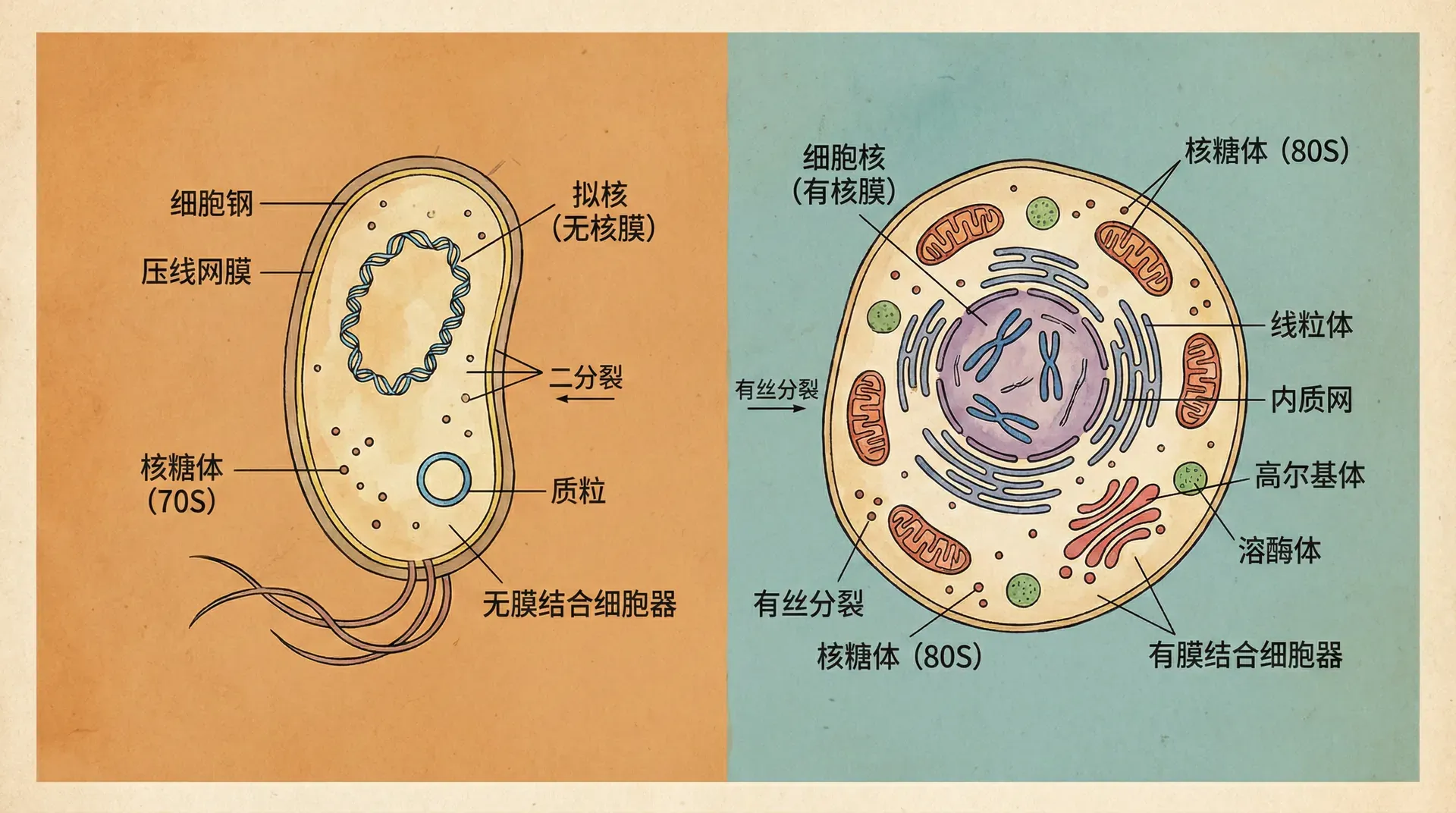
在开始细胞培养之前,我们首先需要认识两类完全不同的细胞类型。生物界的细胞按照细胞核结构的有无,可以分为原核细胞和真核细胞。这种分类不仅仅是形态学上的差异,更反映了生命演化历程中的重大分水岭。
原核细胞是地球上最早出现的生命形式。大肠杆菌、金黄色葡萄球菌等细菌都属于原核生物。这类细胞的遗传物质直接分散在细胞质中,没有被核膜包裹起来,形成一个称为"拟核"的区域。原核细胞的结构相对简单,但这并不意味着它们的生命活动简单。相反,原核细胞以其高效的代谢速率和快速的繁殖能力,在自然界中占据着重要的生态位置。在实验室中,大肠杆菌可以在理想条件下每20分钟分裂一次,这种快速增殖的特性使其成为基因工程的理想宿主。
真核细胞的出现标志着生命复杂性的巨大飞跃。动物、植物、真菌等生物都由真核细胞构成。这类细胞拥有被核膜包裹的细胞核,遗传物质被整齐地组织在染色体上。更重要的是,真核细胞内部划分出多个具有特定功能的细胞器,如同一座城市中的不同功能区域。线粒体负责能量生产,内质网负责蛋白质加工,高尔基体负责物质运输和分泌。这种精细的内部分工使得真核细胞能够完成更加复杂的生命活动。
从上图可以看出,原核细胞与真核细胞在大小上存在显著差异。一个典型的大肠杆菌细胞直径约为2微米,而人的成纤维细胞直径可达20微米,是大肠杆菌的10倍。这种大小差异背后反映的是细胞内部结构复杂性的巨大差距。真核细胞需要更大的空间来容纳各种细胞器和复杂的细胞骨架系统。
两类细胞在培养要求上也截然不同。原核细胞培养相对简单,只需要提供基本的碳源、氮源和必需的无机盐,在37℃恒温培养箱中震荡培养即可。而真核细胞的培养则复杂得多,它们对培养环境有着苛刻的要求。温度需要精确控制在37℃,二氧化碳浓度需要维持在5%以保持培养基的pH值稳定,培养基中还需要添加多种生长因子、维生素和血清成分。更重要的是,大多数动物细胞需要贴壁生长,这意味着培养皿表面的材质和处理方式都会影响细胞的生长状态。
在实验室中选择培养原核细胞还是真核细胞,需要根据研究目的来决定。如果研究重点是基因表达或蛋白质生产,大肠杆菌等原核系统因其快速生长和易于操作而成为首选。但如果研究涉及蛋白质的翻译后修饰、细胞信号转导或药物筛选,则必须使用真核细胞培养系统。
细胞生长的动态过程
细胞培养不仅仅是将细胞投入培养基坐等生长。理解细胞生长的阶段性规律能够帮助我们优化培养条件,选择合适的实验和传代时机。当细胞接种到新鲜培养基后,其数量变化通常会经历四个典型阶段,形成所谓的细胞生长曲线。下面以表格和示意图的方式对四个时期进行整合梳理:
例如,E.coli(二分裂的原核细胞)通常在37°C、营养充足的LB培养基中,从种入到对数期顶峰仅需2-4小时。如果是哺乳动物细胞,则对数生长期可长达数十小时。
此外,细胞繁殖方式影响它们的生长特性。下放对比梳理:
真核细胞的分裂(有丝分裂)过程可细分为四个时期。不同类型细胞的各期耗时可有很大差别。如下表以人成纤维细胞和HeLa细胞为例:
提示: 正常人成纤维细胞完成一次细胞周期约需24小时,肿瘤来源的HeLa细胞仅约18小时。选择实验操作时间时,应参考生长曲线和细胞周期阶段。
细胞培养实验宜在对数生长期收获细胞,此时细胞状态最佳。传代时建议在细胞汇合度80-90%时操作,避免进入稳定期影响活力。
细胞污染的识别与防控
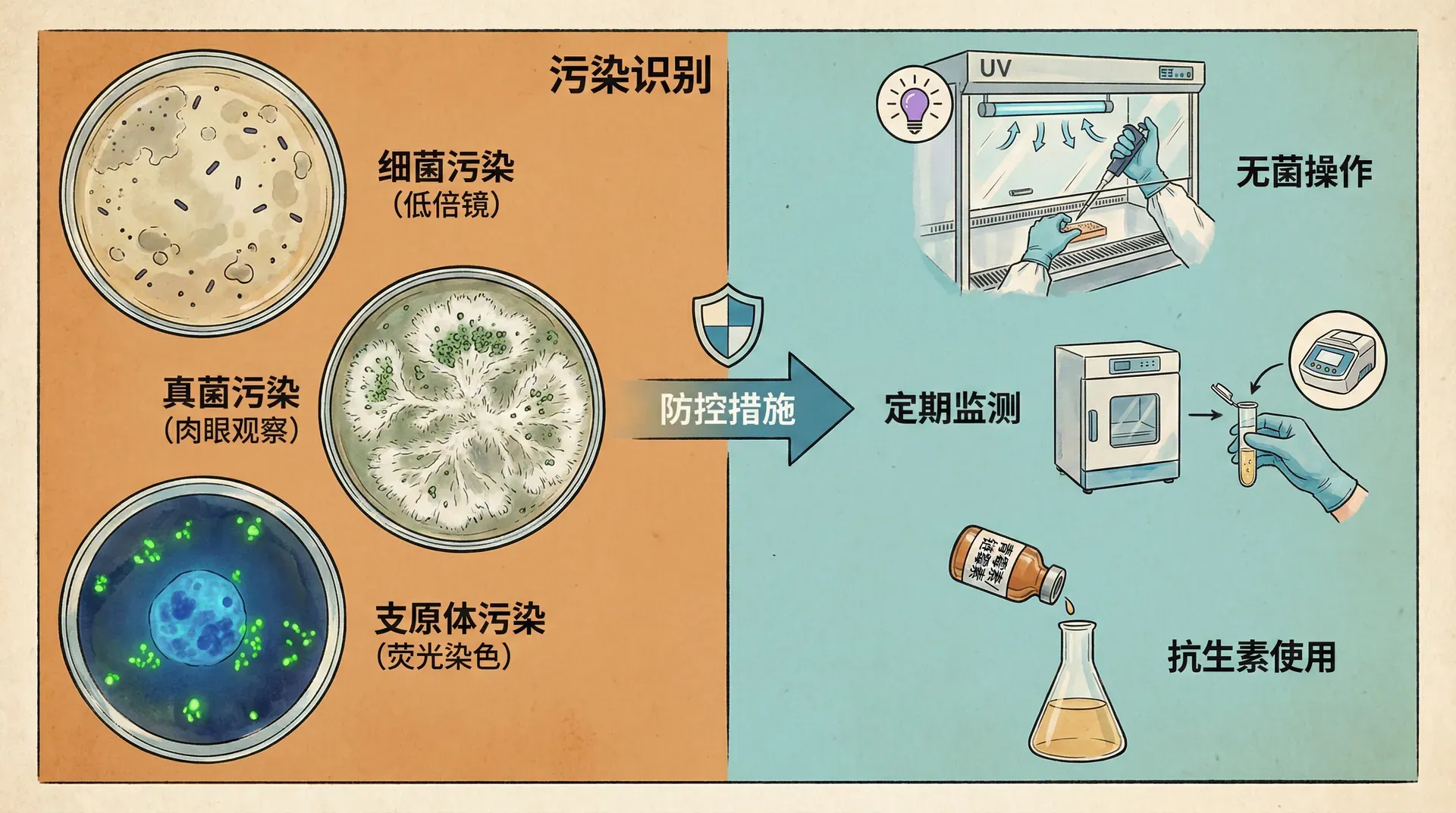
细胞污染是细胞培养中最常见且危害极大的问题,一次污染往往会导致实验全部作废,甚至延误数月的工作。尤其是隐匿型污染,容易使实验者误判结果,危及数据可靠性。因此,建立严格的无菌规范与污染防控体系,是所有细胞培养者的必修课。
常见的细胞污染主要包括细菌、真菌、支原体以及细胞系交叉污染,各自具有不同的特点和典型判别方式。
-
细菌污染
最容易被察觉。细菌大量生长后,培养基短时间内从清澈变得混浊(如牛奶状),并且伴随pH改变和气味异常。显微镜下可见微小、高度活动的颗粒。污染来源可能包括操作者皮肤、呼吸道、器材残留或环境空气。举例:如果实验操作后一天培养基变浑浊,且肉眼能观察到漂浮的颗粒,多为细菌污染。 -
真菌污染
霉菌污染产出肉眼可见的白色、黑色或绿色絮状物,培养基表面往往可见菌丝团。酵母较难辨认,通常表现为轻微浑浊,可在显微镜下看到出芽的圆形细胞。污染多由空气中孢子或培养箱清洁不到位所致。如长时间打开培养皿盖操作,极易诱发真菌污染。 -
支原体污染
支原体污染最为隐蔽。污染时培养基无明显变化,pH值通常不变,细胞生长可仅有轻度下降。支原体可通过0.22微米滤膜,普通消毒措施对其无效,仅借助DNA荧光染色或PCR才能检出。来源常为被污染的血清、细胞系或实验室气溶胶。据统计,高校及医院实验室支原体污染率达15%-35%。
以下总结主要污染类型的特征和检测方法:
例如,曾有实验者因使用未经高温高压灭菌水浴锅,导致所有新接种的培养瓶3天内全部发霉——可见污染源不仅限于空气,设备清洁也极为关键。
交叉污染也是细胞实验中的“隐形杀手”。常见于使用同一生物安全柜操作多种细胞或共用试剂、移液器等。极具竞争力的细胞系(如A549、HeLa)可在多次传代中“侵占”其他细胞,甚至导致整个实验室的细胞系错乱。历史案例显示,早年全球多地实验室的不同癌细胞系因HeLa污染而变成HeLa细胞,造成极大科研资源浪费。
细胞污染预防措施可以用以下要点归纳:
遇到污染后,污染细胞及培养液应密封送高压灭菌,不可直接倒入下水道。污染培养容器单独处理,污染区彻底消毒。尤其是支原体污染,建议直接舍弃整个细胞谱系,避免反复隐性污染。
细胞系的身份认证
随着细胞培养技术广泛应用,细胞系身份混淆已经成为文献和期刊高度关注的问题。错误的细胞系不仅浪费科研经费,更导致结论不可靠甚至被撤稿。数据统计显示,全球约20%-30%的细胞系有标签混乱或交叉污染风险。
常用细胞系鉴定方法对比:
实际操作中,STR分析被国际细胞库、主流SCI期刊广泛认可,也是细胞系新购或关键实验投稿的“金标准”。其流程为:提取细胞基因组DNA → 多重PCR扩增STR位点 → 毛细管电泳分型 → 与参考数据库比对身份。
如上图,STR分析在准确性和灵敏度上远超其他方法,对实验结论可靠性至关重要。形态学观察作为辅助手段快速、经济,但局限明显;核型和同工酶分析仅特定场景适用。
实验室细胞管理小贴士:
- 每个新购或长期传代的细胞系都应STR鉴定并归档
- 培养瓶标签需标注细胞系、日期、操作人和传代数
- 推荐为每株细胞建立“主库”(液氮长期保存)和“工作库”(日常使用),定期回源复苏避免漂移
- 长期传代期间应定期抽样再次鉴定,警惕早期交叉污染
例如,某研究组在论文答辩前夕发现多年培养的“293T细胞”实际STR匹配HeLa系,避免了严重的学术后果。此事件中,如果该组没有进行STR鉴定,或者鉴定结果不准确,都可能导致严重的学术后果。
建议优先从ATCC(美国)、中科院细胞库(中国)、JCRB(日本)等权威细胞库获得细胞,并严格保存随货STR数据,最大程度保障实验的真实性和细胞谱系纯正。
无菌操作的技术

无菌操作是细胞培养成功的基础。实现无菌不仅依赖于设备(如二级生物安全柜的HEPA高效过滤层流系统),更要靠科学规范的操作流程与良好的个人习惯。生物安全柜在保护细胞和操作者安全的同时,其有效运行需要提前预热和紫外消毒(操作时注意关闭紫外灯,避免伤害),并用70%乙醇对操作台和所有入柜物品表面仔细擦拭。
在安全柜内,合理物品布局同样重要:清洁物品与污染源分区,操作区域保持宽敞、气流畅通,所有进入的器材应先消毒。移液和加样等操作要做到动作轻柔、规范,避免手部和吸取端污染,切勿让移液管尖端暴露于空气,所有一次性耗材用后及时丢弃。培养瓶和多孔板开盖应尽量缩短暴露时间,瓶/板盖面朝下避免内表面污染,操作结束后立即盖好。
现代实验室火焰灭菌基本仅用于玻璃器皿,避免用于塑料器材或在生物安全柜内产生明火,以防破坏层流和带来安全隐患。进入细胞操作区前应备齐所有所需物品,减少进出;操作中避免交谈、打喷嚏,头发束好,个人物品不得带入,动作始终平稳避免扬尘和形成气溶胶。
无菌操作的核心在于始终保持“无菌区域”概念:凡无菌物品一旦接触非无菌表面即视为被污染,所有开放状态的培养基或细胞都应尽快操作并及时密封。只有坚持并内化这些原则,才能在日常工作中自然养成安全高效的无菌操作习惯。
总结
细胞培养基础是生物技术研究中的核心技能。我们了解了原核细胞与真核细胞在结构和培养需求上的本质差异,掌握了细胞生长的四个阶段及其特征,认识到细胞污染的危害和防控策略,理解了细胞系鉴定的重要性和方法,并学习了无菌操作的核心技术。
成功的细胞培养不仅依赖于理论知识,更需要在实践中不断磨练操作技能。每一次无菌操作都是对细心和耐心的考验,每一次培养观察都是对细胞生长规律的深入理解。随着经验的积累,你会逐渐建立起对细胞状态的敏锐判断力,能够从细胞的形态、生长速度、培养基的细微变化中察觉潜在的问题。