PCR技术
聚合酶链式反应(PCR, Polymerase Chain Reaction)是20世纪分子生物学领域最具影响力的技术之一。自1983年由美国科学家凯利·穆利斯(Kary Mullis)发明以来,PCR极大推动了生命科学、精准医学以及生物技术产业的发展。
该技术利用耐高温DNA聚合酶通过温度循环对目标DNA进行指数级扩增,只需极微量的初始样本,即可在数小时内获得大量DNA拷贝。因此,PCR很快成为基因检测、临床诊断(如病原体检测、遗传病筛查)、法医鉴定(如亲子和刑事案件DNA比对)、食品安全(如转基因检测、致病菌筛查)等众多领域的标准工具,被誉为“分子复印机”或“DNA扩增器”。
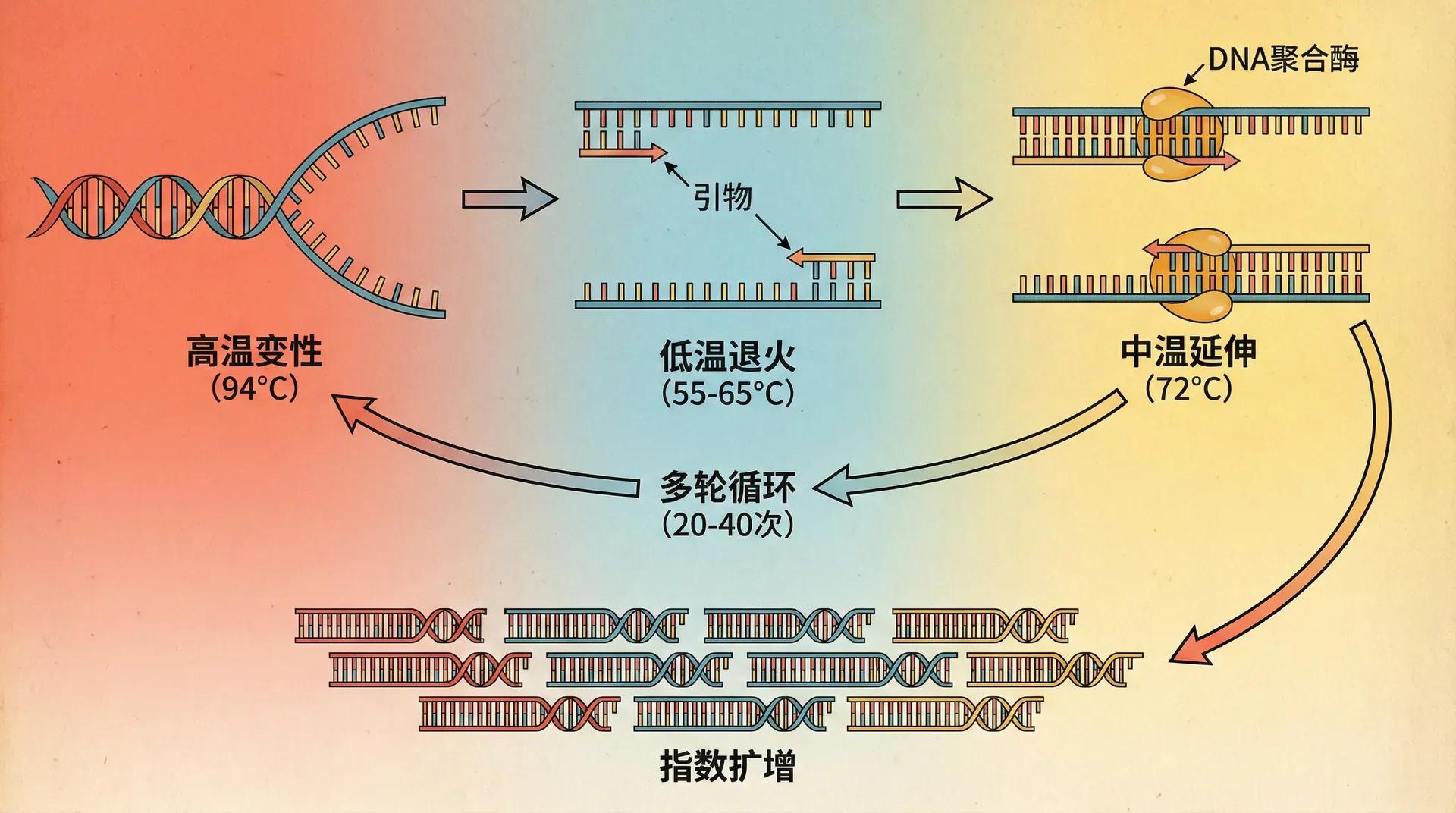
PCR的核心思想是模拟体内DNA复制过程,在体外用酶促反应实现目标片段的高效扩增。其原理是在不同温度下通过三步循环:首先在90-95℃将DNA双链变性为单链;其次在50-65℃使人工合成的引物与目标序列结合;最后在72℃耐热DNA聚合酶沿模板链合成新链。这样循环数十轮,实现指数扩增。
PCR的发明使科学家可以通过极微量线索(如一根毛发或一滴血)获得充足DNA进行分析,这在刑侦物证鉴定中具有重大价值。例如,通过PCR技术,公安部门建立起全国DNA数据库,有效促进了案件侦破和冤假错案的纠正。
一个典型的PCR反应体系包含五大关键组分:模板DNA(目标序列,纳克级)、一对引物(15-30个碱基,精准界定扩增区域)、DNA聚合酶(如Taq酶,耐热且高效催化)、dNTPs(提供合成新链的原料)、缓冲液(维持pH和离子环境)。这些组分的合理配置直接影响扩增的效率与准确性。
PCR反应的三个基本步骤
每个PCR循环包含三个温度阶段,每个阶段都有明确的生化反应发生。在变性阶段,反应温度升高至94-96℃,DNA双螺旋结构中的氢键断裂,两条互补链分离成为单链状态。这个过程通常持续15-30秒,时间过短会导致变性不完全,而时间过长则可能损伤DNA聚合酶的活性。
退火阶段的温度取决于引物的序列组成,一般在50-65℃之间。在这个温度下,引物能够通过碱基互补配对与模板DNA上的目标序列结合。退火温度的选择需要在特异性和效率之间取得平衡:温度过高,引物难以结合,扩增效率降低;温度过低,引物可能与非目标序列结合,产生非特异性扩增产物。
延伸阶段在72℃进行,这是Taq DNA聚合酶活性最佳的温度。聚合酶从引物的3'端开始,沿着模板链逐个添加互补的脱氧核苷酸,合成新的DNA链。延伸速度大约为每分钟1000个碱基对,因此延伸时间需要根据目标片段的长度来设定。
这张图展示了一个完整PCR循环中的温度变化过程。从图中可以看出,温度在三个特定数值之间快速切换,每个温度平台对应一个特定的生化反应。整个循环通常在2-5分钟内完成,这种快速的温度变化需要高精度的热循环仪来实现。
PCR扩增的指数特性
PCR技术最显著的特点是其指数级扩增能力。在理想条件下,每经过一个循环,目标DNA片段的数量就会加倍。如果初始模板有N个拷贝,经过n个循环后,理论上可以得到N×2ⁿ个拷贝。这意味着仅需25-35个循环,就能将单个DNA分子扩增到数百万甚至数十亿个拷贝。
在实验室实际操作中,中国的科研人员经常需要从极微量的样本中提取DNA。例如,在新生儿遗传病筛查项目中,通过采集婴儿足跟的几滴血液,经过DNA提取后可能只能得到几十纳克的DNA。但通过PCR扩增,这些微量的DNA足以进行数十种遗传性疾病的基因检测,包括地中海贫血、苯丙酮尿症等在中国南方和北方地区高发的遗传病。
然而,扩增效率并非始终保持在100%。在反应的初期,由于反应组分充足,扩增效率接近理论值;但随着循环数的增加,dNTPs等反应底物逐渐消耗,扩增产物之间也会发生竞争性重新退火,导致扩增效率下降。最终,反应进入平台期,产物量不再显著增加。
这张图清楚地展示了PCR扩增过程中的三个阶段。蓝色曲线代表理想状态下的指数扩增,而红色曲线则反映了实际扩增情况。在前15-20个循环中,实际扩增接近理论值;之后由于各种限制因素,扩增效率逐渐降低,最终进入平台期。理解这一扩增动力学对于优化PCR条件和准确定量分析至关重要。
实时荧光定量PCR技术
实时荧光定量PCR(Real-time Quantitative PCR,简称qPCR或Real-time PCR)是在传统PCR基础上发展起来的技术,能够在扩增过程中实时监测产物的生成量,从而实现对初始模板量的精确定量。这项技术在2020年初新冠疫情暴发后成为中国乃至全球最广泛使用的病毒检测方法。
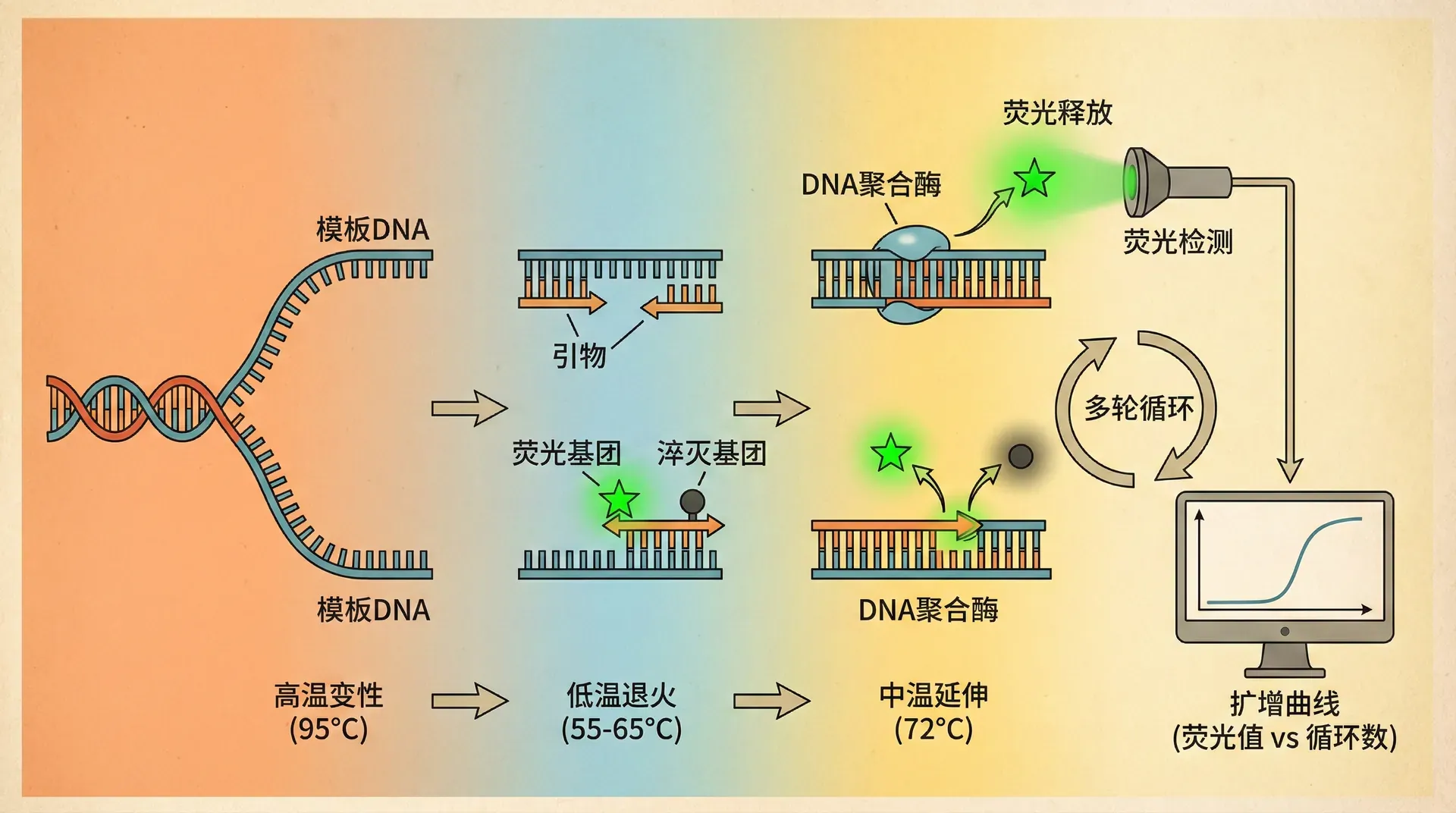
qPCR技术的核心是在反应体系中加入荧光染料或荧光探针。随着PCR扩增的进行,产物量不断增加,荧光信号也相应增强。仪器在每个循环结束时采集荧光信号,绘制出荧光强度随循环数变化的曲线。当荧光信号达到设定的阈值时所对应的循环数称为阈值循环数(Ct值),Ct值与初始模板量呈对数线性关系:初始模板越多,达到阈值所需的循环数越少。
Ct值是qPCR定量分析的关键参数。初始模板量每增加一倍,Ct值理论上减少一个循环。这个关系使得我们可以通过比较不同样本的Ct值来推算它们之间的模板量差异。
在中国的新冠病毒核酸检测实践中,检测试剂盒通常针对病毒基因组的多个保守区域设计引物和探针。当样本中存在病毒核酸时,qPCR反应会产生特异性的扩增曲线,且Ct值通常在20-35之间。医疗机构根据Ct值的大小可以初步判断患者体内的病毒载量:Ct值越小,说明病毒载量越高,传染性可能越强。
qPCR技术使用的荧光检测方法主要分为两类。非特异性染料法采用能够结合双链DNA的荧光染料(如SYBR Green),这种方法成本低廉,但无法区分特异性产物和非特异性扩增或引物二聚体。特异性探针法则使用带有荧光基团的寡核苷酸探针,只有当探针与目标序列结合并被聚合酶的5'外切酶活性降解时才会释放荧光信号,特异性更高但成本也更高。
这张图展示了三个不同初始浓度样本的qPCR扩增曲线。水平虚线代表荧光阈值,曲线与阈值的交点对应各自的Ct值。从图中可以清楚地看到,初始模板浓度最高的红色样本最早达到阈值(Ct=15),而浓度最低的蓝色样本则需要28个循环才能达到阈值。三条曲线的形状相似,但在时间轴上发生了平移,这正是利用Ct值进行定量分析的理论基础。
逆转录PCR(RT-PCR)技术
在分子生物学和医学检测领域,许多研究和临床分析的对象是RNA,例如信使RNA(mRNA)表达谱分析、RNA病毒(如流感病毒、乙肝病毒等)的检测等。然而,RNA分子因化学结构不稳定,极易被环境中的RNA酶降解,因此不能直接作为传统PCR的模板。
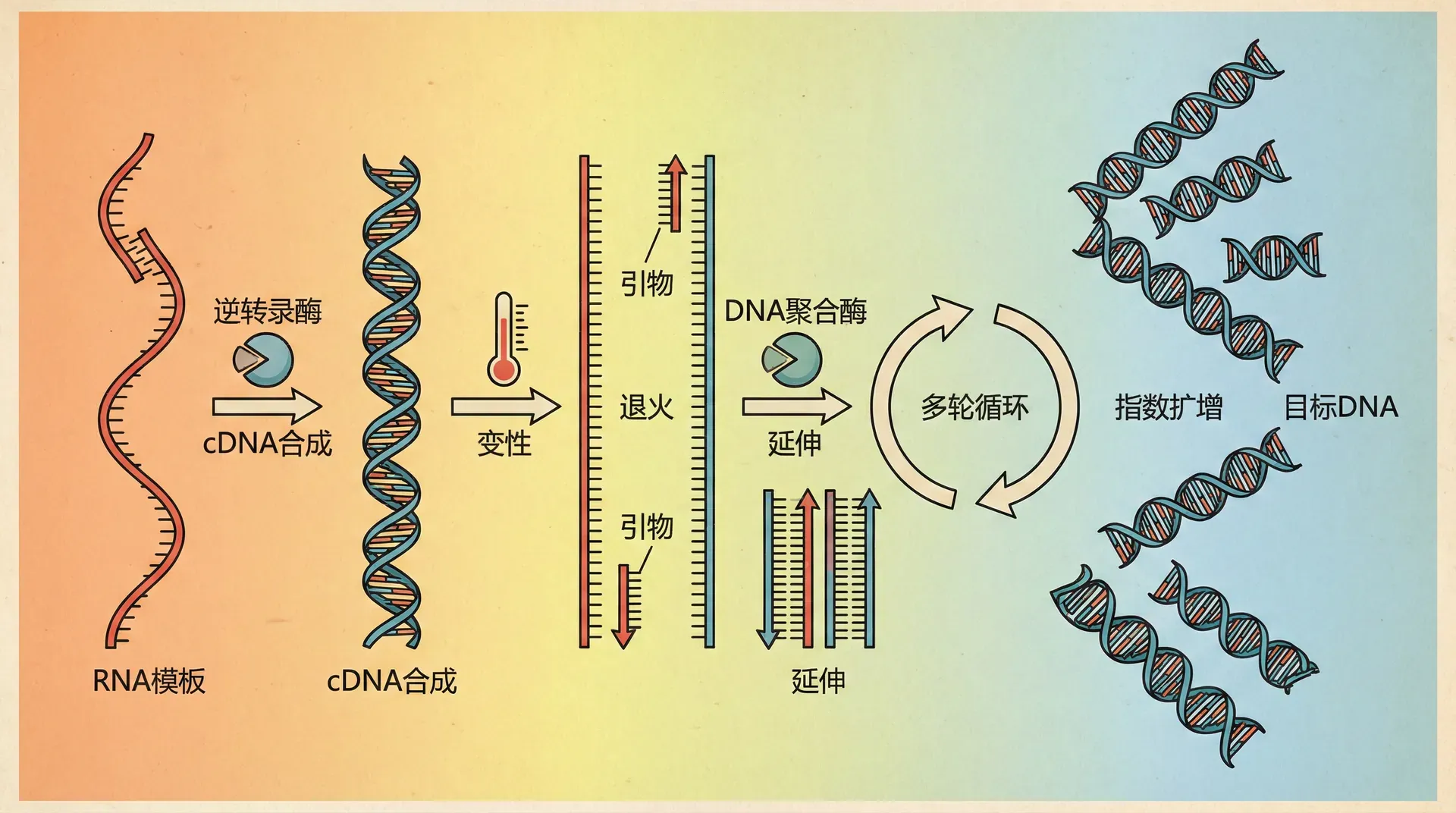
为了解决这一难题,逆转录PCR(Reverse Transcription PCR,简称RT-PCR)技术应运而生。RT-PCR技术首先利用逆转录酶把RNA反转录生成互补DNA(cDNA),然后再以cDNA为模板进行后续的PCR扩增,从而实现对RNA水平的间接检测。
RT-PCR技术极大地拓宽了PCR应用的范围,尤其在基因表达调控研究、肿瘤分子分型、遗传性疾病诊断、以及病毒性疾病的核酸检测中占据核心地位。例如,临床医生能够通过检测患者肿瘤组织中特定基因的mRNA表达量来判断肿瘤的类型及恶性程度,辅助疾病分型和预后。例如在乳腺癌分子分型过程中,需检测雌激素受体(ER)、孕激素受体(PR)、HER2等基因的表达,而这些检测往往采用RT-qPCR(一种定量RT-PCR)完成。
常见逆转录引物类型与应用场景
逆转录反应通常依赖三类引物,选择合适引物类型有助于提升产物的覆盖度和特异性:
例如,假如科学家要检测新冠病毒(SARS-CoV-2)是否存在于患者样本中,会选择针对病毒基因组特定区域(如N基因或ORF1ab)的特异性引物进行RT-PCR。对于全基因表达分析,则多用寡聚(dT)或随机引物以获得更全面的cDNA信息。
新冠病毒核酸检测广泛采用的是RT-qPCR技术。新冠病毒是一种RNA病毒,检测流程为:首先利用逆转录酶将病毒RNA转录为cDNA,随后通过qPCR扩增并实时检测信号。通常采用一步法试剂盒,在同一反应管内连续完成逆转录和扩增,提高操作便捷性并减少样品损失。
RT-PCR实验流程与质量控制要点
RT-PCR对RNA样本的质量要求极高。RNA极易降解,从样本采集、RNA提取、储存到逆转录过程,每一环节都需严格防止RNA酶污染。为降低降解风险,实验人员需佩戴一次性手套、使用无RNA酶耗材,并定期对工作区进行去RNA酶处理。
在基因表达定量分析中,为确保结果准确可靠,常常需要加入内参基因(如β-actin、GAPDH、18S rRNA等)作为标准。这些基因在不同细胞或样本间相对稳定表达,通过内参校正可排除RNA提取量、逆转录效率差异带来的干扰。
RT-PCR/RT-qPCR常见应用举例
主要核酸检测技术对比
通过掌握RT-PCR及相关变体技术,可以精准、高效地实现RNA分子的检测和定量,在现代生物医药和公共卫生领域扮演不可替代的角色。
PCR质量控制与问题排查
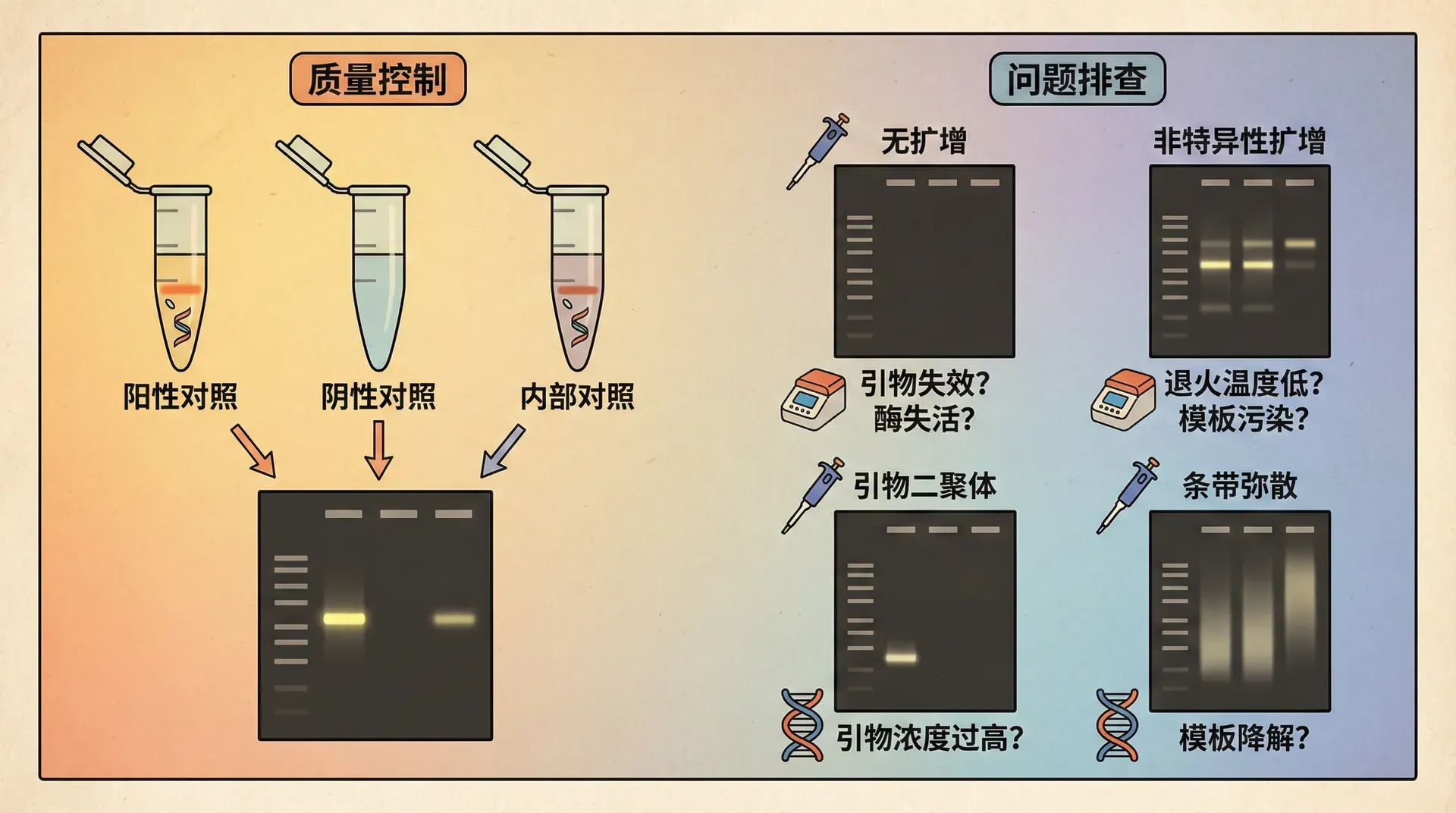
PCR技术原理虽简单,但实际操作中极易受到多种因素的影响,因此建立全流程的质量控制体系至关重要,涵盖样本处理、反应配置、扩增程序和结果分析等环节。首先,防止污染是核心,尤其要避免扩增产物回流引起的假阳性。实验上常通过物理分区、专用耗材与移液器以及单向操作流程等手段,有效降低污染风险。此外,每次实验必须设立阳性、阴性和空白对照,分别用于验证体系有效性、检测污染和监控试剂本身的问题,任一对照异常都意味着数据不可信。
优良的引物设计同样是保障特异性和扩增效率的关键。一般要求长度18-25个碱基、GC含量40-60%,避免二级结构、引物二聚体,3'端不宜富含GC,并建议结合如Primer Premier、Primer-BLAST等软件进行辅助设计。
一旦出现扩增失败、多条带、信号拖尾等问题,应系统分析:无产物多由模板质控、引物设计、退火温度过高或酶失活所致;非特异性扩增则与引物、退火温度、离子浓度及循环数相关。通过优化退火温度、调整引物/镁离子浓度,或采用触降PCR等策略,往往能有效提升扩增质量。
临床PCR检测更需高度重视质量控制,严防假阴性与假阳性:前者可能导致漏诊、延误治疗,后者则带来误判和不必要的医疗决策。因此,操作流程要严格规范,检测人员需经过专业培训和考核。
随着数字PCR、多重PCR、巢式PCR等多种技术变体的兴起,PCR在基因组学、疾病诊断与分型、以及精准医疗如早期筛查、用药指导和疗效监测等领域展现出更广应用前景。系统掌握PCR原理、质量控制与排查要点,既是生命科学专业学生的基础功,更是生物医药行业从业者的核心能力,为科研与临床提供坚实、可靠的技术支撑。