光学测量技术
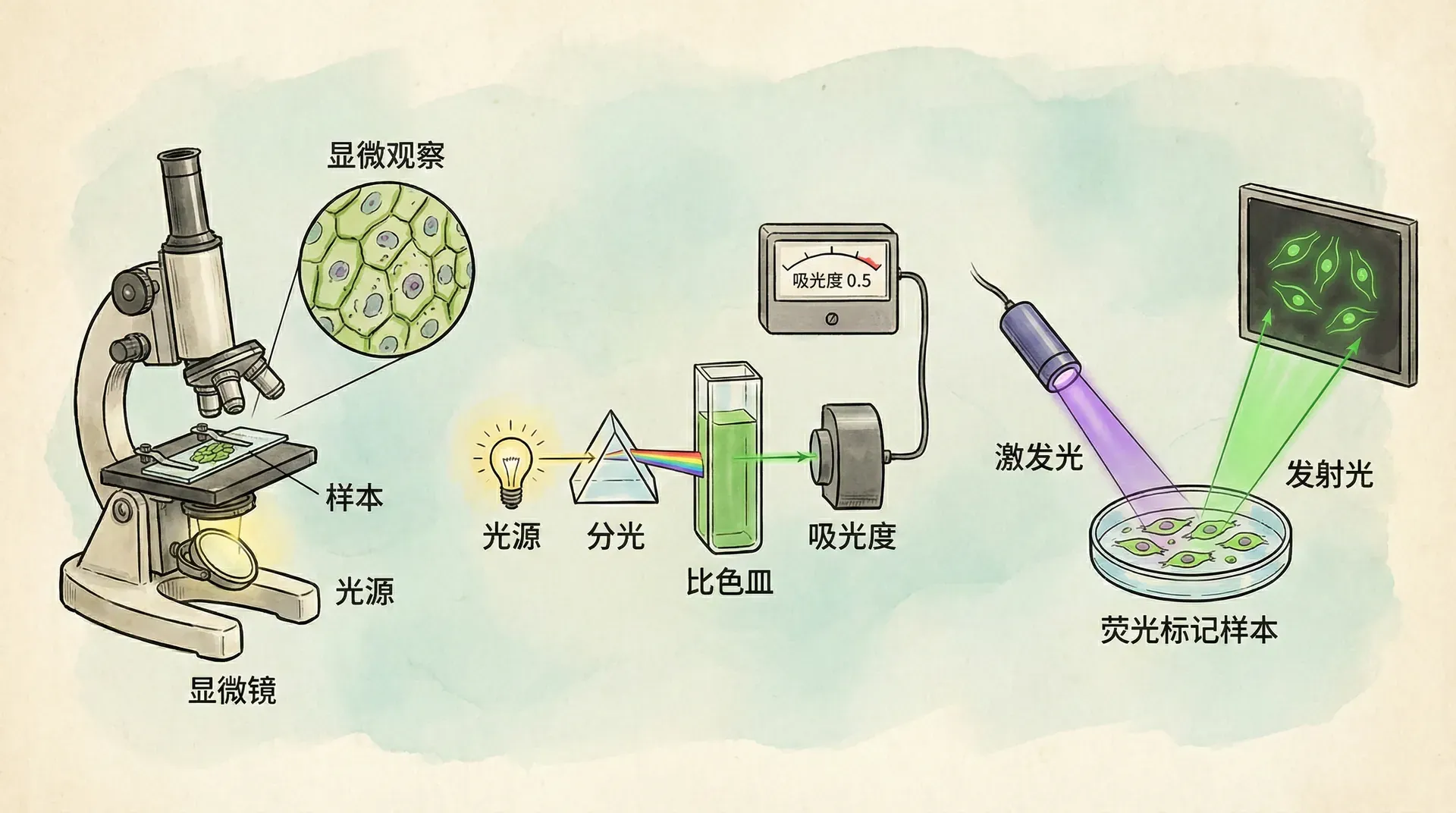
光学测量技术已经成为现代生命科学实验室中的基础工具,无论是在基础研究还是应用开发中都发挥着极其重要的作用。它不仅涉及蛋白质浓度的快速测定,还广泛应用于酶活性分析、DNA/RNA纯度评估以及细胞增殖等多种实验环节。绝大多数生物化学和分子生物学实验的准确性与重现性,都离不开高质量的光学检测。
分光光度计,是实验室中应用最为广泛的光学仪器之一,其依据的是光与物质的吸收、散射等相互作用原理。只有深入掌握光学测量的方法和基础理论,才能确保仪器的正确操作,保障实验数据的可靠解读,更好地探索生物体系的本质规律。
光的基本性质
光是一种电磁波,具有典型的波粒二象性(即既表现为波动又具有粒子特征)。量子力学认为,这种性质是光的本质。但在实验室的日常测量与分析中,我们主要利用和关注光的波动特性——即光作为波传递的规律。掌握这些基本参数,是深入理解光学测量原理、正确使用仪器的第一步。
光的波动特性
在空间中传播的光,其本质是电场和磁场的周期性振荡。这种振荡可用波长()、频率()和能量()三个物理量来共同描述:
- 波长():相邻两个波峰之间的距离,常用纳米(nm)或微米(μm)为单位。在生物和化学分析场景下,紫外-可见区域的波长尤为重要。
- 频率():指单位时间内通过某一点的完整波的数目,单位为赫兹(Hz)。
- 能量():每个光子携带的能量,与频率成正比。
三者之间有以下数学关系式:
其中为光速( m/s)。能量和频率的关系由普朗克公式给出:
其中为普朗克常数()。由此可知,波长越短,频率越高,能量也越大。因此,紫外线的能量通常大于可见光,而红外线能量较低。
下面总结这三者关系:
如果某紫外光波长为 ,则其频率为 ,能量为 。
实际实验中,紫外光(UV)和可见光(Visible) 波段最常用:
- 可见光波长约 ,人眼可见,不同波长对应不同颜色。
- 紫外光约 ,虽人眼不可见,但对生物分子的测量很重要。
光的传播与折射现象
当光从一种介质(如空气)进入另一种介质(如水或玻璃)时,速度会发生改变,此现象称为折射。折射率 定义为光在真空中速度与在介质中速度之比:
例如,水的折射率约为,普通玻璃约为,空气约为。不同介质的折射率不同会导致光线发生弯曲,所以透镜和棱镜能够聚焦和分光。
有趣的物理效应包括色散现象——不同波长的光在同一介质中折射率略有差异,因而白光通过三棱镜后能分为彩虹色,这是分光光度计等仪器实现单色光的重要原理。
介质折射率示例:
折射率不仅影响光速,还会左右光在界面的反射与透射。因此在实验中,光学窗口、比色皿等部件表面必须干净无污染,否则会引入折射率突变,影响信号精确度。
光的强度与衰减机制
光强度是指单位时间穿过单位面积的能量,常用单位为(瓦特每平方米),在光学实验中,也称为辐照度。实验更关注光通过样品前后强度的变化——这些变化主要来自吸收、散射和反射三个过程:
- 吸收:分子吸收光子的能量发生能级跃迁。例如,蛋白质、核酸中特定基团会在特定波长吸收光,这就为生物分析提供了基础。
- 散射:当光遇到悬浮微粒或细胞时,传播方向被改变,导致检测信号削弱或偏移。
- 反射:光遇到介质界面时部分被反射,未能进入样品。
以比色皿测量为例,若比色皿或试管未妥善清洗,其表面上的污染会增加散射和反射,直接影响测定准确性。
某实验小组分别用清洁与未清洁的比色皿测定蛋白吸光度,发现表面有残留液滴或指纹时,检测误差平均增大左右。因此,合适的实验器具选择和标准化清洁流程,是获得可靠数据的前提。
下面列出三种主要光损耗类型及典型影响:
电磁波谱
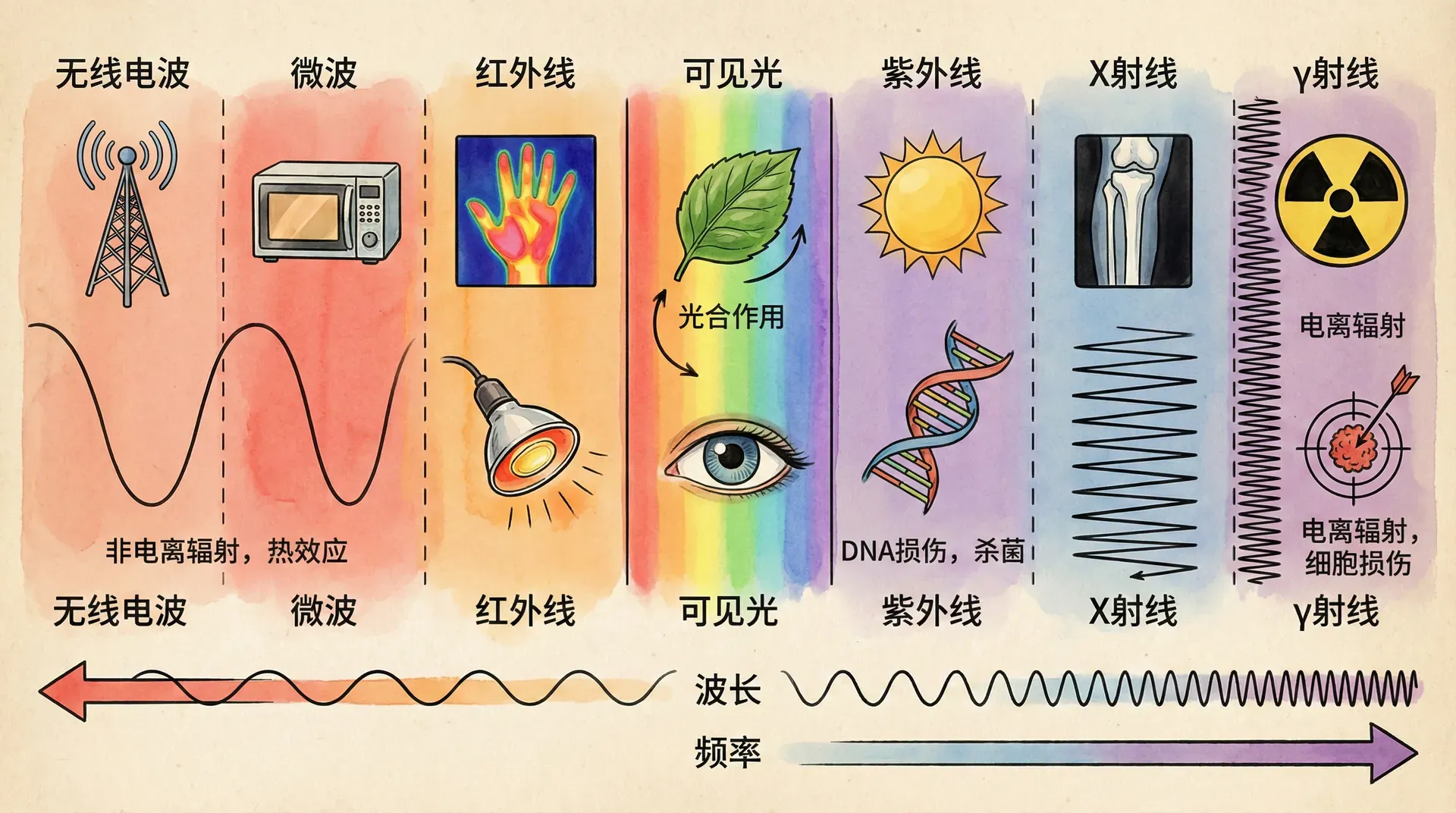
电磁波谱是按照波长或频率排列的所有电磁辐射的集合。从波长极长的无线电波,到波长极短的伽马射线,电磁波谱涵盖了超过20个数量级的范围。在这个庞大的家族中,可见光仅占据极小的一部分,但正是这一部分以及邻近的紫外光和红外光区域,构成了生物技术实验室光学测量的主要工作范围。
电磁波谱的区域划分
整个电磁波谱可以根据波长划分为若干区域,每个区域的电磁波具有不同的性质和应用。无线电波的波长最长,从几毫米到几千米不等,主要用于通信和广播。微波的波长范围为1毫米至1米,除了通信应用外,微波加热也是实验室中常见的技术。红外光的波长范围为780纳米至1毫米,虽然人眼看不见,但可以感受到其热效应。
可见光区域是电磁波谱中人眼能够感知的部分,波长范围为380-780纳米。这个范围的选择并非偶然,而是生物进化的结果。太阳光辐射在可见光波段最为强烈,生物体在长期进化过程中,视觉系统适应了这一波段。紫外光的波长短于可见光,范围为10-400纳米,根据波长又可细分为UVA(320-400nm)、UVB(280-320nm)和UVC(200-280nm)。X射线和伽马射线的波长更短,能量更高,在生物技术中主要用于结构分析和成像技术。
紫外
在生物技术实验室中,紫外-可见光区域(通常简称UV-Vis区域)是应用最广泛的波段。这个区域涵盖了约200-800纳米的波长范围,恰好对应于许多生物分子的电子跃迁能量。蛋白质中的芳香族氨基酸(色氨酸、酪氨酸和苯丙氨酸)在280纳米附近有强吸收,而肽键在远紫外区(190-220nm)有吸收。核酸的碱基在260纳米附近有最大吸收,这使得我们可以方便地通过测量260纳米的吸光度来定量DNA和RNA。
图中显示了DNA在不同波长紫外光下的吸收曲线。可以看到,DNA在260纳米处的吸光度最大(λmax=260nm),这是核酸分子中特有的吸收峰。其余波长下吸光度较低,说明DNA对260纳米附近的紫外光具有特异性强吸收。这一特性被广泛用于DNA和RNA的定量分析,例如通过测量260纳米的吸光度可以计算核酸的浓度。
不同波长的能量差异
电磁波的能量与波长成反比,这意味着波长越短的光子携带的能量越高。这种能量差异决定了不同波段电磁波与物质相互作用的方式。低能量的无线电波和微波主要引起分子的转动,红外光引起分子的振动,而可见光和紫外光的能量足以引起电子跃迁。
在260纳米处,光子的能量约为4.77电子伏特(eV),这个能量刚好可以激发核酸碱基中的π电子。而在280纳米处,能量约为4.43电子伏特,可以激发蛋白质芳香族氨基酸中的电子。这种精确的能量匹配,使得UV-Vis光谱法成为生物分子定量和定性分析的有力工具。
理解光子能量与波长的反比关系,对于选择合适的测量波长至关重要。波长越短的紫外光虽然能量更高,但也更容易对生物样品造成损伤,同时对仪器材料的要求也更严格。
光与物质的相互作用
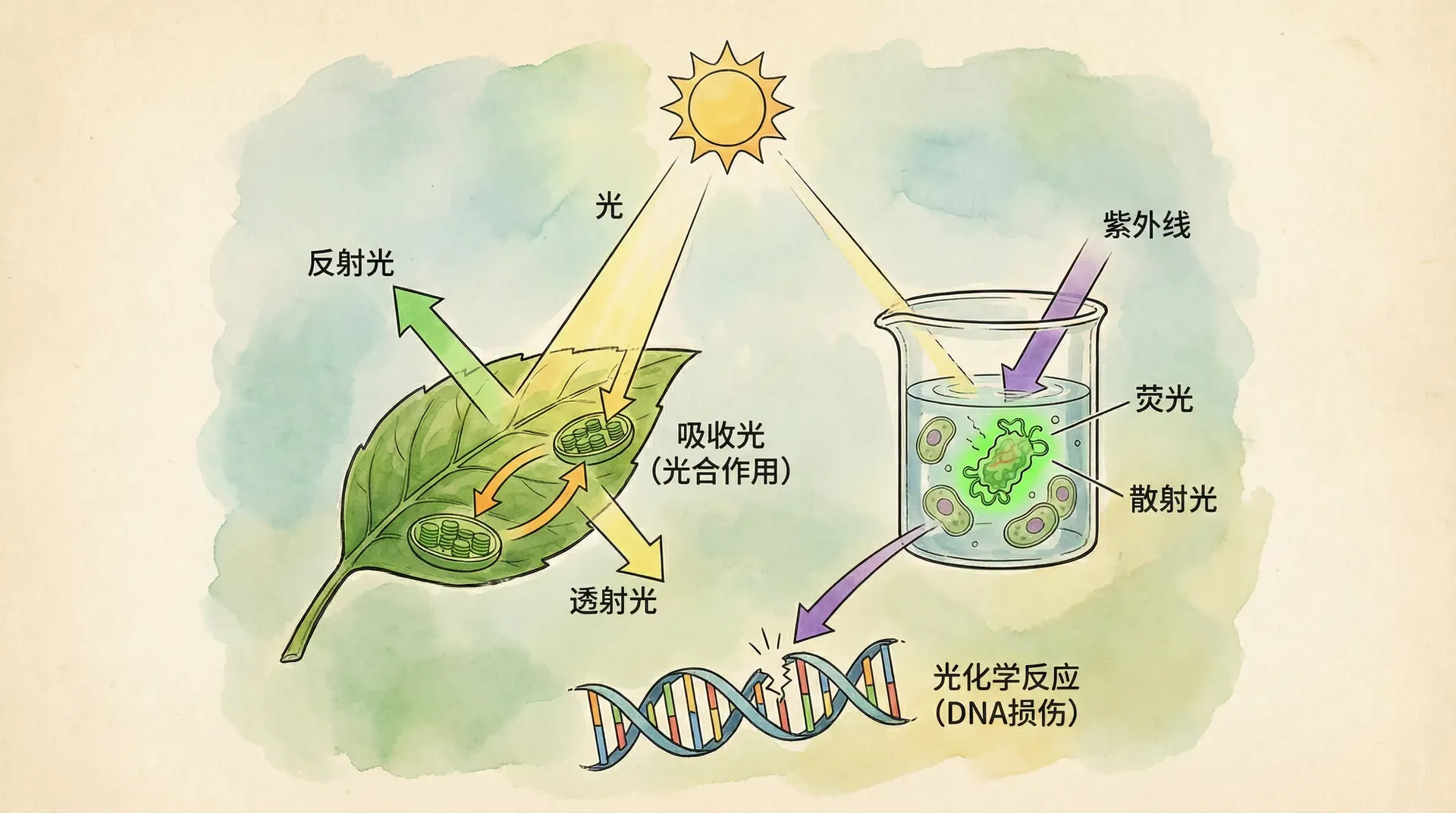
当光穿过物质时,可能会发生多种物理过程,包括吸收、散射、反射和透射。它们共同影响了样品对光的响应,其中心理吸收在分光光度定量分析中最为关键——因为溶液对特定波长光的吸收程度与待测物质的浓度直接相关。
下表总结常见的光-物质相互作用及其意义:
在多数生物化学与分子生物学实验中,我们最关注吸收现象。
光吸收的分子机制
光的吸收本质上是一个量子过程。当入射光子的能量 刚好等于分子两个能级之间的能量差 时,分子可以吸收光子,发生能级跃迁。其关系描述为:
其中 为普朗克常数, 为光的频率, 为光速, 为波长。
有机分子的主要吸收大都源自价电子,特别是 电子(如共轭双键)与 电子(如未成键孤对电子)的跃迁。例如:
- 跃迁:常见于芳香环、共轭双键
- 跃迁:常见于含氧/氮等杂原子的羰基、肽键等
案例一:核酸的吸收
以DNA为例,碱基结构中含有芳香环和共轭双键系统。当波长为260 nm的紫外光照射时,发生 跃迁,表现为强烈吸收峰。这种激发状态极为短暂,分子会通过发射荧光、非辐射弛豫(转化为热)或其他能量释放方式迅速回到基态。
案例二:蛋白质分子吸收
蛋白质的光吸收主要有以下来源:
例如,血红蛋白的“Soret带”在415纳米(nm)波长处具有非常强烈的吸收,这是血红素分子的典型特征吸收峰。Soret带也称为“苏瑞带”或“紫带”,是由于血红素分子中特有的金属-卟啉结构导致的显著可见光吸收,构成了识别与研究血红素家族蛋白的重要光谱依据。
朗伯-比尔定律
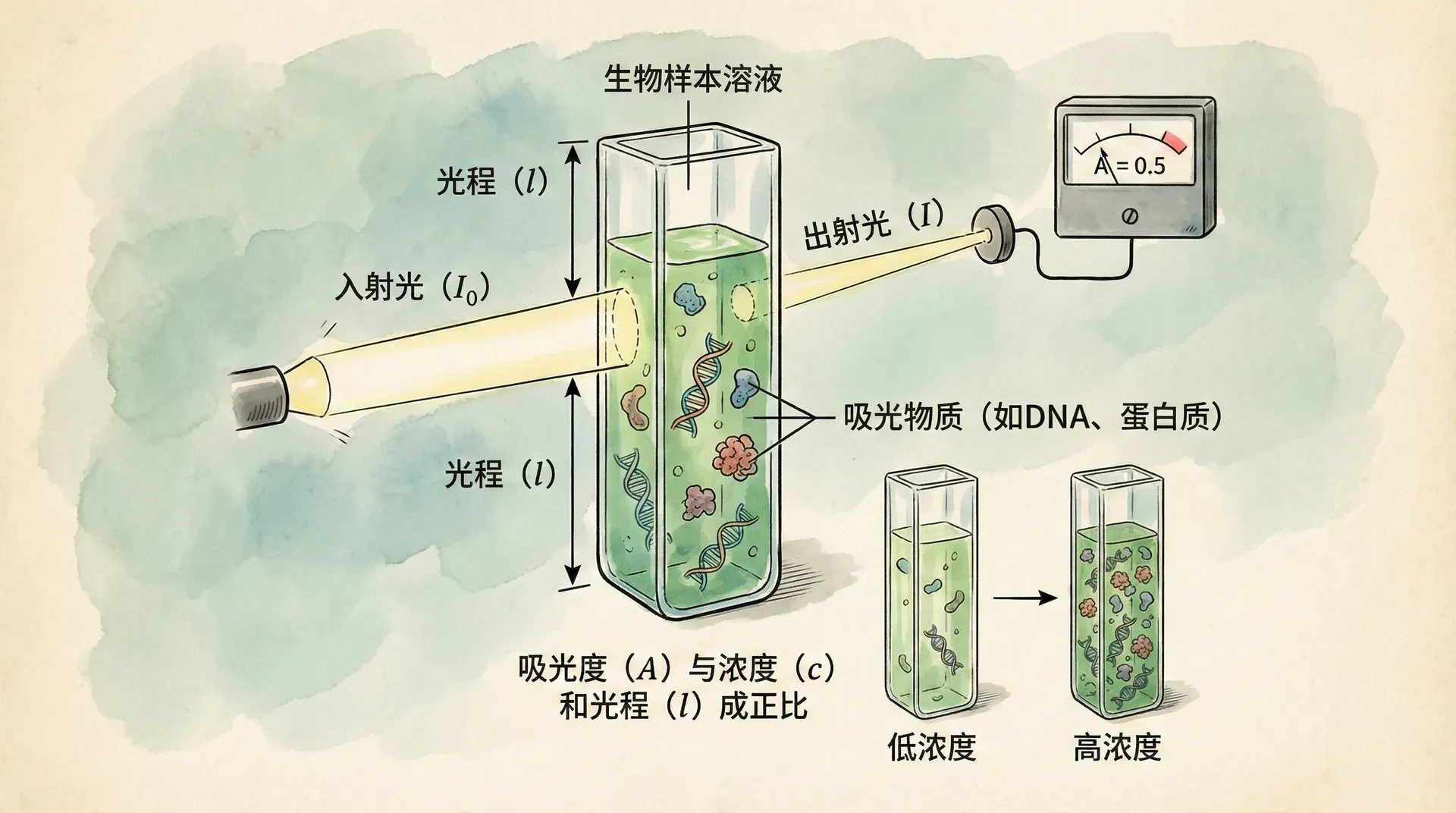
朗伯-比尔定律是分光光度定量分析的理论基础。定律内容表达为:
其中:
- 为吸光度(absorbance),无单位
- 为摩尔吸光系数(L·mol·cm),反映物质在某波长光下的吸收强度
- 为溶液浓度(mol/L)
- 为光程长度(cm)
吸光度 又和入射光强 及透射光强 相关:
摩尔吸光系数具有很强的结构特异性。例如,纯DNA在260 nm的 约为 L·mol·cm(以核苷酸计),这意味着 mol·L、 cm 时,吸光度 。
下表对常见生物分子的摩尔吸光系数做一概览(260 nm处):
朗伯-比尔定律成立条件:
- 光源应为单色光,不同波长差异明显
- 溶液需稀释且均匀,高浓度下分子间效应将使曲线偏离线性
- 光强适当,避免过强光导致光子多重效应
- 溶液应澄清、无散射
一般分析时,吸光度最佳范围为 ,此区间内线性关系最可靠。
例如,某高校实验课对BSA标准蛋白定量,数据显示 mg/mL 范围内吸光度-浓度关系 R² 大于0.999,说明线性极好。若浓度大于2 mg/mL,会产生明显“非线性抬头”,需稀释后再测量,确保定量准确性。
散射和浊度
除了本征吸收以外,散射亦对光通过样品造成影响——尤其是生物样品如细胞悬液、聚集态蛋白、非均一胶体等。当光遇到尺寸与波长相近的颗粒时,就会发生散射,部分光线偏离主传播方向,导致实际到达检测器的透射光减少,从而引起“表观吸光度”升高。
浊度(turbidity)正是基于散射原理,用于反映微粒浓度。例如:
- 微生物培养液通过测量 nm 处的吸光度(通常记为 )来监控细胞生长。
- 实际上, 并非真正意义上的吸收,而主要受散射影响。菌体越多,散射越大, 值越高。
为了获得精确可靠的吸收测量,样品应澄清、无悬浮杂质。散射会导致吸光度高估,使定量失真。可通过离心、过滤去除不溶物,或采用带积分球的分光光度计校正散射影响。
总结
光学测量技术在生物分析、环境监测、医学诊断等诸多领域发挥着重要作用。它能够帮助科研人员检测微量物质,揭示分子水平的结构与变化,是分子生物学和生命科学实验中不可替代的关键工具。
朗伯-比尔定律作为定量测量的基础,建立了吸光度与浓度之间精确的数学联系。实际应用中,了解其适用前提,如样品澄清、单色光源等,有助于获得科学有效的实验数据。同时,分光光度计的各核心部分协同工作,保证了测量的灵敏性、重复性和准确性,因此合理选用和设置仪器参数,对实验成败至关重要。
为了长期获得高质量的数据,应高度重视仪器的性能验证与日常维护。例如,及时更换老化光源、清洁比色皿、校准波长和检查响应线性,都属于规范的操作流程。良好的维护习惯不但能够减少故障发生,也能提升实验效率和数据的可靠性。