生物大分子溶液
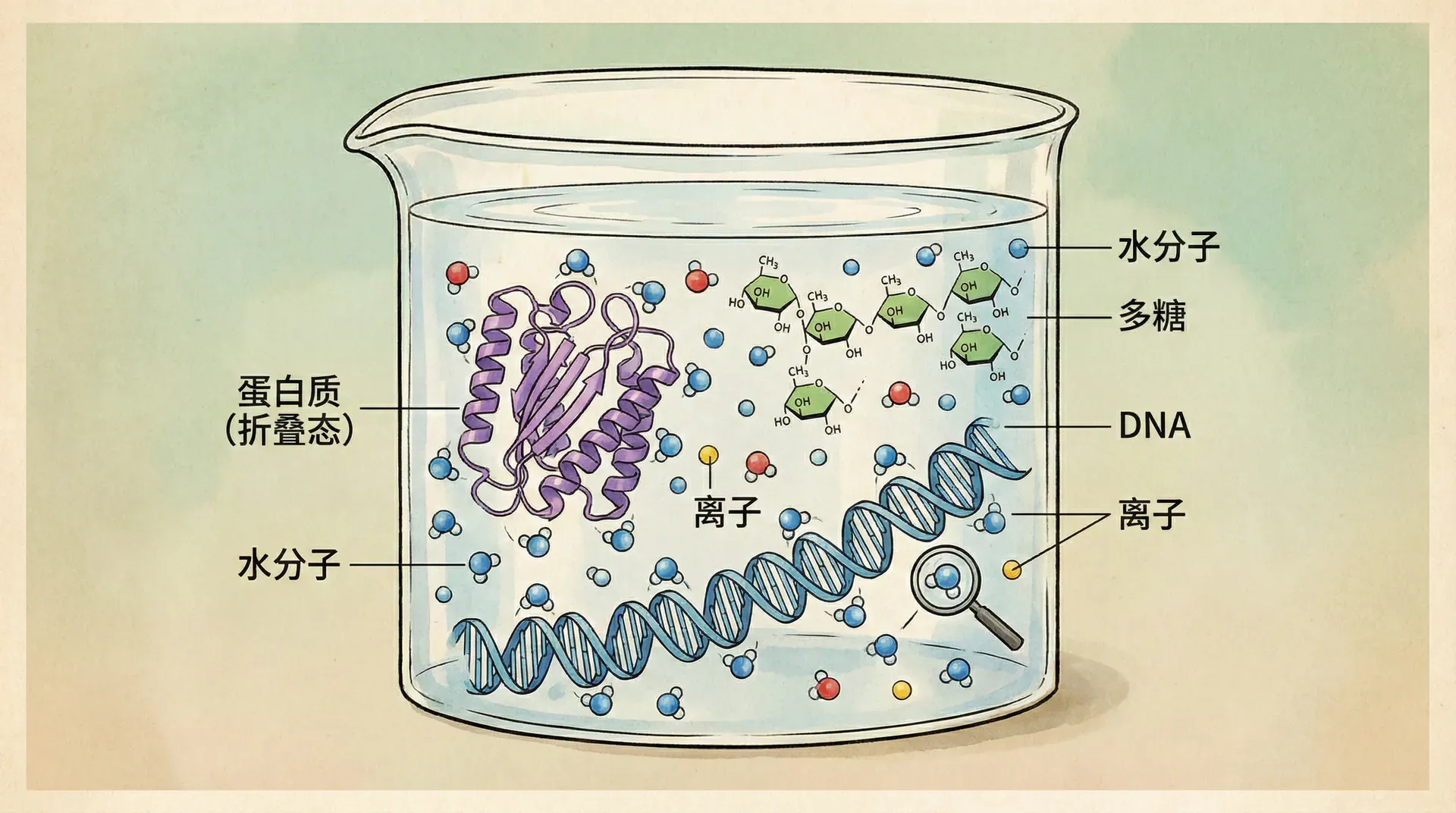
在生物技术实验室中,蛋白质和核酸是两类极为重要的生物大分子。它们不仅构成了细胞的结构和功能基础,也是生命信息传递与生物化学反应的核心执行者。例如,蛋白质以其丰富多样的空间结构,承担着催化、生物信号传递、分子运输、细胞骨架构建以及免疫响应等多种生命功能。核酸则负责遗传信息的存储、复制及表达调控,是生命遗传和进化的根本载体。随着现代分子生物学和生物工程学的快速发展,蛋白质和核酸已经成为医学诊断、药物研发、基因编辑、疫苗制备、疾病机理研究等诸多前沿领域关注的焦点。无论是中国CRISPR基因编辑技术的突破,还是新冠疫苗的mRNA技术应用,都离不开对蛋白质和核酸的深入理解与高质量的实验操作。
因此,理解并掌握如何正确配制、处理和储存这些大分子溶液,对于保证实验数据的准确性、实验结果的可重复性以及下游应用的可靠性具有决定性意义。实际工作中,错误的操作可能导致蛋白质变性、活性丧失,或使核酸发生降解和污染,不仅影响单项实验的结论,还可能直接影响整个科研项目的进程与成败。只有通过科学、规范的实验流程,才能确保蛋白质和核酸在储存和应用过程中的稳定性和活性,为生物医学研究和产业应用奠定扎实基础。
蛋白质的结构与功能
蛋白质是由氨基酸通过肽键连接而成的生物大分子,承担着生命体内几乎所有的功能性工作。从催化生化反应的酶,到构成细胞骨架的结构蛋白,再到调节基因表达的转录因子,蛋白质的功能多样性源于其复杂而精密的结构层次。
蛋白质的结构层次
蛋白质的结构可以分为四个层次,每个层次都对蛋白质的最终功能产生重要影响。一级结构是氨基酸的线性排列顺序,这个序列由基因编码决定。以中国科学家在2003年完成的水稻基因组测序为例,科学家们通过解读基因序列,进而推导出水稻中数万种蛋白质的一级结构,为培育高产优质的水稻品种提供了分子基础。
二级结构是指局部区域的氨基酸链通过氢键形成的规则构象,最常见的是α螺旋和β折叠。这些结构就像建筑中的砖块和钢梁,为蛋白质提供了基本的结构单元。三级结构则是整条多肽链在三维空间中的折叠方式,由多种化学键和相互作用力维持,包括氢键、离子键、疏水作用和二硫键。某些蛋白质还具有四级结构,即多条多肽链组装成的复合体,例如血红蛋白就是由四条多肽链组成的。
蛋白质的功能多样性
蛋白质的功能与其结构密切相关。酶作为生物催化剂,能够将化学反应速率提高数百万倍,这种催化能力来源于其活性位点的精确三维结构。例如,消化道中的胃蛋白酶能在酸性环境下分解食物蛋白,而胰蛋白酶则在小肠的碱性环境中发挥作用。这种环境适应性反映了蛋白质结构对功能的决定作用。
结构蛋白为细胞和组织提供机械支撑。胶原蛋白是人体含量最丰富的蛋白质,占总蛋白质的25%至35%,其三股螺旋结构赋予了皮肤、骨骼和肌腱优异的抗拉伸强度。运输蛋白负责物质的转运,血红蛋白携带氧气从肺部运送到全身组织,而白蛋白则在血液中运输脂肪酸和激素。
蛋白质的功能完全依赖于其正确的三维结构。当蛋白质因高温、极端pH或化学物质而变性时,即使一级结构未改变,其功能也会丧失。这就是为什么在实验室中处理蛋白质溶液时需要格外小心的原因。
蛋白质溶液的组分
配制蛋白质溶液时,需要仔细考虑多种组分,以确保蛋白质维持其天然构象和生物活性。蛋白质溶液的基本组分包括缓冲系统、盐离子、稳定剂和保护剂。
缓冲系统的选择
缓冲液是蛋白质溶液的基础,其主要作用是维持溶液pH的稳定。不同蛋白质对pH的敏感性各不相同,大多数蛋白质在pH 6至8的范围内较为稳定。常用的缓冲系统包括磷酸盐缓冲液(PBS)、Tris缓冲液和HEPES缓冲液。
磷酸盐缓冲液在生理pH范围(pH 7.2至7.4)具有良好的缓冲能力,且对大多数蛋白质无害,因此被广泛应用于蛋白质纯化和储存。以中国疾控中心在疫苗生产中的应用为例,许多疫苗抗原都是在磷酸盐缓冲液中配制和保存的。Tris缓冲液的优点是缓冲范围较宽(pH 7至9),但其缓冲能力受温度影响较大,温度每升高1℃,pH值下降约0.03个单位。
盐离子的作用
盐离子浓度对蛋白质的溶解度和稳定性有显著影响。适当的离子强度可以屏蔽蛋白质表面的电荷,减少分子间的静电排斥或吸引,从而防止聚集。生理盐水含有150 mmol/L的氯化钠,这个浓度接近人体体液的离子强度,适合大多数哺乳动物来源的蛋白质。
低离子强度可能导致某些蛋白质因静电排斥而难以维持正确构象,而过高的离子强度则可能引起“盐析”现象,使蛋白质从溶液中沉淀出来。在实际应用中,通常将氯化钠浓度控制在50至200 mmol/L之间。二价阳离子如镁离子和钙离子对某些酶的活性至关重要,例如DNA聚合酶需要镁离子作为辅助因子才能发挥催化功能。
蛋白质稳定剂
为了防止蛋白质在储存和使用过程中失活,常需要添加各种稳定剂。甘油是最常用的蛋白质保护剂之一,通常以10%至50%的浓度添加。甘油能够降低水的化学活性,减缓蛋白质的水解和氧化,同时在冷冻时作为抗冻剂,防止冰晶形成对蛋白质结构的破坏。
牛血清白蛋白(BSA)常被添加到稀蛋白质溶液中,浓度通常为0.1%至1%。BSA起到“载体蛋白”的作用,可以防止目标蛋白因浓度过低而吸附到容器壁上造成损失。在中国的生物制药企业中,生产单克隆抗体时通常会在配方中加入少量人血清白蛋白,以提高抗体的稳定性和货架期。
二硫苏糖醇(DTT)或β-巯基乙醇等还原剂用于保护蛋白质中的半胱氨酸残基不被氧化。蛋白酶抑制剂则是防止蛋白质被降解的关键添加物,特别是在从细胞或组织中提取蛋白质时,必须加入蛋白酶抑制剂混合物来阻止内源性蛋白酶的活性。
上图展示了蛋白质在4℃条件下储存时活性随时间的变化。可以看到,添加甘油等保护剂后,蛋白质的活性保持率显著提高,储存30天后仍能保持近80%的活性,而未添加保护剂的蛋白质活性下降到45%。
蛋白质的储存与处理
蛋白质的稳定性及活性高度依赖于合理的储存和处理方式。由于蛋白质是高度敏感的生物大分子,很容易受到温度、pH、机械应激和化学添加剂的影响而变性或降解。了解不同影响因素的作用机制,有助于在实验和实际应用中更好地保护蛋白质。
温度控制策略
温度管理是蛋白质储存与处理中的核心。不同蛋白质、不同应用场景对温度要求有所区别。以下汇总了常见蛋白储存温度及注意事项:
实践中,短期储存推荐在4°C;长期储存则宜选用-20°C或-80°C。冷冻过程尤其需要避免多次冻融,因为冰晶反复形成、溶解会对蛋白质造成不可逆结构损伤。通常的做法是预先将蛋白溶液分装成小份,按需解冻。
冷冻蛋白质溶液时,推荐采用快速冷冻方法,例如将样品管瞬时投入液氮或干冰-乙醇浴,使溶液几秒内彻底降温结冰。这一方法有助于生成小冰晶,最大程度地减小对蛋白构象的损伤。
常见冷冻保护剂比较
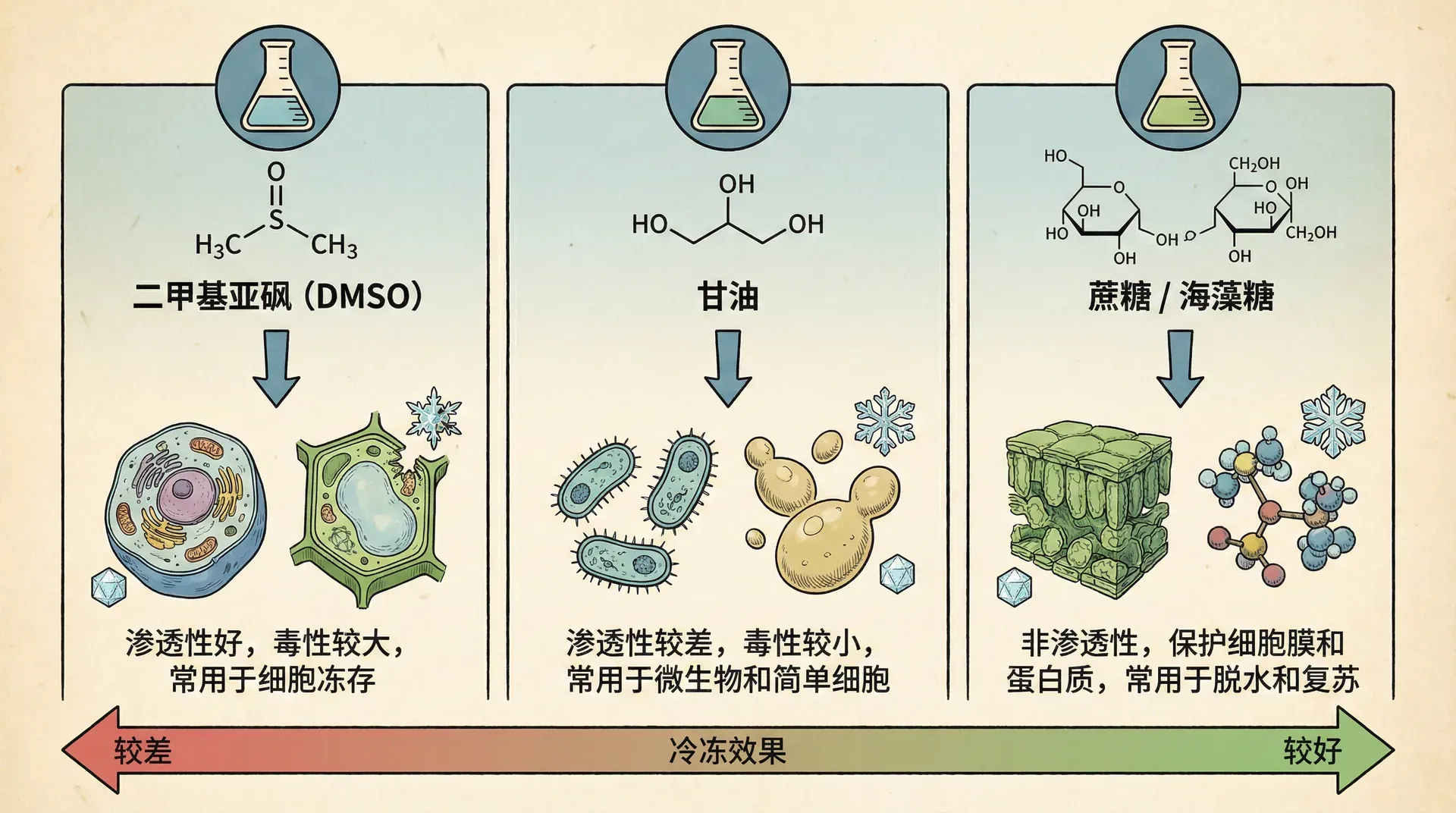
冷冻保护剂的科学选用大大提升蛋白质冷冻保存的成活率。常用冷冻保护剂如下表所示:
例如,海藻糖(Trehalose)在极端环境下的生物保护应用尤为引人注目。中国多家生物技术企业已在冻干疫苗及重组蛋白制备中加入海藻糖,以保证蛋白的长期结构完整性。而甘油因具备良好的通用性,是实验室常用的基本冷冻保护剂。
机械应力的避免
蛋白质不仅对温度敏感,对机械应力同样易受损伤。剧烈的振荡、强烈涡旋和泡沫形成都会导致蛋白的变性、聚集。科学合理的操作可显著减少机械损伤带来的活性损失。
蛋白溶液处理的常见方法:
实验室操作细节注意:
- 混合溶液时采用上下翻转或慢速旋转,避免用力摇晃。
- 吸取/排放溶液时控制速度,防止起泡及飞溅。
- 离心操作需选用合理g值和时间,过度离心易致蛋白聚集沉淀。
上图数据表明,蛋白活性与操作温和程度密切相关。实验显示,经过剧烈机械扰动或多次冻融后,仅有极少部分蛋白能够维持原有活性。例如常用的GFP蛋白,如果反复冻融5次后,活性几乎消失。
核酸的结构与功能
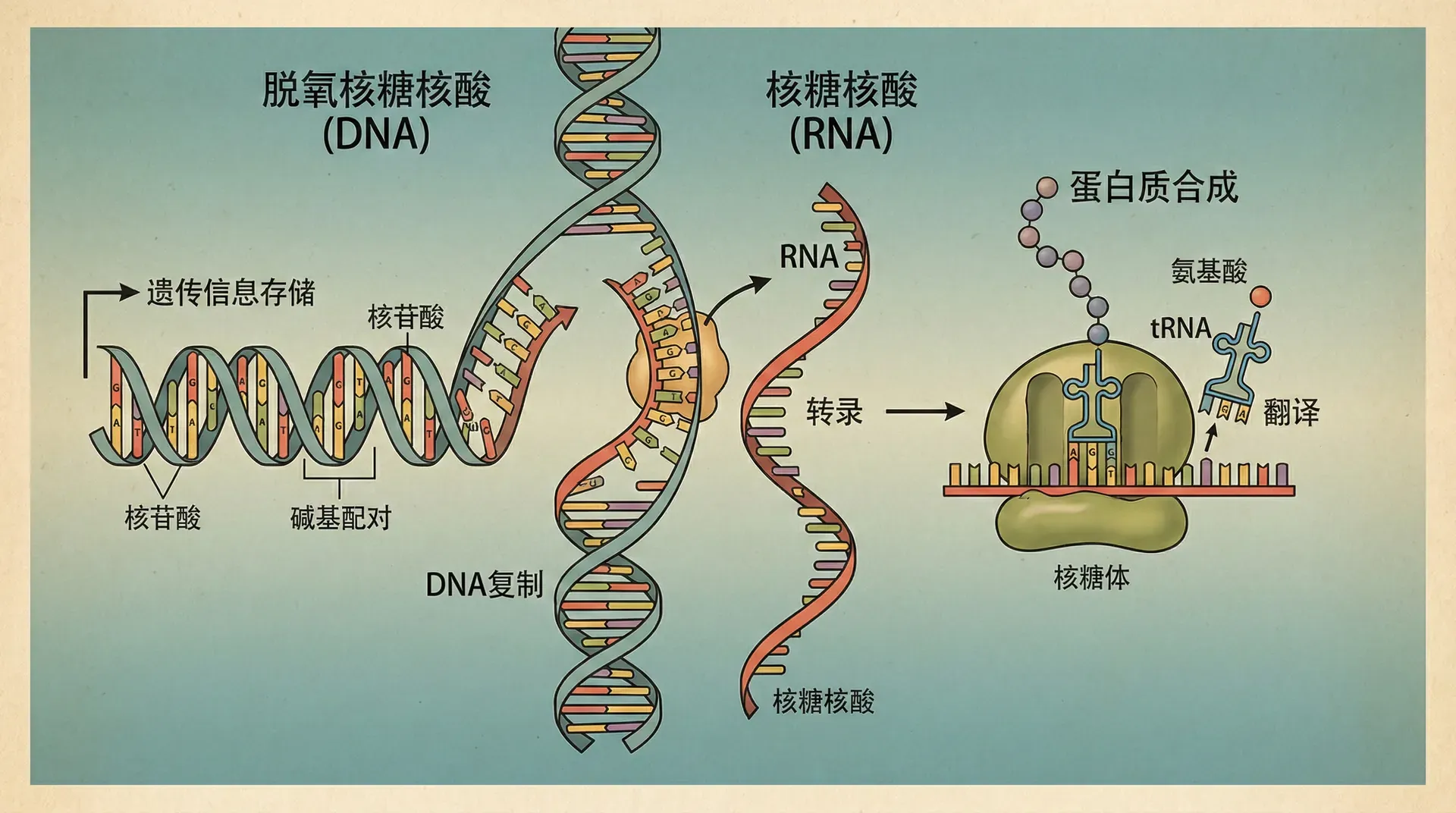
核酸作为遗传信息的核心载体,分为脱氧核糖核酸(DNA)和核糖核酸(RNA)。二者不仅在化学组成上不同,在结构和功能上也各具特色。
DNA的双螺旋结构
DNA的最著名的结构特征是右手双螺旋,由两条互补的多核苷酸链通过碱基配对(A-T,G-C)形成稳定螺旋。如下表所示,DNA碱基配对是通过氢键实现特异识别:
DNA双螺旋的直径约2纳米,每个螺距为3.4纳米(含约10对碱基)。其糖-磷酸骨架带负电荷,因此DNA分子具有良好的水溶性和相对较强的稳定性。人类基因组全长拉开大约有2米,但能在细胞核内高度紧密折叠。
RNA的结构与功能多样性
RNA常以单链形式存在,但局部可形成二级结构如发卡环、茎环等。RNA采用核糖为糖基,尿嘧啶(U)替代胸腺嘧啶。RNA不仅仅是DNA的“信息中介”,还包含多种功能类型:
- 信使RNA(mRNA): 携带DNA编码信息,指导蛋白质合成。例如新冠mRNA疫苗即利用这一途径。
- 转运RNA(tRNA): 识别mRNA密码子,转运特定氨基酸运送至核糖体进行蛋白组装。
- 核糖体RNA(rRNA): 构成核糖体主体,并直接参与蛋白质合成的催化。
- 小RNA如miRNA/siRNA: 基因表达调控、RNA剪接与降解等功能。
实际应用中,例如植物体内miRNA可用于逆境适应,动物细胞的tRNA修饰类型作为疾病诊断生物标志物等,这些都是RNA功能多样性的体现。
理解DNA和RNA的结构差异及其化学性质是分子生物学实验成功的基础。RNA分子含有2'羟基,较DNA更容易在碱性条件下水解。同时,环境中遍布稳定的RNA酶(RNase),操作时需戴手套并用专用无RNA酶试剂,力避降解污染。
实验室实践要点
在配制和处理生物大分子溶液时,需综合考虑缓冲体系、pH值、离子强度、添加剂等多重因素。实验前应规划好方案,备齐所需器材和所有试剂。
溶液配制及处理要点
- 缓冲液选择与溶解: 根据蛋白等电点及实验目的确定pH,并选择合适的缓冲体系。工作pH建议与等电点相差2个单位以上,以避免蛋白聚集沉淀。称量蛋白粉建议在冰浴下操作,溶解时轻柔混匀,避免剧烈振荡和气泡产生。难溶时可4℃冰箱过夜,不宜加热或快速搅拌。
- 清除杂质: 溶解后的溶液需离心(通常10000–15000 g,10–15分钟)或用0.22/0.45 μm低蛋白结合滤膜过滤去除不溶物。取上清或过滤时注意避免交叉污染。
质量控制与检验
记录与样品追溯
每份溶液须详细记录配制日期、配制人、组分来源及批号、浓度、pH、储存条件、质量检验结果等,并在容器贴有名称、浓度、日期和有效期。对于关键生物样品,建议建立完整管理系统,分配唯一编号并保留来源、纯化、分装和使用详情,便于问题追查和溯源。
在中国的药品生产和临床检测实验室,生物大分子溶液必须遵循GMP或ISO 15189等规范进行配制和管理,以保证产品质量与检测数据的可靠性。