基因工程的基本操作
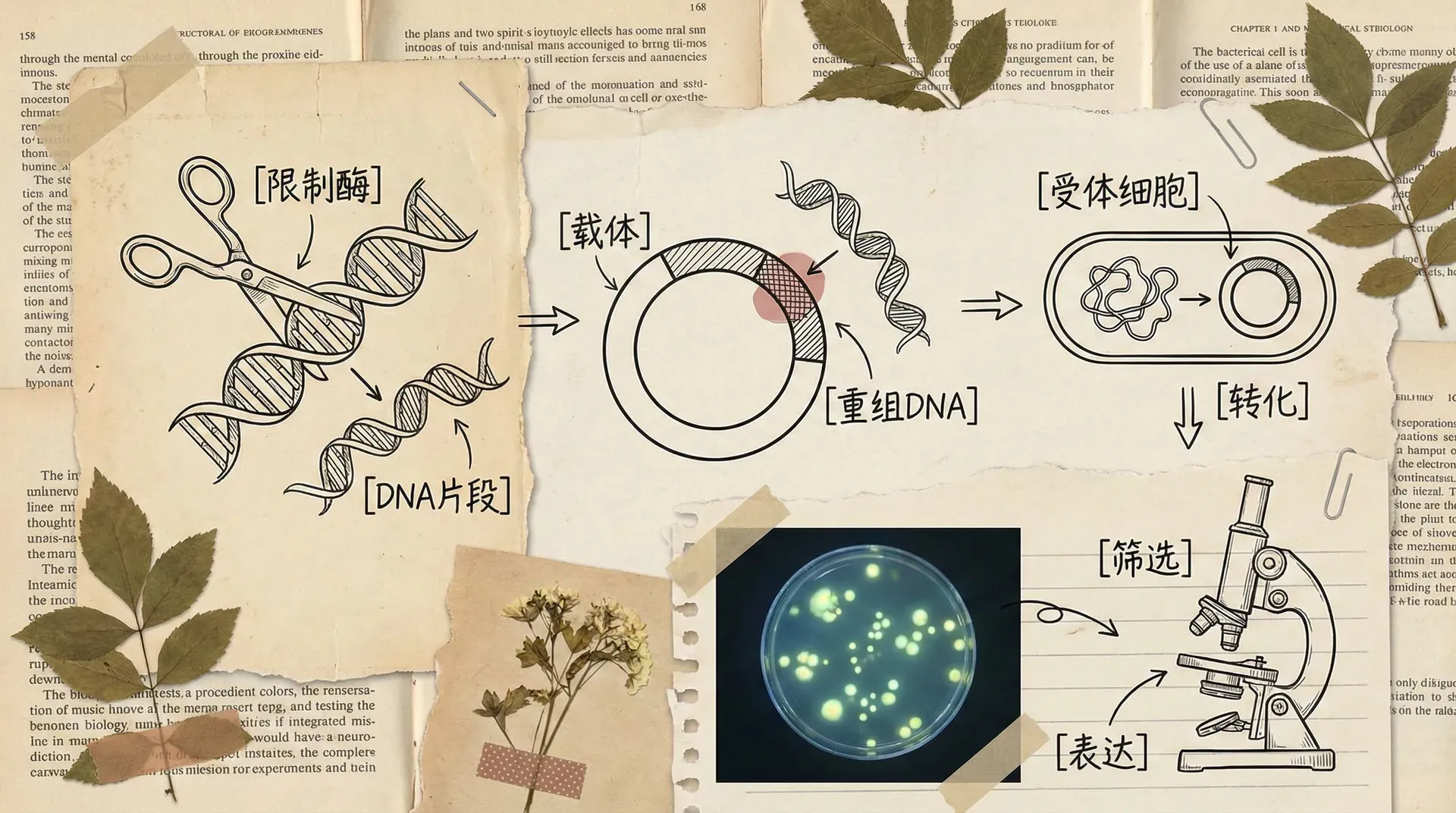
在二十世纪七十年代,生物学家们取得了一项革命性的突破。他们首次利用现代分子生物学技术,将一种生物的基因——即带有特定遗传信息的DNA片段——成功地转移到另一种生物体内,并使其能够正常表达,从而赋予受体生物全新的性状。这一壮举标志着基因工程时代的正式到来,也是人类能够主动、定向地改造生物遗传物质的开端。
基因工程的诞生不仅是生命科学发展史上的里程碑,更为解决粮食短缺、疾病治疗、环境保护等诸多全球性难题开辟了全新的技术路径。自此以后,生物技术不仅深刻地影响了科学研究,而且在农业、医药、环保、工业等领域产生了广泛而深远的应用。例如,通过基因工程可以培育抗病、抗虫的农作物新品种,显著提高粮食产量和安全性;也可以让细菌、酵母等微生物成为“工厂”,批量生产人类所需的胰岛素、生长激素等药物,极大地改善了疾病治疗手段。
如果我们能够像编辑文章一样编辑和重组生物的遗传信息——比如将抗病或高产基因转入普通农作物,使其变得更优良;或者让细菌拥有制造人类蛋白药物的能力,为难治疾病的患者带来希望——这将为人类社会带来怎样翻天覆地的变革。这正是基因工程技术不断发展所实现的“生命奇迹”。
值得一提的是,中国科学家在分子生物学和基因工程领域取得了许多具有国际影响力的重大成就。早在1965年,中国科学家就成功实现了世界上首次人工全合成结晶牛胰岛素,这一划时代的壮举不仅在国际学术界引起巨大反响,更为后来中国基因工程技术的发展奠定了坚实的理论和技术基础。随着科学技术的进步,如今中国已在基因工程药物研发、转基因作物培育等多个领域跻身世界前列,为人类健康和社会进步作出了突出贡献。
基因工程的概念与原理
什么是基因工程
基因工程是指按照人们的意愿,运用现代分子生物学技术,将某个生物的目的基因提取出来,在体外进行剪切、拼接等操作后,导入另一个生物体内,使其表达出原来不具有的性状。这个过程也被称为基因拼接技术或DNA重组技术。
基因工程的核心思想是将基因看作可以操作的“零件”。就像我们可以将一台机器的零件拆卸下来,装配到另一台机器上一样,基因工程技术使我们能够将一个生物的基因“移植”到另一个生物体内。这种跨越物种界限的基因转移,在自然界中是极其罕见的,但通过基因工程技术却可以轻松实现。
基因工程的理论基础
基因工程的实现依赖于几个重要的理论基础:
基因工程技术的成功应用建立在对生物遗传规律深刻理解的基础上。遗传密码的通用性是基因工程跨物种操作的关键前提。
基因工程的特点与优势
基因工程技术具有几个显著的特点。
-
定向性强。传统的育种方法依赖于自然变异和人工选择,过程漫长且结果不可预测。而基因工程可以精确地将特定基因导入目标生物,实现定向改造。
-
突破物种界限。基因工程可以将任何生物的基因转移到另一个生物体内,这在传统育种中是不可能实现的。
-
周期短、效率高。传统育种往往需要数年甚至数十年才能培育出新品种,而基因工程技术可以在较短时间内获得目标性状。
-
可以创造自然界不存在的新性状组合。通过将来自不同生物的多个基因组合在一起,可以创造出自然界从未出现过的新生物类型。
基因工程的工具

基因工程的实施需要一套特殊的“工具”,这些工具主要是一些具有特殊功能的酶和载体。它们就像外科医生手中的手术刀、缝合针和运输工具,使得基因的精确操作成为可能。
限制性核酸内切酶
限制性核酸内切酶,简称限制酶,是基因工程中最重要的工具之一。这类酶能够识别DNA分子上的特定核苷酸序列,并在特定位置切割DNA双链。限制酶最初是在细菌中发现的,它们是细菌的一种防御机制,用于切割入侵的病毒DNA。
限制酶的命名通常包含三个部分。以EcoRI为例,“Eco”代表来源菌种(大肠杆菌Escherichia coli),“R”代表菌株,“I”代表该菌株产生的第一种限制酶。目前已经发现了数百种限制酶,它们识别不同的DNA序列,为基因工程提供了丰富的工具选择。
限制酶的一个重要特性是能够产生“粘性末端”。当限制酶切割DNA时,往往不是平齐切割,而是产生单链突出的末端。这些突出的单链末端可以与其他具有互补序列的DNA片段通过碱基配对结合,就像拼图的凸凹部分可以互相咬合一样。这个特性为不同来源的DNA片段的连接提供了便利。
限制酶的发现是基因工程技术发展的关键突破。它使得科学家能够在分子水平上精确地"剪切"DNA,为基因操作提供了可能。
DNA连接酶
如果说限制酶是基因工程的“剪刀”,那么DNA连接酶就是基因工程的“针线”。DNA连接酶能够将两个DNA片段的末端连接起来,形成一个完整的DNA分子。在细胞内,DNA连接酶的主要作用是修复DNA链的断裂,参与DNA复制和修复过程。
在基因工程中常用的DNA连接酶主要有两种:
DNA连接酶的工作原理是催化DNA链中相邻核苷酸之间形成磷酸二酯键。当两个DNA片段的末端靠近时,DNA连接酶能够识别并结合到这个位置,催化化学键的形成,从而将两个片段牢固地连接在一起。这个过程需要消耗能量,通常由ATP提供。
运载体
目的基因被切割下来后,需要一个“运输工具”将其送入受体细胞,并使其能够在受体细胞内复制和表达。这个“运输工具”就是运载体,也称为载体。载体是基因工程中不可或缺的工具,它就像一辆货车,将目的基因安全地运送到目的地。
理想的载体需要具备几个重要特征。首先,载体必须能够在宿主细胞内自主复制,这样目的基因才能随着载体的复制而扩增。其次,载体应该具有标记基因,便于筛选含有重组DNA的细胞。第三,载体上应该有多个限制酶切割位点,方便目的基因的插入。第四,载体的分子量不宜过大,否则不利于操作和导入细胞。
质粒是最常用的载体之一。质粒是存在于细菌细胞质中的小型环状DNA分子,它独立于细菌染色体进行复制。天然质粒通常携带一些对细菌有利的基因,如抗生素抗性基因。科学家们对天然质粒进行改造,使其成为理想的基因工程载体。
以常用的质粒pBR322为例,它含有氨苄青霉素抗性基因和四环素抗性基因,这两个基因可以作为标记基因用于筛选。质粒上还有多个限制酶切割位点,可以方便地插入外源基因。当含有重组质粒的细菌在含有抗生素的培养基上生长时,只有携带抗性基因的细菌才能存活,从而实现对转化细菌的筛选。
基因工程的基本步骤
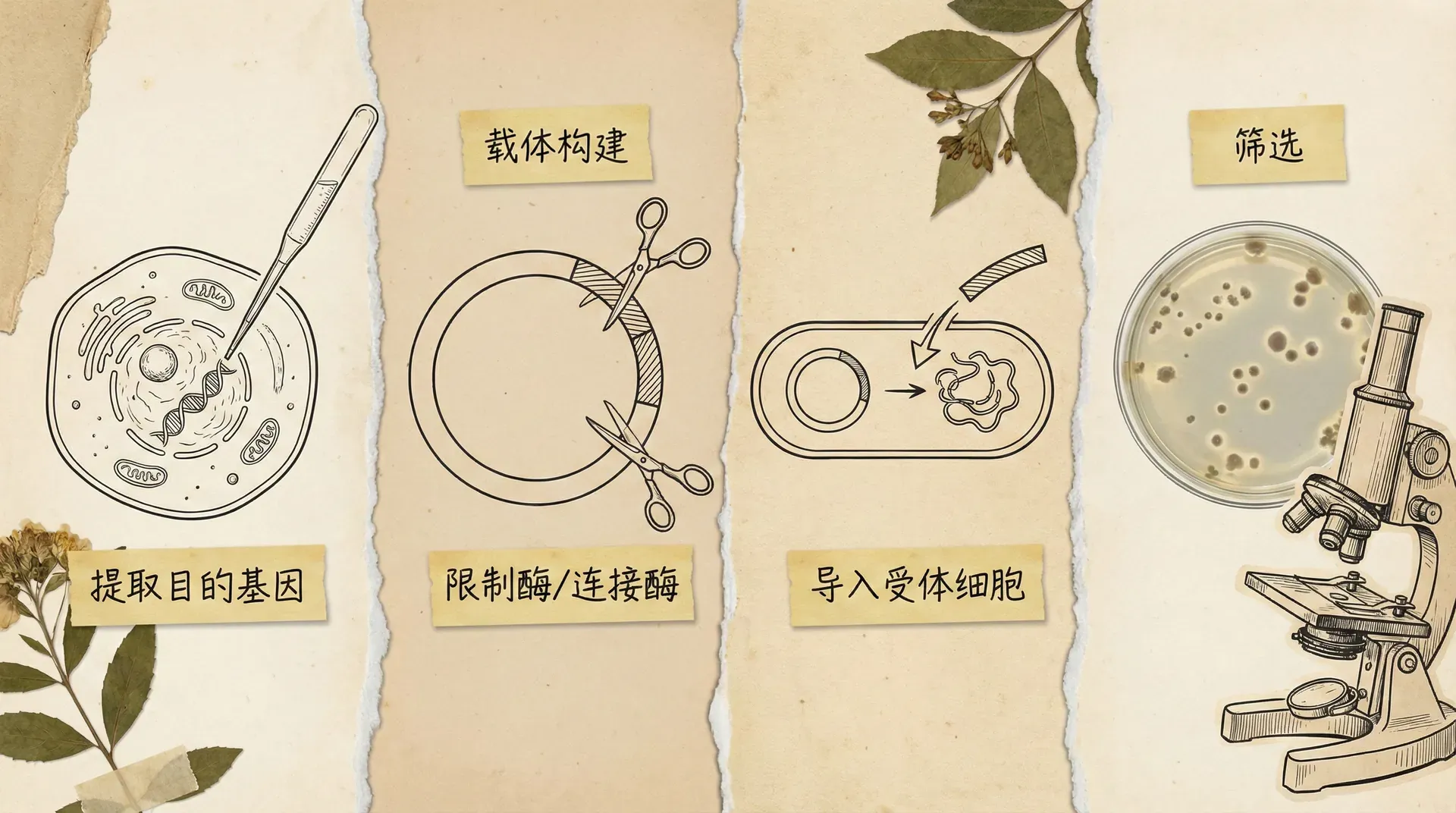
基因工程的实施是一个系统工程,包括四个基本步骤。这四个步骤环环相扣,每一步都至关重要。我们可以将整个过程比喻为一次精密的“基因移植手术”。
获取目的基因
获取目的基因是基因工程的第一步,也是关键的一步。目的基因是指我们希望转移到受体细胞中的特定基因。获取目的基因有多种方法,每种方法都有其适用的场合。
基因工程的四个基本步骤——获取目的基因、构建表达载体、导入受体细胞、筛选鉴定,构成了一个完整的技术体系。每一步都需要精心设计和严格操作,才能确保基因工程的成功。
PCR技术
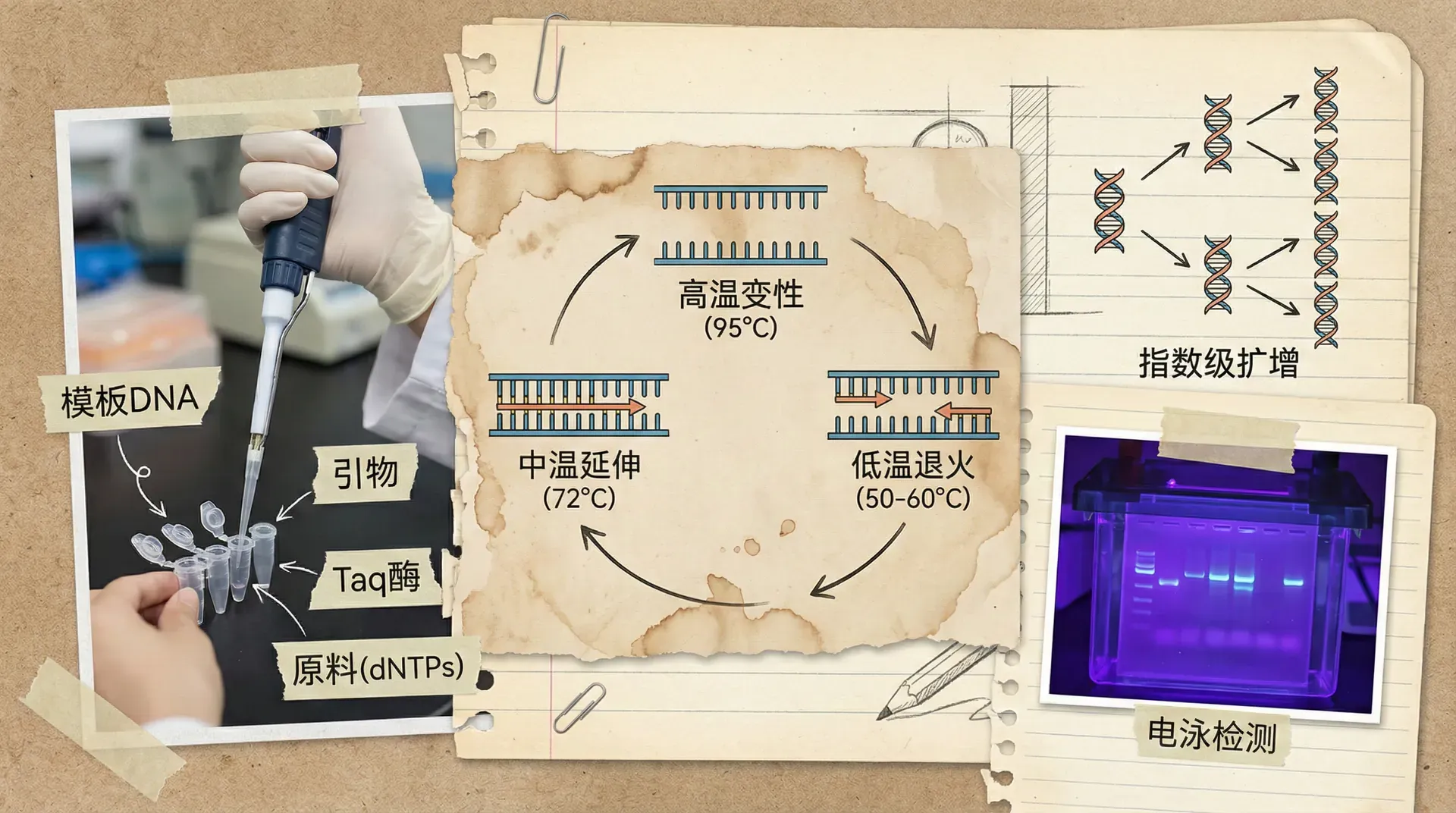
PCR技术的原理
聚合酶链式反应(Polymerase Chain Reaction,简称PCR)是一种在体外快速扩增特定DNA片段的技术。这项技术由美国科学家凯利·穆利斯(Kary Mullis)于1983年发明,他也因此获得了1993年的诺贝尔化学奖。PCR技术的出现极大地推动了分子生物学的发展,被誉为分子生物学的“革命”。
PCR技术的基本原理模拟了细胞内DNA复制的过程,但整个反应在试管中进行,不需要细胞的参与。PCR反应需要几个关键成分。第一是模板DNA,即含有目标序列的DNA分子。第二是引物,这是两段短的单链DNA,分别与目标序列的两端互补。第三是DNA聚合酶,通常使用耐高温的Taq DNA聚合酶。第四是四种脱氧核苷酸(dNTP),作为合成新DNA链的原料。
PCR反应包括三个基本步骤,这三个步骤在不同温度下循环进行。
变性,在94-95℃的高温下,DNA双链解开成为单链。
退火,温度降至50-60℃,引物与模板DNA的互补序列结合。
延伸,温度升至72℃,DNA聚合酶从引物的3'端开始,沿着模板链合成新的DNA链。
这三个步骤构成一个循环。每完成一个循环,目标DNA片段的数量就增加一倍。经过n个循环后,理论上可以得到2ⁿ个目标DNA分子。通常进行25-35个循环,就可以将极微量的DNA扩增到可以检测和使用的水平。例如,经过30个循环,一个DNA分子可以扩增到约10亿个拷贝。
PCR技术的应用
PCR技术由于其快速、高效、灵敏的特点,在多个领域得到了广泛应用。在基因工程中,PCR技术可以快速扩增目的基因,为基因克隆提供充足的材料。在医学诊断中,PCR技术可以检测病原体的DNA,实现疾病的早期诊断。
在新冠疫情期间,PCR检测成为了最主要的病毒检测方法。通过检测病毒的核酸,可以快速准确地判断是否感染。PCR技术的高灵敏度使得即使在感染早期,病毒量很少的情况下,也能够检测出来。中国在疫情防控中大规模应用PCR检测技术,为疫情防控做出了重要贡献。
在法医学中,PCR技术可以用于DNA指纹鉴定。每个人的DNA序列都是独特的(同卵双胞胎除外),通过PCR扩增特定的DNA片段,分析其长度和序列,可以进行个体识别。这项技术在刑事侦查、亲子鉴定、灾难遇难者身份确认等方面发挥着重要作用。
在考古学和进化生物学研究中,PCR技术可以从古老的生物样本中扩增DNA。即使是几千年前的木乃伊或化石中残存的微量DNA,也可以通过PCR技术进行扩增和分析,为研究古代生物和人类进化提供了宝贵的信息。
PCR技术虽然强大,但也需要严格的操作规范。实验室污染、引物设计不当、反应条件不优化等都可能导致假阳性或假阴性结果。因此在应用PCR技术时,必须建立严格的质量控制体系。
基因工程的发展历程
基因工程技术的发展是众多科学家共同努力的结果。1953年,沃森和克里克提出DNA双螺旋结构模型,为基因工程奠定了理论基础。1970年,科学家们发现了限制性核酸内切酶和DNA连接酶,为基因操作提供了工具。1973年,科恩和博耶首次成功构建了重组DNA分子,标志着基因工程技术的诞生。
1978年,科学家们利用基因工程技术,使大肠杆菌生产出人胰岛素,这是基因工程技术的第一个重要应用。1983年,PCR技术的发明使得基因扩增变得简单快捷。1996年,世界上第一只克隆哺乳动物多莉羊诞生,展示了基因工程技术的巨大潜力。
中国在基因工程领域也取得了重要成就。1965年,中国科学家在世界上首次人工合成了结晶牛胰岛素。1981年,中国科学家成功克隆了人生长激素基因。1988年,中国培育出第一批转基因鱼。2000年,中国参与完成了人类基因组计划,承担了1%的测序任务。这些成就展示了中国科学家在基因工程领域的实力。
基因工程面临的挑战
尽管基因工程技术取得了巨大成就,但在发展过程中也面临着一些挑战。
基因工程技术的应用必须遵循安全性和伦理性原则。任何基因工程产品在应用前都必须经过严格的安全评估,确保不会对人类健康和生态环境造成危害。
总结
基因工程是现代生物技术的核心,它使人类能够按照自己的意愿改造生物的遗传特性。基因工程的实现依赖于限制酶、DNA连接酶和载体等工具,通过获取目的基因、构建表达载体、导入受体细胞、筛选鉴定等步骤来完成。PCR技术作为基因工程的重要辅助技术,能够快速扩增特定的DNA片段,在多个领域得到广泛应用。
基因工程技术的发展为解决人类面临的粮食、医药、环境等问题提供了新的途径。但同时,我们也必须认识到基因工程技术面临的挑战,包括技术难题、安全性问题、伦理争议等。只有在科学、理性、负责任的态度下发展和应用基因工程技术,才能使其真正造福人类。
本节练习
第一题:下列关于基因工程工具的叙述,正确的是
A. 限制酶只能识别和切割病毒DNA,不能切割细菌DNA
B. DNA连接酶只能连接具有粘性末端的DNA片段
C. 质粒是基因工程中常用的载体,它能在宿主细胞中自主复制
D. 所有的限制酶切割DNA后都会产生粘性末端
答案:C
解析: A选项错误。限制酶能够识别特定的DNA序列并进行切割,不管这段DNA来自病毒、细菌还是其他生物。限制酶最初在细菌中发现,是细菌用来防御外来DNA的工具,但它也能切割细菌自身的DNA(细菌通过甲基化保护自己的DNA)。
B选项错误。虽然大肠杆菌来源的DNA连接酶只能连接粘性末端,但T4噬菌体来源的DNA连接酶既能连接粘性末端,也能连接平末端。因此不能说DNA连接酶只能连接粘性末端。
C选项正确。质粒是存在于细菌细胞质中的小型环状DNA分子,能够独立于染色体进行复制。这个特性使质粒成为理想的基因工程载体。质粒上通常还含有标记基因(如抗生素抗性基因)和多个限制酶切割位点,便于目的基因的插入和筛选。
D选项错误。不同的限制酶切割DNA的方式不同。有些限制酶切割后产生粘性末端(单链突出),有些则产生平末端(双链平齐)。例如,EcoRI产生粘性末端,而SmaI产生平末端。
本题考查的知识点: 基因工程的工具酶和载体的特性,包括限制酶的作用特点、DNA连接酶的功能、质粒载体的特征等。
第二题:在基因工程中,要将人的胰岛素基因导入大肠杆菌并使其表达,应选用下列哪种方法获取目的基因
A. 直接从人的胰腺细胞中提取胰岛素基因
B. 以人胰腺细胞的mRNA为模板,反转录合成cDNA
C. 用限制酶从人的染色体DNA中切割出胰岛素基因
D. 利用PCR技术直接从人的基因组DNA中扩增胰岛素基因
答案:B
解析: 这道题考查的是真核基因在原核生物中表达的特殊性。人的胰岛素基因是真核基因,含有内含子和外显子。如果直接将含有内含子的基因导入大肠杆菌,由于大肠杆菌缺乏剪接内含子的机制,无法正确表达该基因。
A选项错误。虽然可以从胰腺细胞中提取DNA,但提取的基因组DNA中的胰岛素基因含有内含子,无法在大肠杆菌中正常表达。
B选项正确。胰腺细胞中的mRNA是经过加工的成熟mRNA,已经去除了内含子,只保留外显子序列。以mRNA为模板,利用反转录酶合成cDNA,得到的基因不含内含子,可以在大肠杆菌中正常转录和翻译。这是将真核基因在原核生物中表达的常用方法。
C选项错误。用限制酶切割得到的基因仍然含有内含子,无法在大肠杆菌中正确表达。而且限制酶的切割位点是特定的,不一定正好在目的基因的两端,可能会切到基因内部或者切不到合适的位置。
D选项错误。虽然PCR技术可以扩增基因,但如果模板是基因组DNA,扩增出的基因仍然含有内含子。除非模板是cDNA,否则扩增出的基因无法在大肠杆菌中正常表达。
本题考查的知识点: 真核基因的结构特点(含有内含子和外显子)、原核生物的基因表达特点(不能剪接内含子)、反转录技术在基因工程中的应用。
第三题:下列关于PCR技术的叙述,错误的是
A. PCR技术可以在体外快速扩增特定的DNA片段
B. PCR反应需要耐高温的DNA聚合酶,如Taq酶
C. PCR反应的三个步骤是变性、复性、延伸
D. 经过n个循环后,目标DNA分子的数量可以达到2ⁿ个
答案:C
解析: 这道题考查PCR技术的基本原理和过程。
A选项正确。PCR(聚合酶链式反应)技术的核心功能就是在体外快速扩增特定的DNA片段。这项技术不需要细胞参与,在试管中就可以完成,而且速度很快,几个小时就可以完成数十个循环的扩增。
B选项正确。PCR反应过程中需要在94-95℃的高温下使DNA变性,普通的DNA聚合酶在这样的高温下会失活。因此PCR反应使用的是从嗜热菌(如栖热水生栖热菌)中提取的耐高温DNA聚合酶,最常用的是Taq DNA聚合酶,它在高温下仍能保持活性。
C选项错误。PCR反应的三个基本步骤应该是:变性(denaturation)、退火(annealing)、延伸(extension)。变性是指在高温下DNA双链解开;退火是指引物与模板DNA结合;延伸是指DNA聚合酶合成新链。选项中说的“复性”不够准确,“退火”才是标准术语。复性通常指DNA双链的重新结合,而退火特指引物与模板的结合过程。
D选项正确。PCR反应每个循环都使目标DNA数量翻倍,因此理论上经过n个循环后,一个DNA分子可以扩增到2ⁿ个。例如,经过30个循环,可以扩增到约10亿个拷贝(2³⁰≈10⁹)。实际操作中,由于各种因素的影响,扩增效率可能达不到理论值,但仍然可以实现百万倍以上的扩增。
本题考查的知识点: PCR技术的原理、反应条件、反应步骤和扩增效率等基础知识。
第四题:在基因工程操作中,下列有关载体的叙述正确的是
A. 载体必须具有多个不同限制酶的单一切割位点
B. 载体上的标记基因有利于筛选含有重组DNA的细胞
C. 质粒载体只能用于原核生物的基因工程
D. 载体的分子量越大越好,可以携带更多的目的基因
答案:B
解析: 这道题考查基因工程载体的特征和功能。
A选项错误。虽然载体上确实需要有限制酶切割位点以便插入目的基因,但不一定必须是“多个不同限制酶的单一切割位点”。实际上,载体上可以有一个或多个限制酶切割位点,关键是这些位点不能位于载体的关键功能区域(如复制起点、标记基因等),否则会破坏载体的功能。有些载体设计有多克隆位点(MCS),包含多种限制酶的切割位点,便于选择合适的酶进行操作。
B选项正确。标记基因是载体的重要组成部分,最常用的是抗生素抗性基因。当载体导入细胞后,只有成功接受载体的细胞才具有标记基因表达的性状(如抗生素抗性)。通过在含有相应抗生素的培养基上培养,可以筛选出含有载体的细胞,而没有载体的细胞会被抗生素杀死。这大大提高了筛选效率。
C选项错误。虽然质粒载体最常用于原核生物(如大肠杆菌)的基因工程,但经过改造的质粒也可以用于真核生物。例如,酵母表达载体就是一种可以在酵母细胞中复制和表达的质粒。此外,还有一些穿梭载体,可以在原核生物和真核生物之间转移。
D选项错误。载体的分子量并非越大越好。载体太大会给操作带来困难,不利于导入细胞,复制效率也可能降低。理想的载体应该大小适中,既能容纳目的基因,又便于操作和转化。常用的质粒载体通常在几千到几万碱基对之间。如果需要克隆大片段DNA,可以选择噬菌体载体或人工染色体载体。
本题考查的知识点: 基因工程载体的基本特征,包括限制酶切割位点、标记基因的作用、载体的适用范围和大小选择等。
第五题:请简述基因工程的四个基本步骤,并说明每个步骤的主要目的和常用方法。
参考答案:
基因工程包括四个基本步骤,每个步骤都有其特定的目的和方法。
第一步:获取目的基因
目的是从供体生物中分离出我们需要转移的特定基因。常用方法包括:
从基因文库中筛选目的基因,适用于已知功能但序列未知的基因。利用PCR技术扩增目的基因,这是目前最常用的方法,前提是已知目的基因的序列信息。人工合成目的基因,适用于小基因或需要密码子优化的基因。反转录法,即以成熟mRNA为模板合成cDNA,这种方法特别适合将真核基因在原核生物中表达,因为得到的cDNA不含内含子。
第二步:构建基因表达载体
目的是将目的基因与载体DNA连接,形成能够在受体细胞中复制和表达的重组DNA分子。主要步骤包括:
用同一种限制酶分别切割目的基因和载体DNA,使它们产生相同的粘性末端。将切割后的目的基因和载体DNA混合,在DNA连接酶的作用下连接,形成重组DNA。在构建表达载体时,需要确保目的基因位于启动子的下游,这样才能正常转录。还需要包含终止子、标记基因等必要元件。
第三步:将重组DNA导入受体细胞
目的是将构建好的重组DNA转移到受体细胞中。不同类型的细胞采用不同的方法:
对于细菌细胞,常用Ca²⁺处理法制备感受态细胞,然后通过热激使DNA进入细胞。对于植物细胞,可以使用农杆菌转化法或基因枪法。农杆菌转化法利用农杆菌的天然基因转移能力,基因枪法则是用物理方法将DNA直接射入细胞。对于动物细胞,可以使用显微注射法、电穿孔法或病毒载体法。
第四步:筛选含有目的基因的细胞
目的是从大量细胞中找出成功导入目的基因的细胞。主要方法包括:
利用标记基因进行初步筛选,例如在含有抗生素的培养基上培养,只有含有抗性基因的细胞能够存活。使用蓝白斑筛选法进行更精确的筛选。通过PCR、DNA测序、Southern杂交等方法鉴定目的基因是否存在。通过Western杂交或酶活性测定等方法检测目的蛋白是否表达。
这四个步骤环环相扣,共同构成了完整的基因工程技术体系。每个步骤都需要精心设计和严格操作,才能确保基因工程的成功。
第六题:简要说明PCR技术的基本原理,并举例其在医学和法医学中的一种应用。
参考答案:
PCR技术的基本原理:
PCR(聚合酶链式反应)是一种在实验室中快速扩大量少的特定DNA片段的方法。其基本思路是利用DNA聚合酶和一对专门设计的引物,使目标DNA片段在3个步骤中循环扩增:
- 变性:高温使DNA双链分开成为单链;
- 退火:温度降低,引物结合到目标DNA片段的两端;
- 延伸:DNA聚合酶利用引物起始,沿模板合成新的DNA链。
如此循环多次,大量扩增特定DNA序列。
PCR技术的应用举例:
- 医学:用PCR检测新冠病毒感染。即使病人体内病毒很少,PCR也能扩增病毒的DNA或RNA,帮助快速准确诊断感染。
- 法医学:通过PCR扩增犯罪现场留下的极少量DNA样本,如头发或血迹,进行个人身份鉴定(DNA指纹),辅助案件侦破。