扩散与运输
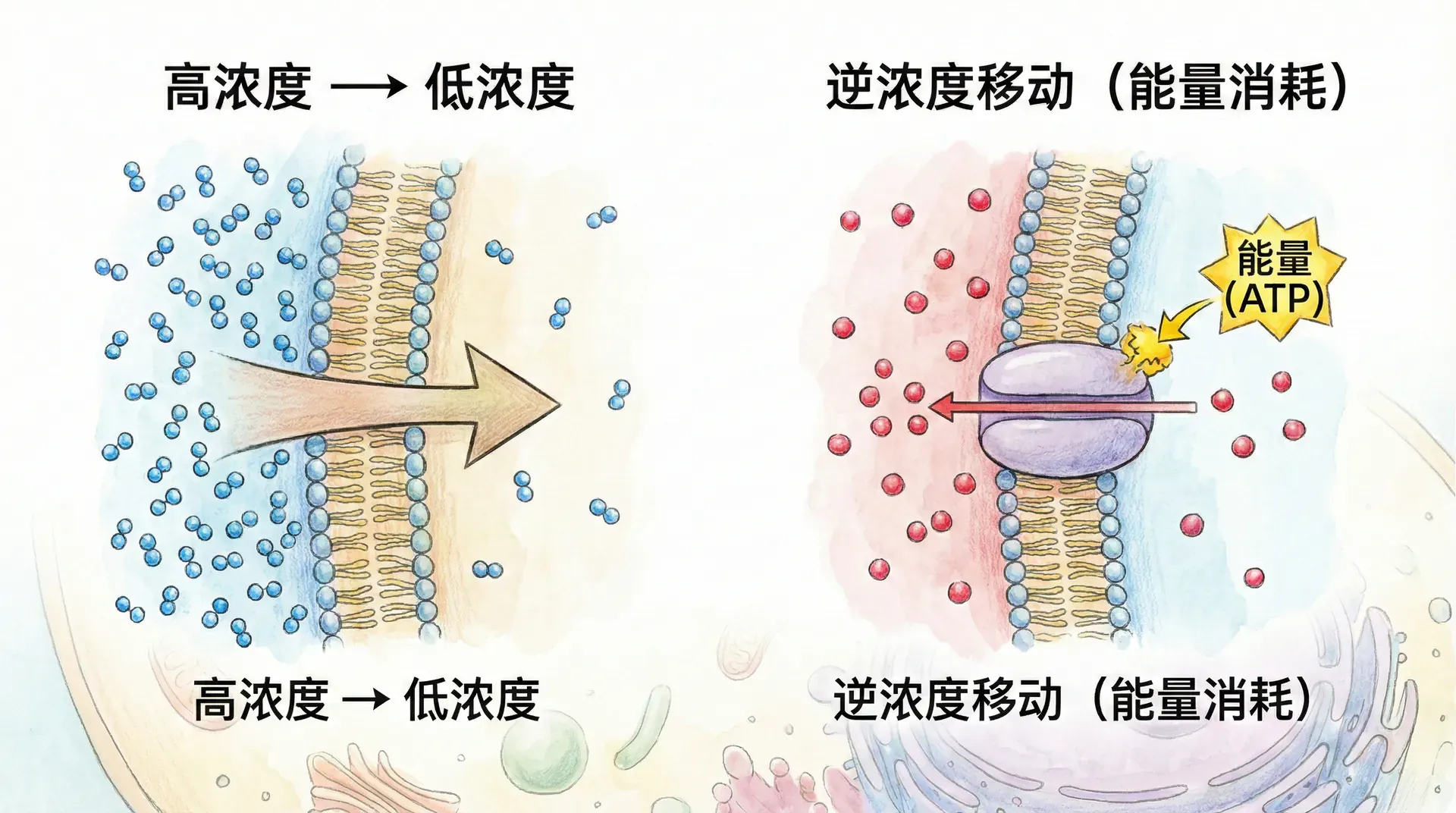
生命活动离不开分子的运动,无论是在细胞外环境中,还是在极其复杂的细胞内部。分子的扩散和运输机制不仅决定了能量、信息与物质在生物体中的传递效率,也是细胞适应和响应外界环境变化的基础。比如,氧气和二氧化碳通过扩散跨越细胞膜实现气体交换,激素和神经递质通过扩散或主动运输实现信号传导,蛋白质和RNA等大分子可以依赖胞内运输系统进行定向分布,细胞内废弃物也需要依靠转运机制及时清除。除此之外,病原体入侵、药物分布、组织再生等重要生理和医学现象也都和分子的扩散、运输方式密不可分。
理解这些扩散与运输的物理本质,不仅有助于揭开生命行为背后的规律,还为药物设计、疾病治疗和先进生物技术开发提供理论指导。例如,通过调控分子的扩散效率,可以提高药物到达病灶的能力,或者优化组织工程中营养物质的均匀供应。因此,深入学习分子的扩散和主动运输原理,是现代生物科学与生物医学的重要基础。
随机游走
布朗运动的发现
1827年,英国植物学家布朗在显微镜下观察花粉颗粒时,发现这些微小颗粒在水中做着不规则的运动。这种看似混乱的运动现象后来被称为布朗运动。长久以来,这一现象让科学家困惑不已:难道真的有哪种“看不见的力”在推动这些颗粒?直到爱因斯坦在1905年提出理论解释,人们才认识到这种运动反映了分子热运动的统计性质。随后,法国物理学家让·佩兰通过实验测量颗粒运动,间接验证了原子的存在,为原子论提供了重要证据。
在细胞内环境中,蛋白质分子同样在进行着类似的随机运动。想象一个蛋白质分子在细胞质中的“漫步”:它不断地与周围的水分子发生碰撞,每次碰撞都会改变它的运动方向和速度。这种运动轨迹是完全不可预测的,就像醉汉在街道上行走一样。而且,这种随机运动赋予了分子到达目标位置的“概率”,也使得细胞中的过程具备高度的动态灵活性。例如,信号分子通过扩散传递信息,速度取决于它们随机游走的统计特性。
随机游走的数学描述
我们可以用一个简单而经典的模型来描述分子的随机运动:一维随机游走。设想一个分子在一条直线上走动,每走一步有 1/2 的概率向左,也有 1/2 的概率向右。步长可以设为恒定(如一个单位长度),时间步也假设为恒定间隔。这种模型虽然简单,却揭示了分子运动背后的本质。
从图中可以看出,虽然两个分子都从同一起点出发,但它们的运动轨迹完全不同。有时右走多一些,有时左走更多,每一个轨迹都是独一无二的。这正是随机运动的特征:单个分子的运动轨迹是不可预测的,但大量分子的统计行为却遵循确定的规律。这一性质对于生物系统尤为重要,因为在细胞尺度上,生命活动经常涉及少量分子的相互作用,随机性主导了许多微观事件。
实际上,随机游走可推广到更高维空间以及考虑不同步长、不同概率等情形。例如在实际生物膜或细胞质环境中,分子的扩散往往是“三维的”,偶尔也会遇到障碍或捕获,使其运动更加复杂。
位移分布的统计特性
虽然单个分子的运动是随机且不可预测的,但当我们考虑大量分子的行为时,就会发现明确的、可重复的统计规律。例如,我们可以记录成千上万个分子的最终位置,统计它们的分布。经过足够长的时间后,分子位移的分布呈现高斯分布(正态分布)的特征,这就是所谓的中心极限定理的体现。
高斯分布,也称为正态分布,是自然界中最常见的概率分布之一。它的钟形曲线特征反映了大多数随机现象的统计规律。在随机游走下,分子的最终位移分布近似于高斯分布,其数学表达式为
对于一维随机游走,经过时间 t 后,分子的均方位移(即“平均位置的平方”)与时间成正比:
其中 D 是扩散系数,这个关系式被称为爱因斯坦关系。这意味着分子扩散的“典型距离”与时间的平方根成正比,而不是与时间成正比。这种“增长减缓”体现了扩散的本质 —— 尽管分子一直在运动,但它们离开原点的速度却随着时间推移而减缓。
从图中可以看出,随着时间的增加,位移分布变得越来越宽且越来越平坦,但始终保持高斯分布的钟形特征。分子扩散的典型距离(标准差)随着增长,“左”“右”均有可能。实际上,这种扩散现象是生物系统中许多重要过程(如物质的传递、信号的扩散、细胞因子的分布等)的物理基础。例如,神经递质在突触间隙的扩散速率、细胞内信号分子的到达概率,都能用扩散和随机游走理论加以解释。这也是生物物理学和系统生物学研究必不可少的基石知识。
扩散定律
扩散是一种普遍的物理现象,从分子到宏观的生物体系都发挥着至关重要的作用。它不仅影响物质的混合和分布,还深刻影响细胞内外物质交换、代谢和信号传递等生物学过程。理解扩散现象的定量规律,是分子生物学、生物物理和生医学等多个领域的基础。
Fick第一定律
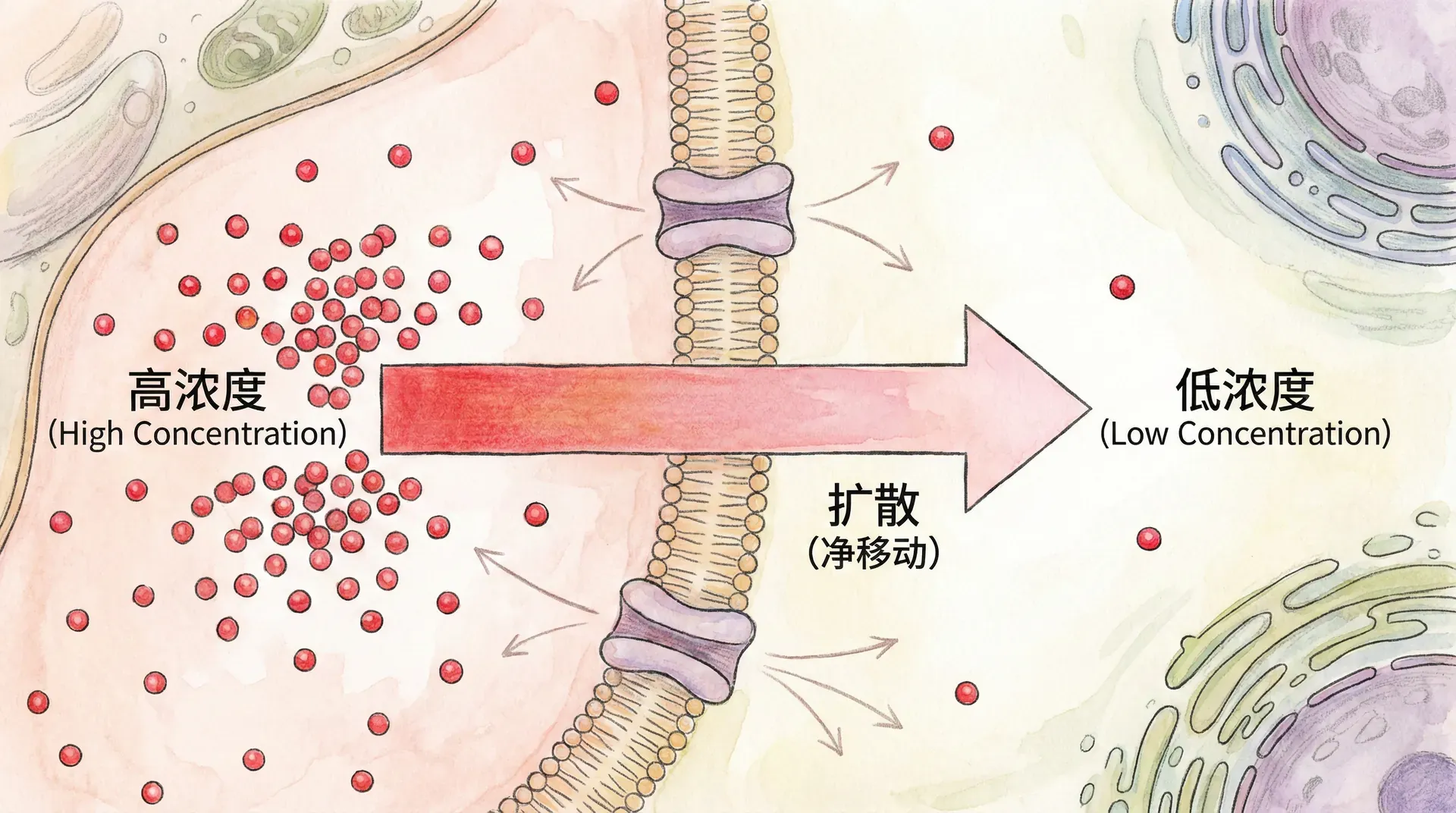
1855年,德国生理学家阿道夫·菲克(Adolf Fick)首次定量描述了扩散现象,提出了著名的Fick第一定律。Fick第一定律揭示了扩散通量(即在单位时间通过单位面积的分子数目)与空间浓度梯度之间的线性关系:
其中, 表示扩散通量(常用单位为mol/(m²·s)), 是分子的空间浓度, 是扩散系数(单位为m²/s)。负号意味着分子总是从高浓度向低浓度移动,这也是自发趋向于系统混乱、熵增加的体现。
通俗地说,Fick第一定律就像描述热量如何从高温处传导到低温处。例如,在房间一隅点燃一支香,香味分子会由点燃处(高浓度区)向远处扩散,在随后的时间内逐渐“充满”整个房间。香味扩散的速度,正是由空间中的浓度梯度和分子的扩散系数共同决定的。若空气流通缓慢,香味扩散仅靠分子热运动,遵循Fick定律;若开了风扇,则对流成为主导。
浓度差异越大,扩散速率越快;一旦环境达到均匀,扩散驱动力消失,通量变为零。这一定律是许多生理、化学工程过程如呼吸气体交换、营养传递等的核心理论支撑。
Fick第二定律
Fick第二定律进一步揭示了扩散引起的浓度分布随时间的演变:
它是第一定律和质量守恒结合的结果。公式显示,某一点上浓度的时间变化速率取决于该点处的空间二阶导数,也就是说,哪里浓度分布有“曲率”,哪里就存在净扩散。第二定律是扩散现象的动力学描述,是理解扩散“过程”不可或缺的工具。
在细胞生物学中,Fick第二定律帮助我们理解如下场景:比如葡萄糖分子如何由血管扩散进入组织细胞,信号分子如何在胞质中传播,药物如何在组织中分布等。它还能解释生物体系中为何小分子的信号响应快,大分子的传递慢。
如上图所示,如果某种分子初始时高度集中在某一位置(比如细胞内某个区域),那么随着时间推移,这些分子将逐渐扩散到周围区域,使得浓度分布变得更均匀。红色曲线是初始分布状态,其他曲线显示不同扩散时间后的分布。从尖锐到平缓,反映了分子的不断扩散和混合。这种扩散动力学对理解神经递质信号的空间扩散、营养分子扩散到细胞组织等皆有现实意义。
扩散系数的意义与影响因素
扩散系数是反映分子在介质中扩散能力的核心参数。它不仅与分子的性质相关,还受环境条件影响。对理想球形分子,扩散系数可以用著名的Stokes-Einstein方程表示:
其中为玻尔兹曼常数,为绝对温度,为溶液粘度,为分子半径。
这个公式蕴含了多个生物学与物理意义:
- 温度升高 → 分子运动加剧,扩散加快(D增大)。所以发烧时体内化学反应、分子交换的速率也会升高。
- 分子体积(半径)变大 → 分子扩散变慢(D减小)。大分子如蛋白质、DNA等在细胞内扩散远慢于小分子。
- 溶液粘度变大 → 分子扩散变慢。例如脱水或疾病等引起血液粘度升高,将影响营养物质的高效输送。
下表归纳了主要影响因素及其生物学意义:
在生理温度下,水中小分子的扩散系数通常在量级,而大分子如蛋白质的扩散系数约,相差约100倍。这也是为什么蛋白质或核酸很难仅靠扩散迅速跨越细胞。
扩散系数的巨大数量级差异,决定了细胞对大分子经常需要额外的主动运输方式(如胞吞、胞吐或分子马达)来加快效率。
生物系统中的分子运输
生物体内各种分子的空间和时间分布,既依赖随机扩散,也依赖主动运输。了解这些不同的机制,有助于我们解释生命活动的高效性和复杂性。
DNA上的一维搜索与“滑动机制”
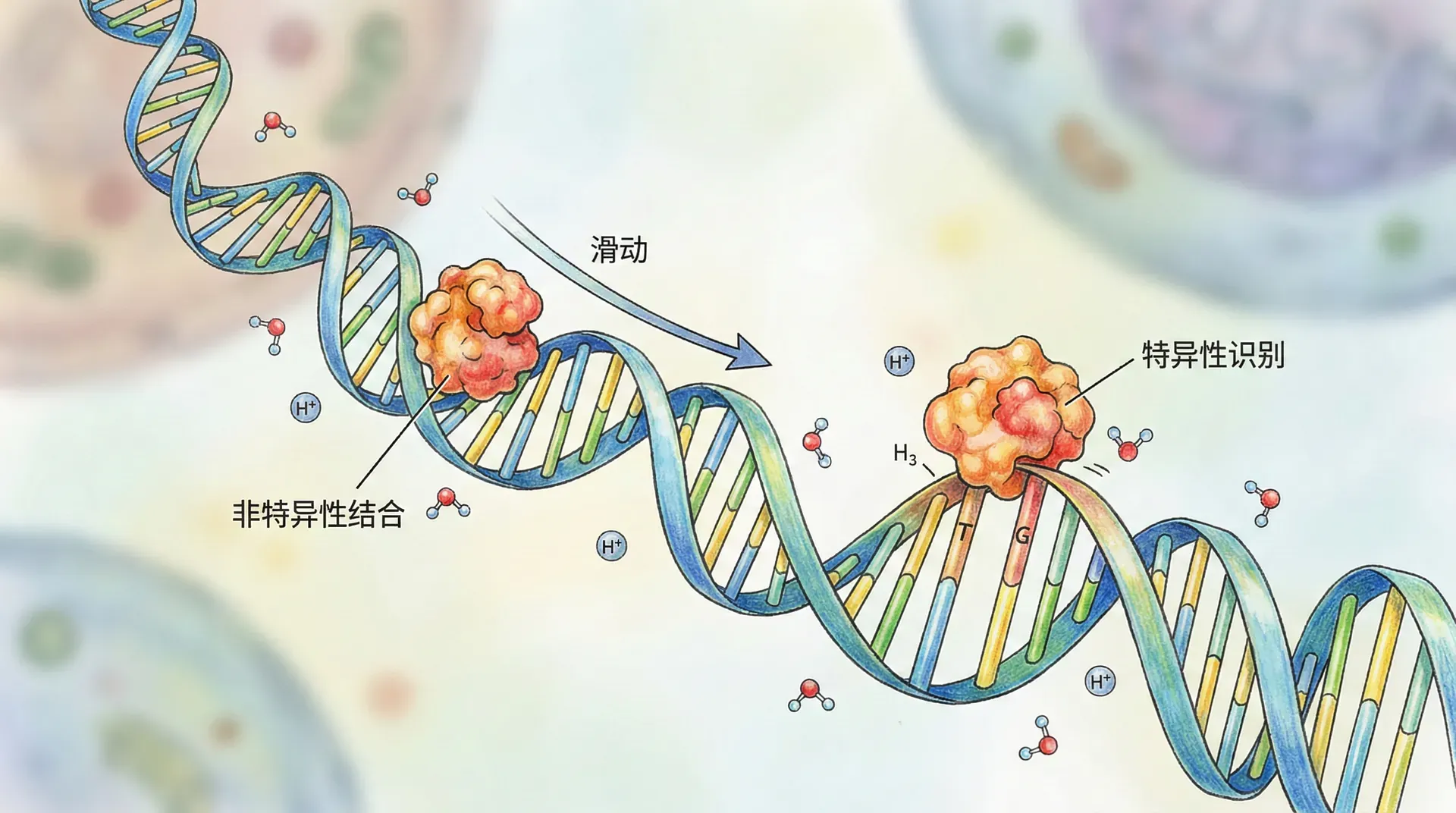
转录因子、限制性核酸酶等DNA结合蛋白需要在长达数百万碱基的基因组中迅速准确地找到自己的特异性靶点。然而,如果只靠随机的三维扩散碰撞,找到目标将极其缓慢。实验与理论研究表明,生物分子采用了“多轮驱动”的复合搜索策略:
- 首先,转录因子通过三维扩散随机碰撞到DNA任意非特异性区域;
- 随后,沿DNA链进行一维“滑动”或“爬行”——短时间内在DNA表面上顺序扫描大量碱基;
- 必要时脱离DNA再以三维扩散寻找新位置,如此循环往复。
这种机制极大地提升了靶点的寻找效率,被称为“一维滑动搜索”或“促进性扩散”。通过这种方式,分子的实际搜索效率可以比纯粹的三维扩散高出上百倍。
可以借图书馆找书来比喻:仅在馆内乱走(对应三维扩散)很难直接找到目标;先定位到对应书架(一维滑动),再逐一攻克,很快锁定目标。这种聪明的搜索方式展现了生物分子的高效与“智慧”。
研究表明,以大肠杆菌的乳糖阻遏蛋白(Lac抑制子)为例,它可以在约3秒内定位到约400万个碱基对中的特定位点。这一速度比理论上仅依靠三维扩散碰撞预测的快了两到三个数量级——也就是说能在“秒”级完成关键生命过程,而不是“小时”级。
事实上,这种复合搜索模式受到物理、生化领域广泛关注。现代单分子成像等技术还原了蛋白沿DNA“滑动”、“跳跃”甚至“螃蟹步”般的复杂行为,进一步助力理论和实验的统一。
分子马达
扩散虽然普遍,但在很多情境下无法满足细胞长距离、大分子、高速运输的需要。此时,主动运输机制便起了主导作用。例如驱动蛋白、胞动蛋白等分子马达通过“步行”方式运输细胞器、囊泡及大分子。
驱动蛋白的例子是沿细胞骨架中的微管方向运动,过程模拟如下:
驱动蛋白每个步长约8纳米,正好对应微管蛋白二聚体的间距。这种精确的步长匹配体现了进化的精妙设计。
在神经元中,这种机制尤其突出。神经元的轴突长度可达1米甚至更长,如果仅通过自由扩散,囊泡或神经递质就算运动一整年也难以到达末端;通过驱动蛋白沿微管主动运输,则只需几小时到几天。这对神经信号的高效传递和物质周转提供了物理保障。
此外,细胞也能巧妙地调控分子马达与扩散的配合。在细胞某些区域,仍有部分分子通过扩散“最后一公里”到达目标地,这种灵活的协作是生物系统高效、灵活响应环境变化的重要基础。
通过上述扩散定律和分子运输机制的理解,我们能够深入认识生物体系自下而上的物理本质。这既有助于科学研究,也直接指导医学、工程等领域中的实际应用。
测定扩散参数
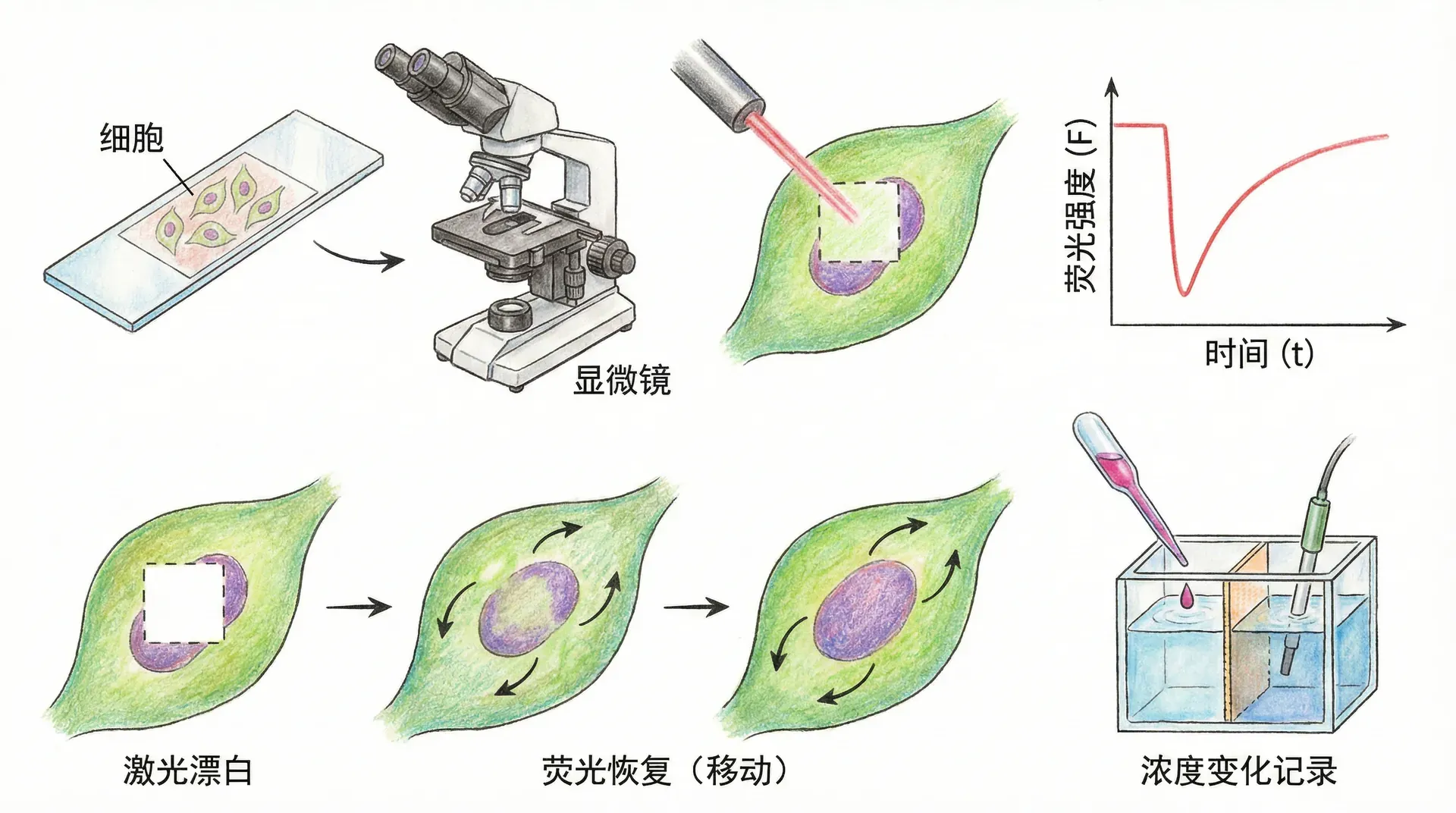
生物分子的扩散系数等动力特性的测定,常见方法包括荧光恢复(FRAP)、单分子追踪(SPT)以及电泳与离心技术,每种各具特色且常结合使用。
FRAP技术(荧光恢复):利用强激光将细胞内某一区域荧光分子漂白后,观测未漂白分子扩散进入“漂白区”时荧光信号的恢复情况。对恢复曲线进行数学建模和拟合,即可得出分子的扩散系数、迁移率,甚至分子的结合-解离参数。FRAP尤其适合于活细胞内蛋白质在细胞膜及胞质中的扩散动态测量,也可用于转录因子的交换与亚区扩散异质性的探究(如多区域FRAP、聚焦漂白等变体)。
单分子追踪技术(SPT) 则通过单分子荧光标记和高分辨率显微成像,实时追踪单个分子的运动轨迹,揭示其扩散、受限或定向运动特点。通过统计大量粒子的运动路径,并运用均方位移(MSD)分析,可区分不同运动模式并定量扩散参数。SPT可揭示细胞膜中蛋白运动的复杂性(如膜骨架“围栏”效应、纳米岛等),还可用于胞内大分子的路径追踪及受体-配体动力学测量。
电泳与离心则多用于大规模分子分离和分析。电泳利用带电分子(如蛋白、DNA、RNA)在电场中的迁移速度差异实现分离,常见有SDS-PAGE(按蛋白质分子量)、琼脂糖凝胶(按核酸片段大小)、等电点聚焦(按等电点)等;离心技术依赖颗粒在离心力下的沉降速度差异,既可高效分离亚细胞组分,也可用于测定分子量及分级,通过梯度离心甚至可实现高分辨率分离。沉降速度与颗粒密度、半径平方成正比,与介质粘度成反比,可用斯托克斯定律进行描述。
采用这些技术进行扩散与运动测量时,实验环境(如温度、pH、盐浓度、粘度等)变化可显著影响结果。科学的实验设计和对照是保证数据准确的前提。
总结
扩散与运输现象是生命活动不可或缺的物理基础,从纳米级的分子随机游走,到细胞内外大分子的定向运输,再到更高层次的物质分布,保障了生命系统的稳态与高效。虽然单个分子的运动充满随机性,难以预测,但大量分子集体运动却呈现高度可重复、可用物理定律(如Fick定律、Einstein扩散公式等)描述的统计规律。科学家据此能够定量模拟细胞内物质流动、反应速率,以及疾病发展等复杂过程。
扩散理论的应用极为广泛,不仅帮助我们理解生命机制,还为药物开发、治疗方案设计、诊断技术和生物工程等实际领域提供了重要指导。例如,通过调控扩散过程提升药物递送效率,突破生理屏障,或基于分子扩散开发高灵敏度生物传感器等。
因此,扩散和运输过程体现了生命体系“有序中的无序”这一独特本质。真正掌握这些原理,不仅有助于揭示生命奥秘,更是推动科学与医学进步的基石。