神经系统疾病
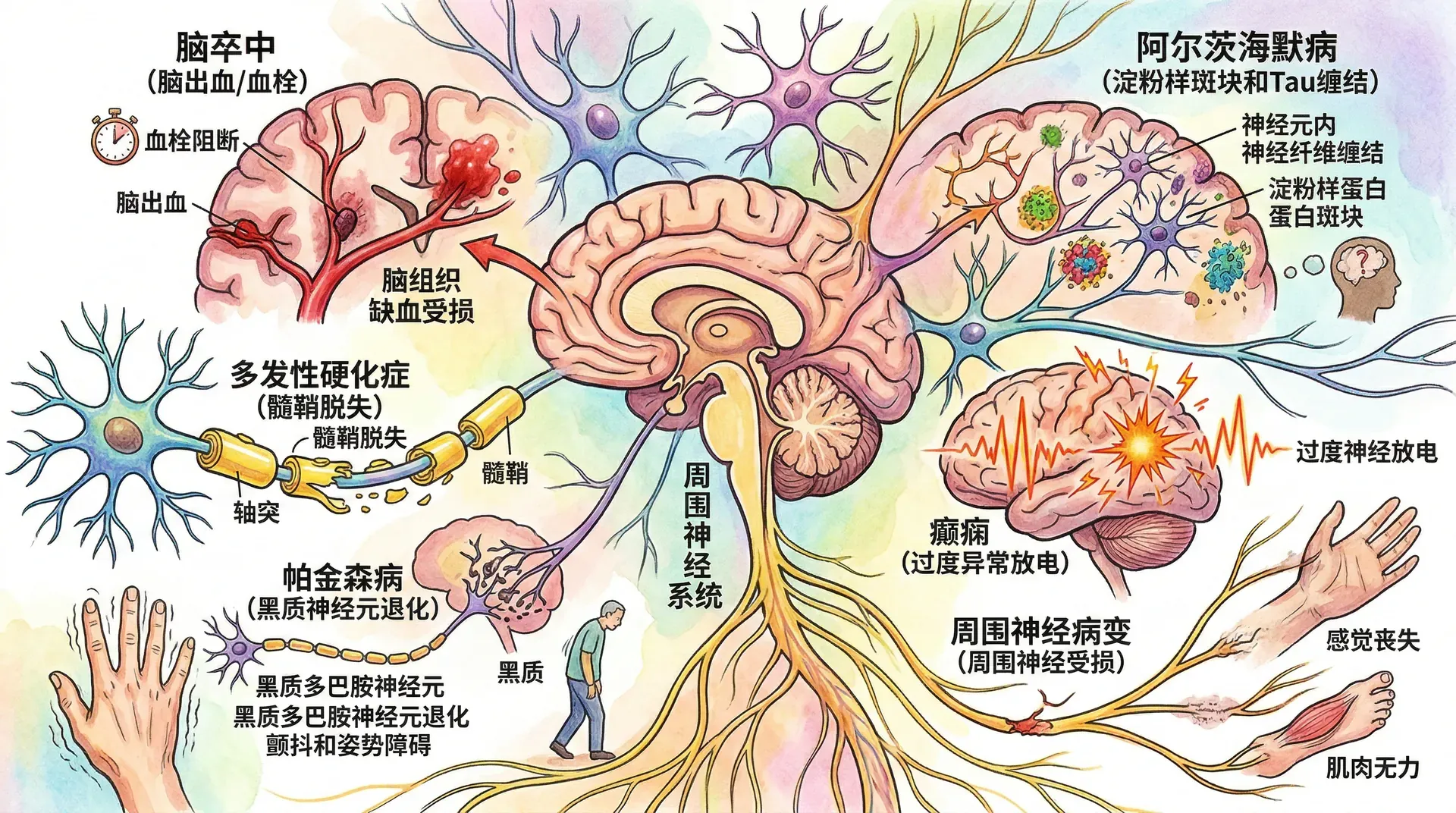
神经系统是人体最精密、最复杂的系统,它控制着我们的思维、情感、运动和感知。然而,这个精密系统也面临着各种疾病的威胁。从影响老年人的阿尔茨海默病,到困扰儿童的自闭症,再到突发的脑损伤,神经系统疾病已成为全球重大的公共卫生问题。根据中国疾病预防控制中心的统计数据,我国约有超过1000万阿尔茨海默病患者,300万帕金森病患者,神经系统疾病的防治已成为国家医疗卫生事业的重点领域。
理解神经系统疾病的发病机制,不仅有助于我们认识大脑的正常功能,更能为疾病的预防和治疗提供科学依据。本章将系统介绍神经系统疾病的分类、主要疾病的病理机制、临床表现,以及目前的研究进展和治疗策略。我们将特别关注中国在神经科学研究领域的贡献,探讨如何将基础研究转化为临床应用。
神经系统疾病的分类与病理特征
疾病分类的基本框架
神经系统疾病种类众多,通常可从下述角度进行分类:
其中,神经发育障碍主要发生于儿童期,常见包括智力发育障碍、自闭症谱系障碍(ASD)、注意缺陷多动障碍(ADHD)等。这类疾病多源于大脑发育过程中的异常,如神经元迁移障碍、突触形成失调或神经回路构建错误。自闭症患者,常见大脑发育早期过度生长,神经连接模式异常。
神经退行性疾病常影响中老年人。典型如阿尔茨海默病(AD)损失海马和大脑皮层神经元,导致记忆、认知障碍;帕金森病(PD)受累黑质多巴胺能神经元,致运动障碍。此类疾病多缓慢进展,早期隐匿,诊断有一定挑战。
神经退行性疾病指神经元或其髓鞘逐渐损失的疾病。这类疾病多起病隐匿、进行性加重,难以逆转,目前仅能对症治疗和延缓进展。
神经系统疾病的共同病理机制
虽然神经系统疾病各异,但很多疾病在分子与细胞水平上存在共性机制,包括蛋白质错误折叠与聚集、氧化应激、线粒体功能障碍和慢性神经炎症。
常见病理机制举例如下:
蛋白质聚集与“朊病毒样传播”
以阿尔茨海默病为例,Aβ聚集形成斑块,tau蛋白异常聚集形成神经纤维缠结。帕金森病中,α-突触核蛋白在神经元内异常折叠聚集成路易小体。近年来研究发现,这些异常蛋白可在神经元间“传递”,类似朊病毒感染过程,推动疾病在神经系统内扩展。
氧化应激与线粒体障碍
大脑仅占体重2%,却消耗约20%氧气,因而极易产生活性氧。神经元富含不饱和脂肪酸,极易被氧化。疾病状态下,氧的代谢产物(ROS)增多且清除功能下降,结合线粒体障碍,协同加剧神经损伤。
神经炎症的“双刃剑”效应
小胶质细胞为CNS的主要免疫细胞,监测并清除碎片、异常蛋白、分泌生长和免疫介质。在慢性病理条件下,如AD和MS,小胶质细胞持续激活,释放大量促炎因子(如TNF-α、IL-1β),反致神经元损害,加重疾病进展。
主要神经系统疾病的病理对照
下方归纳了部分重要疾病的主要病理特征:
阿尔茨海默病与帕金森病
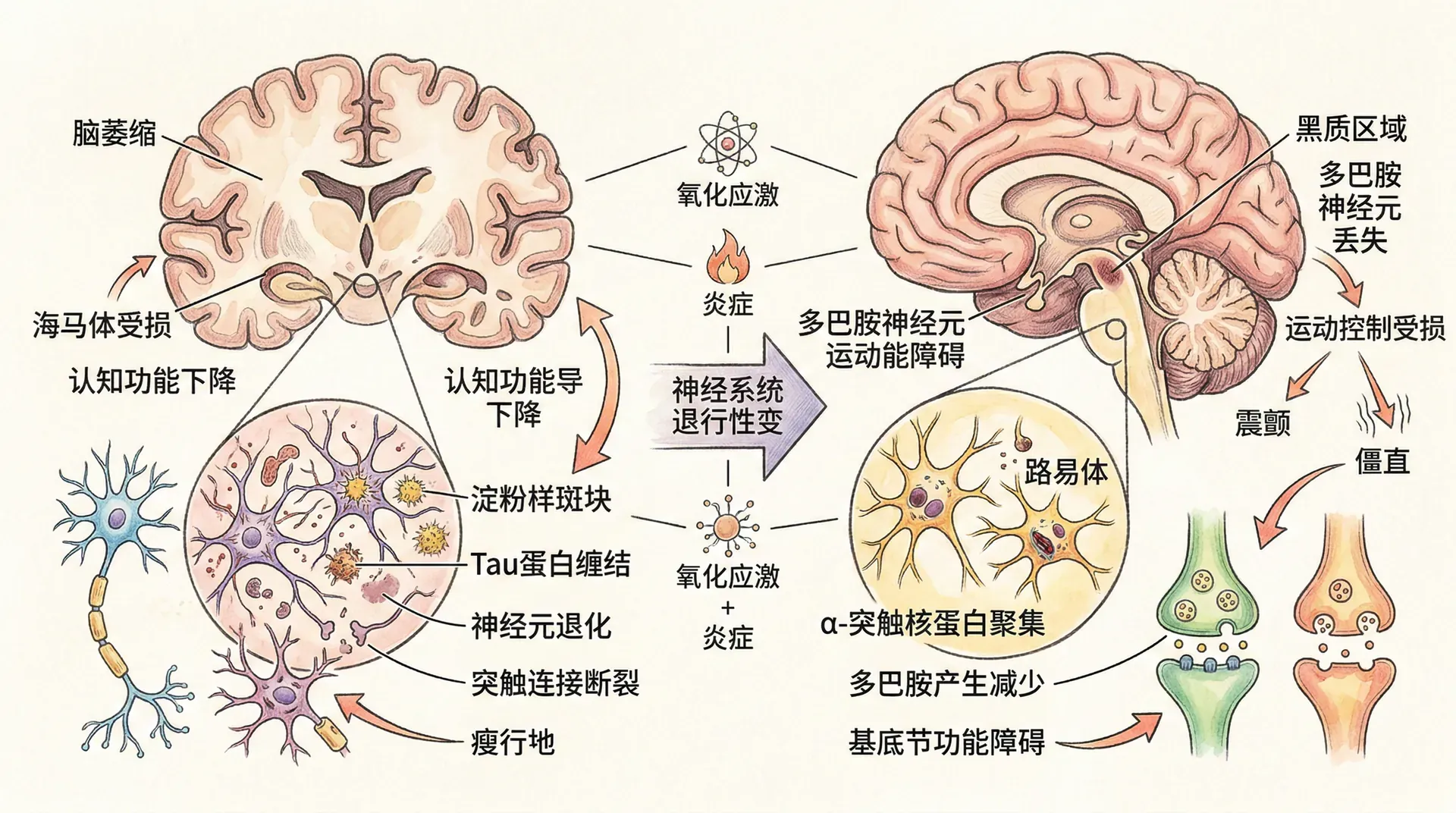
阿尔茨海默病的病理与临床表现
阿尔茨海默病(Alzheimer's disease, AD)是最常见的神经退行性疾病,约占所有痴呆的六至八成。自1906年首次报告以来,随着中国老龄化进程加速,患病人数急剧上升,2023年逾千万,2050年或将达2800万。
阿尔茨海默病核心病理如下:
阿尔茨海默病的核心病理包括淀粉样斑块和神经纤维缠结。斑块的形成是由于淀粉样前体蛋白(APP)在β和γ分泌酶异常切割下生成Aβ,Aβ的初期寡聚体形式具有明显的神经毒性,可干扰神经元间的突触功能。
与此同时,tau蛋白在疾病进展中出现过度磷酸化,导致其失去与微管的结合能力,最终在神经元胞内聚集成缠结,这种缠结妨碍了轴突内的物质运输。值得注意的是,tau蛋白的病理变化与认知障碍的严重程度相关性更高,其在大脑内的扩散轨迹也与临床症状的进展密切吻合。
临床表现:
- 早期:近期记忆力显著下降,常常忘事、丢三落四。
- 进展期:认知障碍加重、表现为表达障碍、判断力下降,伴精神行为异常(如妄想、易怒、焦虑)。
- 晚期:严重生活不能,完全丧失认知与自理能力。
阿尔茨海默病年龄相关患病率如下图:
图中可见,患病率随年龄快速上升,65岁起每增5岁风险几乎翻倍,此规律在全球范围,以及中国人群均一致。
当前机制观点多倾向于“淀粉样蛋白级联假说”:Aβ聚集诱发整个病理级联,包括tau异常、突触障碍、神经炎症、氧化应激等。但Aβ为靶点的药物多告失败,提示机制远比预想复杂。
帕金森病的发病机制与症状
帕金森病(Parkinson's disease, PD)仅次于阿尔茨海默病的另一常见神经退行性疾病,突出表现为运动障碍。其主因是中脑黑质致密部多巴胺能神经元进行性减少。
运动神经回路涉及以下重要环节:
α-突触核蛋白正常为可溶蛋白,病理时折叠聚集,形成路易小体。近年来证据发现,该蛋白有细胞间扩散的“朊病毒样”特性,为疾病扩展的新解释。
临床症状归纳如下:
- 运动“四主征”:静止性震颤(手脚不自主抖动,休息时明显)、肌强直(肢体被动移动有“铅管感”)、运动迟缓(动作减速、幅度变小、表情呆板,称“面具脸”)、姿势不稳(身体前倾、小步走路)。
- 典型运动表现“两例”:
- 患者起步困难,走路小碎步,步态拖曳(“慌张步态”)。
- 静止时手指搓丸样颤抖,活动时缓解。
帕金森病不仅有典型的运动症状,还常常伴随多种非运动症状,如嗅觉减退、便秘、抑郁、失眠及认知功能的改变等。有些非运动症状甚至在经典的运动症状出现多年之前就已显现,其中快速眼动睡眠行为障碍(RBD)是一项重要的早期预警信号。研究发现,大多数出现RBD的患者最终会发展为帕金森病或其他类似的神经退行性疾病,因此对此类症状的早期识别对于疾病的预警和干预具有重要意义。
帕金森病多巴胺能神经元丧失如下:
如图,临床出现运动症状时,多巴胺能神经元多已损失八成以上。因此早期诊断、推迟发病进展尤为重要。
两种疾病的治疗策略
阿尔茨海默病和帕金森病目前均无法实现根治,治疗主要目标是延缓进展与改善症状,药物和非药物疗法结合。
部分经典药物治疗方式对比如下:
左旋多巴为帕金森病“金标准”,但无法阻止病情进展,长期易出现剂量波动和异动症。临床需“剂量滴定+多模式治疗”,结合康复训练、心理支持等。
除药物治疗外,非药物疗法同样在疾病管理中具有重要作用。对于阿尔茨海默病患者,建议定期进行认知训练,同时多参加社交活动和各种智力活动,如拼图、下棋,有助于延缓功能的减退。帕金森病患者则推荐规律的有氧运动(如太极拳、舞蹈),配合语言和吞咽能力的训练,以提升和维持日常生活能力。此外,针灸、按摩等传统医学方法在部分患者中也能带来一定的改善效果。
神经发育障碍与自闭症谱系障碍
神经发育障碍的基本概念
神经发育障碍是一组起病于儿童发育早期、主要表现为大脑发育和功能异常的疾病。这类障碍涉及认知、语言、社交、运动等多个方面,常见类型包括:
神经发育障碍的病因复杂,涉及遗传和环境因素。大脑发育过程极为精细,从胚胎期的神经管形成,到神经元增殖、迁移、分化和突触修剪,每一个环节若出现异常,都可能导致各类神经发育障碍。例如,神经元迁移问题可引起皮层结构异常(如灰质异位),突触形成/修剪失衡则与自闭症有关。
遗传因素:
大量研究显示,多基因异常或罕见基因突变均可导致发育障碍。典型单基因病例如下:
事实上,大多数神经发育障碍的发生离不开遗传与环境等多种因素的复杂交互。环境因素方面,常见的包括孕期感染、营养不良、接触酒精或铅等有毒物质、早产以及缺氧等。
近年来,孕期免疫激活(MIA)这一机制受到高度关注。研究发现,母体在孕期发生感染或炎症反应可能通过胎盘影响胎儿大脑发育。动物模型进一步证实,MIA可导致后代出现自闭症样行为,这为环境因素在神经发育障碍中的作用提供了重要证据。
自闭症谱系障碍的核心特征
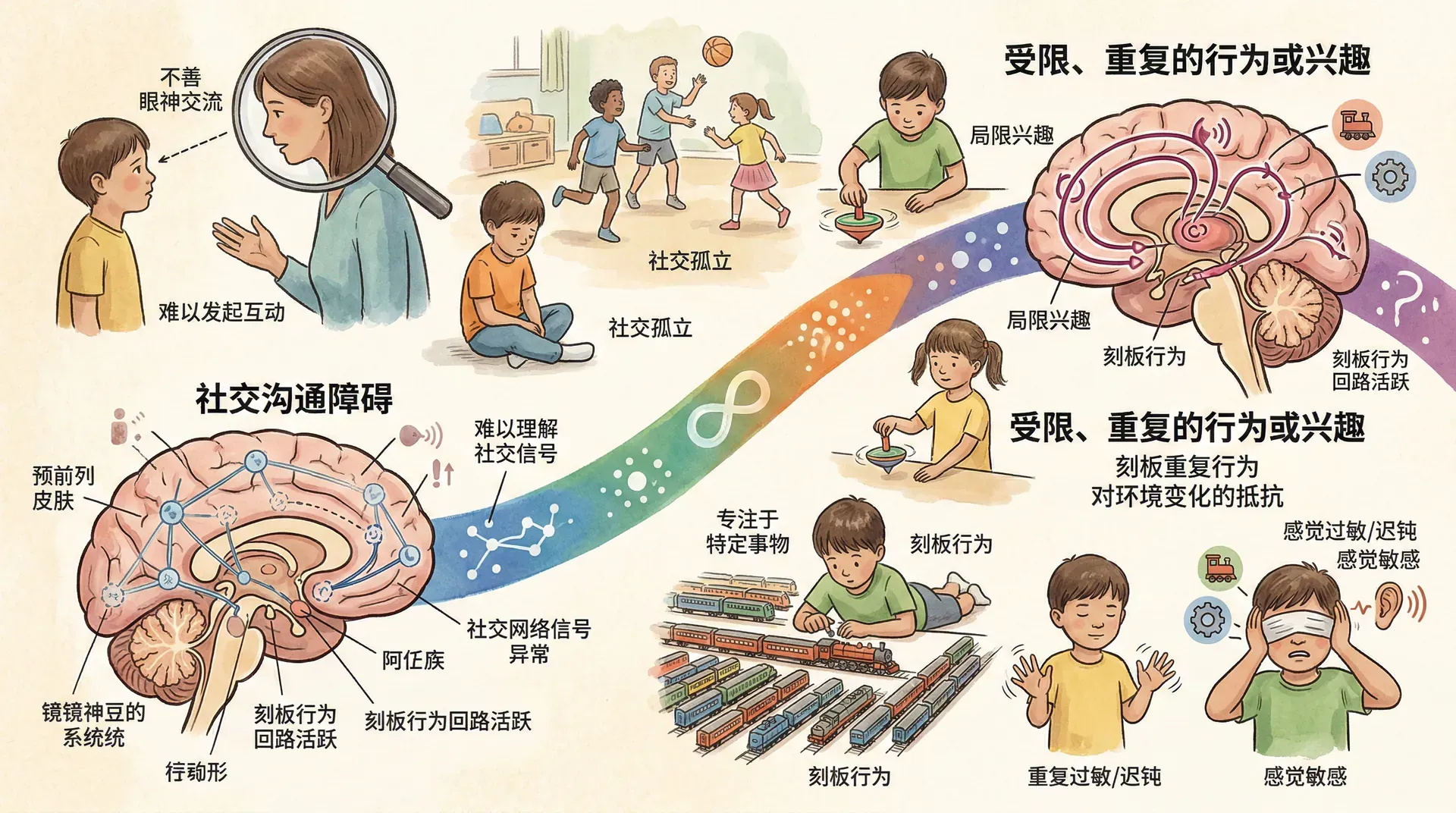
自闭症谱系障碍(ASD)以社交沟通障碍和刻板重复行为为两大核心特征。"谱系"表示症状严重程度极具异质性:既有重度、需大量支持的个体,也有高功能、社交能力部分保留者。
例如:患儿若日常安排被改变,常出现剧烈情绪反应。这些行为有时是对焦虑/不确定性的应对机制。
神经机制如下:
这些发现支持“突触病”假说: ASD是突触连接异常导致的脑网络失调。
上图比较了社交沟通等能力的发育轨迹。可以看到自闭症患儿逐渐与正常儿童分离,发育滞后逐年加重,说明早期识别、干预十分关键。
自闭症的早期识别与干预
2-3岁前密集干预效果最佳,因此早期筛查极为重要。常用早期预警信号如下:
临床筛查工具有CDCC量表、孤独症行为量表(ABC)、ADOS和ADI-R等。一旦高风险,即应转诊专业评估。
主要干预方式:
- 行为干预:以应用行为分析(ABA)为核心,通过行为分解与正向强化提升沟通、社交、自理等能力。
- 发展性干预:如早期丹佛模式(ESDM)、关键反应训练(PRT)、社交技能/语言治疗等,注重自然情境中训练。
- 融合教育:普通学校支持下,促进包容与互动。
- 家庭参与:家长是最重要的“训练师”,日常生活中应贯彻干预原则。
中国如“星星雨”、“以琳”等公益组织为家庭提供课程和持续支持,减轻照护压力。融合教育进入越来越多主流校园,不但帮助特殊儿童成长,也提升全社会的包容度和科学素养。
脑损伤与神经修复
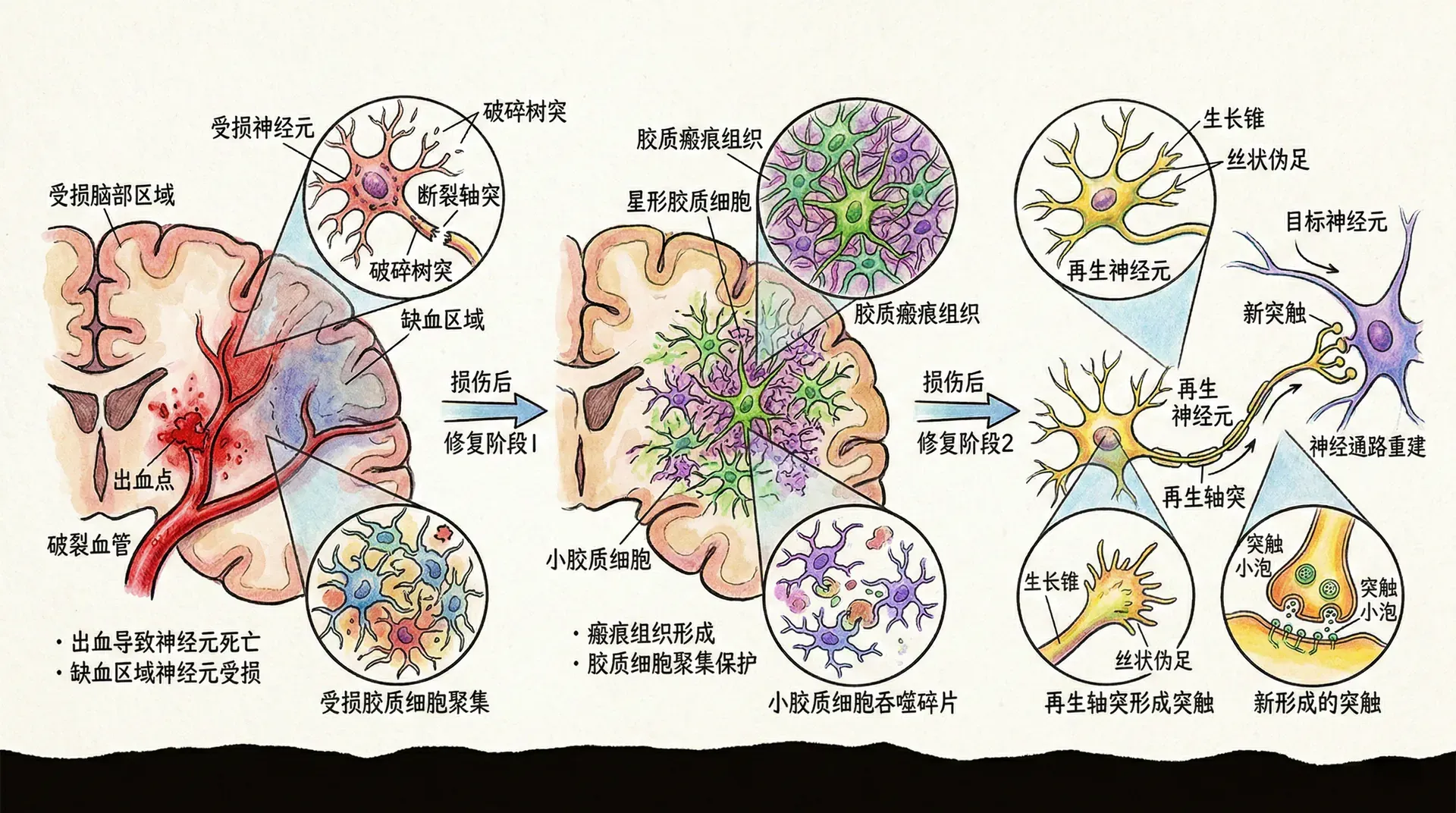
脑损伤的类型与机制
脑损伤(Brain Injury)包括外伤性(TBI)和非外伤性两大类。TBI常见原因为车祸、跌倒、暴力、运动损伤,是青壮年致残和死亡主因。非外伤性如中风、缺氧、感染、中毒等。
脑损伤分为原发性(外力直接导致)与继发性(脑水肿、缺血、炎症、兴奋性毒性等次生反应)。继发性损伤是临床干预重点。
“兴奋性毒性”即脑损伤或卒中后谷氨酸过度激活,钙进入神经元,激活蛋白酶、氧化酶,加速细胞死亡。炎症反应亦既有修复又可能加重二次损伤,在临床上成为药物干预新靶点。
神经可塑性与功能恢复
大脑损伤后具有一定自我恢复能力,称为神经可塑性(Neuroplasticity):
- 结构可塑性:树突增生、新突触、轴突重建、部分脑区新生神经元(如海马)。
- 功能可塑性:脑网络重组,健侧半球或损伤周边区代偿功能。
恢复过程分期:
如图,积极康复训练(尤其早期大量介入)大大提升了功能恢复,且损伤越轻、恢复越快。即使中度损伤,长期不进行康复也会错失最佳恢复期。
康复治疗与再生医学
脑损伤康复需多学科协同。常见康复手段包括:
- 物理治疗:运动训练、肢体被动/主动锻炼、平衡/步态训练,防止萎缩、促进动作功能恢复。
- 作业治疗:着重日常自理训练(进食、如厕、穿衣等)。
- 语言治疗:改善失语、发音、理解能力。
- 认知训练:针对记忆、注意力、执行功能障碍。
- 心理支持:减轻焦虑、抑郁等并发问题。
中国传统医学(针灸、推拿、中药等)也被广泛应用。临床试验证明,针灸可促进运动和认知恢复,其机制可能包括调控神经营养因子、改善脑血流等。2010年《NEJM》一项中国多中心研究显示,针灸+标准康复联合优于单纯康复训练,这一证据促进了针灸康复国际认可。
再生医学与干细胞治疗:干细胞移植为脑损伤修复带来希望。通过分化补充神经元/胶质细胞、分泌营养因子、调节炎症等机制,有望促进组织再生。中国在神经干细胞、间充质干细胞等临床研究方面进展迅速,但疗效和大规模应用还需较多数据积累与安全性验证。
脑损伤康复“黄金时间窗”在伤后三至六个月,此期神经可塑性最活跃。康复是长期过程,慢性期持续训练同样有效。只要坚持不懈,就有希望取得进步。
中国神经科学研究的临床应用
中国神经科学发展起步较晚,但近年来进步迅速。自20世纪80年代改革开放以来,随着1988年中国神经科学学会的成立及“973”“863”等国家重大科研计划,以及“脑科学与类脑研究”等项目的推进,大量投入推动了神经科学基础与应用研究的飞跃。中国学者在阿尔茨海默病相关蛋白结构解析(施一公团队)、自闭症猕猴模型与致病基因研究(张永清团队)、干细胞修复脊髓损伤(苏国辉团队)、帕金森病神经元再生(戴建武团队)、针灸机制现代化(刘存志团队)、脑机接口助力高位截瘫患者(郑筱祥团队)等领域取得国际瞩目成果,推动了基础成果向临床转化。
基础研究的突破也带动了诸多临床创新。例如阿尔茨海默病早期诊断方面,北京师范大学开发的成像标志物和神经心理评估可早期识别高风险人群,上海瑞金医院的PET-CT分子影像用于疾病早筛和干预。帕金森病治疗方面,脑深部电刺激(DBS)等高水平手术广泛开展,部分中心还探索DBS与干细胞移植的联合治疗,中山大学自研“智能DBS”能根据脑电实现精准刺激。脑卒中方面,中国通过“卒中中心”网络大幅提升急救和干预效率,多项研究(如CHANCE研究)改变了国际诊疗实践,针灸康复也获WHO推荐。
随着老龄化加剧,疾病预防、早筛和慢病管理成为神经科学公共卫生的前沿。阿尔茨海默病尚无特效预防药物,但“Lancet委员会”提出通过教育、控血压、控糖脂、避免吸烟酗酒、增加运动和社交等干预,可预防/延缓40%病例。中国在社区开展“脑健康促进计划”,普及风险评估与健康指导。
帕金森病的防控同样依赖健康生活方式(如有氧运动、地中海饮食),也在推进高危人群监测、早期干预。卒中防治体系侧重“三高”管理、急救能力下沉以及心房颤动等危险因素识别干预。儿童神经发育障碍的预防聚焦孕产期保健、疾病早筛、早干预,全流程的“自闭症筛查-干预-康复”模式逐步推广。
预防神经系统疾病的“五大基石”:健康饮食、规律运动、充足睡眠、认知训练、社交活动。不仅有助于远离疾病,还关系到健康老龄化与生活质量提升。“预防胜于治疗”在神经领域尤为关键。
总结
神经系统疾病涵盖范围极广,从儿童期常见的神经发育障碍(如自闭症谱系障碍、注意缺陷多动障碍、智力低下等),到中青年时期的遗传性及炎症性疾病(如肌萎缩侧索硬化、多发性硬化、癫痫等),再到老年期的神经退行性疾病(如阿尔茨海默病、帕金森病、脑卒中后遗症等)。虽然这些疾病在病因、年龄层和临床表现上各有差异,但研究发现许多神经疾病在分子和细胞层面上存在共同的病理机制,如蛋白质错误折叠、异常氧化应激、线粒体功能障碍、神经炎症、细胞凋亡/自噬,以及神经元信息传递障碍等。
不论是因老龄化加剧的神经退行性疾病(如阿尔茨海默病、帕金森病),还是影响儿童正常成长和社会适应能力的发育障碍(如自闭症、脑瘫),都已成为家庭与社会高度关注的健康问题。此外,脑卒中及脑外伤等损伤后的功能障碍通过对神经可塑性和修复机制的研究,为康复带来希望;而基因检测和编辑等新技术也为遗传性疾病的诊治提供了新方向。
因此,深入理解这些常见疾病的发生发展机制,推动早期诊断与筛查并对高危人群进行及时干预,同时加强健康教育、生活方式改善与慢病管理,是神经科学研究和临床实践的核心目标。近年来,中国在基础与应用脑科学、疾病机制解析、诊断创新和新疗法转化等方面取得显著进步,相关团队在阿尔茨海默病蛋白结构解析、帕金森病干细胞治疗、自闭症基因与动物模型、卒中急救体系建设等领域取得了一系列国际认可成果。这些进展不仅推动了理论创新,也为临床疾病防治提供了科学依据和“中国方案”,中国的经验和智慧正在为全球神经科学领域提供重要借鉴。
本节练习
1. 阿尔茨海默病最主要的病理特征是什么?
A. 黑质多巴胺神经元丧失
B. β-淀粉样蛋白斑块和神经纤维缠结
C. 脱髓鞘斑块
D. 路易小体
答案:B
解析:阿尔茨海默病的两大病理标志是细胞外的β-淀粉样蛋白斑块和细胞内由过度磷酸化tau蛋白形成的神经纤维缠结。黑质多巴胺神经元丧失是帕金森病的特征(A),脱髓鞘斑块见于多发性硬化症(C),路易小体是帕金森病的病理标志(D)。理解不同神经退行性疾病的特异性病理改变有助于疾病诊断和机制研究。
2. 帕金森病患者出现运动症状时,黑质多巴胺能神经元的丧失比例约为多少?
A. 20-30%
B. 30-40%
C. 50%以上
D. 80-90%
答案:C
解析:帕金森病在临床前期已经悄然进展多年,当黑质多巴胺能神经元丧失达到50%以上,纹状体多巴胺水平下降80%以上时,运动症状才会显现。这说明大脑具有强大的代偿能力,也提示在症状出现前已经有漫长的疾病进程,为早期诊断和干预提供了时间窗口,但也增加了早期发现的难度。
3. 自闭症谱系障碍的核心症状不包括以下哪一项?
A. 社交沟通障碍
B. 刻板重复行为
C. 运动迟缓
D. 感觉异常
答案:C
解析:自闭症谱系障碍的核心症状包括社交沟通障碍(A)和刻板重复行为(B),感觉异常(如对声音、触觉过度敏感)属于刻板重复行为的范畴(D)。运动迟缓是帕金森病的核心症状之一(C),不属于自闭症的诊断标准。区分不同神经发育障碍和神经退行性疾病的特征性症状对于临床诊断至关重要。
4. 脑损伤后功能恢复的“黄金时间窗”是指伤后多长时间?
A. 1-2周
B. 2-4周
C. 3-6个月
D. 1-2年
答案:C
解析:脑损伤后的“黄金时间窗”是伤后3-6个月,此期神经可塑性最活跃,大脑重组、突触重建最为活跃,康复训练效果最好。但这并不意味着过了这个时期就不需要康复,持续的康复训练在慢性期仍可获得功能改善。早期、密集、持续的康复训练是促进功能恢复的关键。
5. 张先生,68岁,近半年来家人发现他记忆力明显下降,经常找不到钥匙、眼镜等物品,出门后找不到回家的路,性格也变得多疑、易怒。请分析张先生可能患有什么疾病?该疾病的发病机制是什么?目前有哪些治疗方法?作为家属应如何照护?
答案:
张先生的临床表现高度提示阿尔茨海默病(AD)。进行性记忆力下降(近期记忆受损突出)、定向力障碍(找不到回家的路)、性格改变(多疑、易怒)都是该病的典型症状。确诊需要进行神经心理测评、脑影像检查(MRI显示海马萎缩)、必要时进行PET-CT检测脑内β-淀粉样蛋白沉积。
发病机制:阿尔茨海默病的核心病理是β-淀粉样蛋白(Aβ)和tau蛋白的异常聚集。Aβ在细胞外聚集形成老年斑,干扰突触功能;tau蛋白过度磷酸化后在细胞内聚集形成神经纤维缠结,破坏神经元骨架,导致神经元死亡和脑萎缩。此外,神经炎症、氧化应激、线粒体功能障碍等也参与疾病进程。
治疗方法:目前尚无根治方法,治疗以对症和延缓进展为主。药物治疗包括胆碱酯酶抑制剂(多奈哌齐、卡巴拉汀等)和NMDA受体拮抗剂(美金刚),可改善认知功能,延缓疾病进展。非药物治疗包括认知训练、社交活动、音乐疗法、运动等,对维持认知功能有益。2023年批准的lecanemab是首个可减少脑内Aβ沉积并延缓认知下降的单克隆抗体药物。
家属照护:建立规律的生活作息,避免环境变化引起混乱;使用记忆辅助工具,如便签、日历提醒;确保家居安全,防止走失(可佩戴定位设备);耐心沟通,避免争论和批评;鼓励参与力所能及的活动,维持社交;照顾者也要关注自己的身心健康,必要时寻求支持小组或专业帮助。
6. 为什么说神经退行性疾病是“蛋白质错误折叠病”?请结合阿尔茨海默病和帕金森病的病理机制说明。
答案:
神经退行性疾病被称为“蛋白质错误折叠病”,是因为这类疾病的核心病理特征是特定蛋白质的错误折叠和聚集,形成有毒的寡聚体或纤维,损害神经元功能,最终导致神经元死亡。
在阿尔茨海默病中,β-淀粉样蛋白(Aβ)和tau蛋白是主要的异常聚集蛋白。Aβ是由淀粉样前体蛋白经异常剪切产生的多肽,正常情况下应被降解清除,但在病理状态下过度产生或清除不足,导致其错误折叠并聚集成寡聚体和纤维,沉积在神经元周围形成老年斑。tau蛋白正常时与微管结合维持细胞骨架,但异常磷酸化后错误折叠,脱离微管并聚集成成对螺旋丝,在细胞内形成神经纤维缠结。
在帕金森病中,α-突触核蛋白是关键的异常聚集蛋白。它正常时是可溶性蛋白,参与突触囊泡功能,但在病理状态下错误折叠并聚集,形成不溶性的纤维状结构,在细胞内沉积形成路易小体。更重要的是,错误折叠的α-突触核蛋白具有“朊病毒样”特性,可以在神经元之间传播,诱导正常蛋白错误折叠,导致病理扩散。
这些蛋白聚集体不仅占据细胞空间,更重要的是具有细胞毒性,干扰多种细胞功能,包括线粒体功能、蛋白质降解系统(蛋白酶体和自噬)、突触传递、轴突运输等,激活氧化应激和炎症反应,最终导致神经元死亡。理解蛋白质错误折叠和聚集的机制,为开发靶向治疗策略(如促进蛋白质清除、抑制聚集、阻断传播)提供了理论依据。