系统生物学的理论与方法
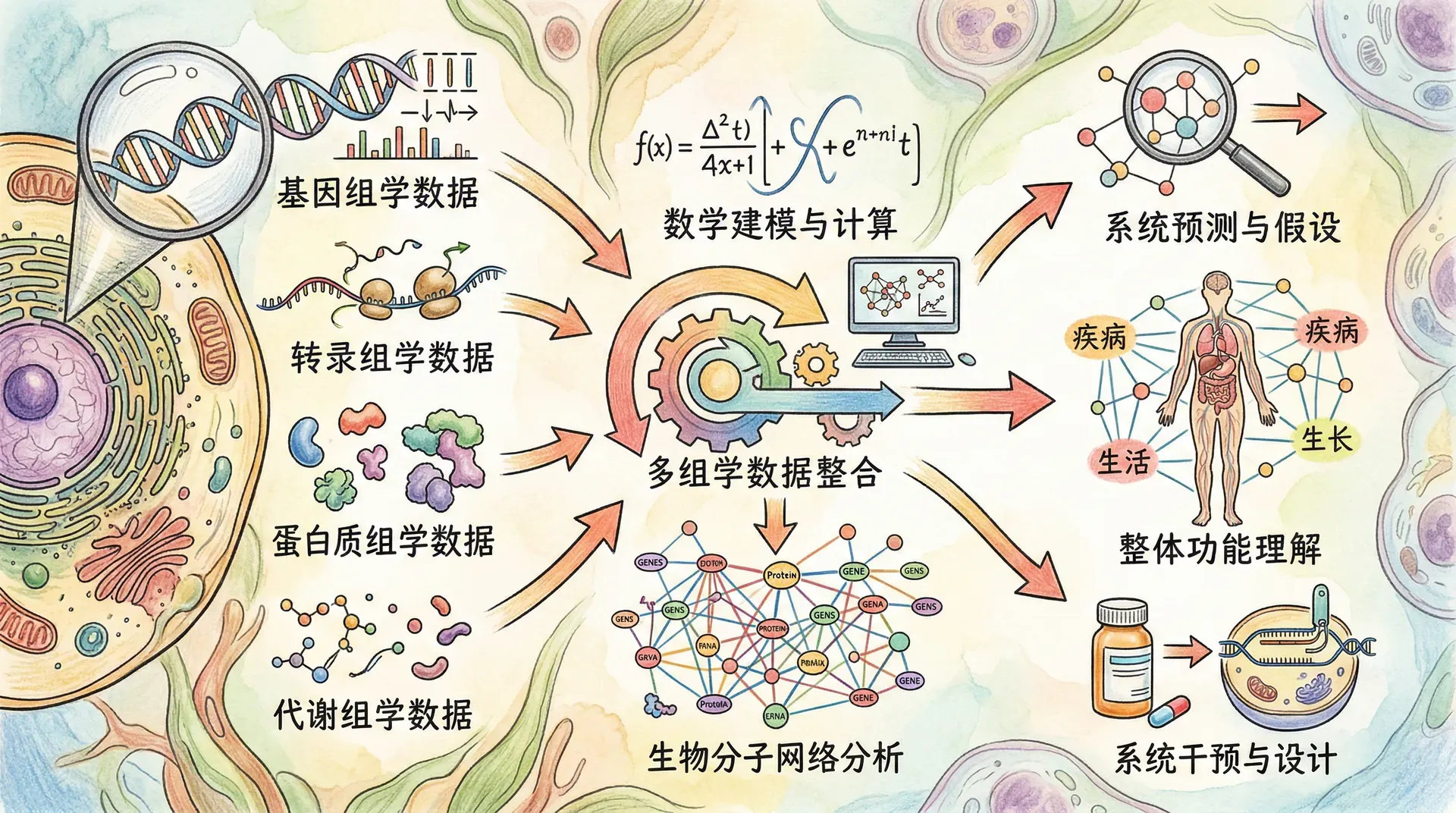
系统生物学代表了生命科学研究范式的重要转变。随着高通量组学技术(如基因组、转录组、蛋白质组和代谢组等分析方法)的迅速发展,科学家能够获取海量、系统层次的生物大数据,这为整体性、动态性的研究提供了坚实的基础。传统生物学更侧重于“还原论”——分析单一分子、蛋白质或基因等组分,试图拆解生命现象,但这种方法难以解释复杂的生物过程,因为许多重要的生理与疾病机制涉及多个组分、多层级之间的动态调控和网络联系。
系统生物学则倡导“整体论”视角,注重生物体系内部各组分的相互作用,通过整合不同层次的数据(如基因组、转录组、蛋白质组、代谢组),分析网络结构和功能模块,揭示如涌现性、鲁棒性和自组织能力等全局特性。在疾病机制分析中,系统生物学不仅考察致病基因本身,也重视其在多分子调控网络中的地位和对系统稳定性的影响。
整体上,科学家逐步认识到,诸如心脏跳动、神经网络信号传递、细胞周期调控等复杂生命活动,只有通过分子和细胞多层次协作才能实现。单个蛋白或基因往往难以揭示整体生物系统的行为。系统生物学正是通过数学建模、网络分析、计算模拟等手段,从更高视角把握生命过程的综合特性,实现对生命现象和疾病机制的全面、定量和动态理解。这不仅推动了基础生命科学发展,也为精准医学、疾病防治与新药研发带来了新理论和新方法。
系统生物学的概念与研究范式
系统生物学是一门整合多学科知识的交叉学科,它将生物学、数学、物理学、计算机科学等领域的理论和方法有机结合,旨在从系统层面理解生命活动的规律。这一学科的兴起与人类基因组计划的完成密切相关。当科学家们获得了完整的基因组序列后,逐渐意识到仅仅知道基因的序列信息是不够的,还需要理解这些基因如何协同工作,形成复杂的生命系统。
中国科学院系统生物学研究中心在2005年成立后,积极推动了系统生物学在国内的发展。研究团队通过整合基因组学、蛋白质组学和代谢组学数据,构建了多个重要生物过程的系统模型。例如,北京大学的研究团队利用系统生物学方法研究了水稻的生长发育过程,发现了多个关键调控网络,为培育高产优质的水稻品种提供了理论基础。
系统生物学的研究范式可以概括为“测量-整合-建模-预测-验证”的循环过程。
系统生物学的核心思想是将生物体视为一个复杂的动态系统,强调整体性、动态性和定量性,通过数学建模和计算模拟来理解生命活动的规律。
生物系统的复杂性与涌现特性
生物系统的复杂性源于其组成成分的多样性以及这些成分之间错综复杂的相互作用。一个细胞包含数千种不同的蛋白质、核酸、脂质和小分子代谢物,它们通过各种生化反应和信号传递途径相互联系,形成了一个高度有序而又动态变化的网络。这种复杂性使得生物系统表现出许多独特的性质,其中最重要的就是涌现特性。
涌现特性是指系统整体表现出的、单个组分所不具备的性质。就像水分子本身并没有“湿润”的特性,但大量水分子聚集在一起就会产生湿润的性质。在生物系统中,涌现特性无处不在。例如,单个神经元只能产生简单的电信号,但数十亿个神经元组成的大脑网络却能够产生意识、记忆和思维等复杂的认知功能。
生物系统的复杂性还体现在其对扰动的响应上。一个健康的生物系统通常具有很强的鲁棒性,能够在面对内外环境的波动时维持稳定的功能状态。这种鲁棒性并非来自单个组分的坚固,而是源于网络结构的冗余和反馈调控机制。例如,细胞内的代谢网络包含大量的替代途径,当某条代谢通路受阻时,其他途径可以补偿其功能,确保细胞的正常运转。
系统建模与计算模拟方法
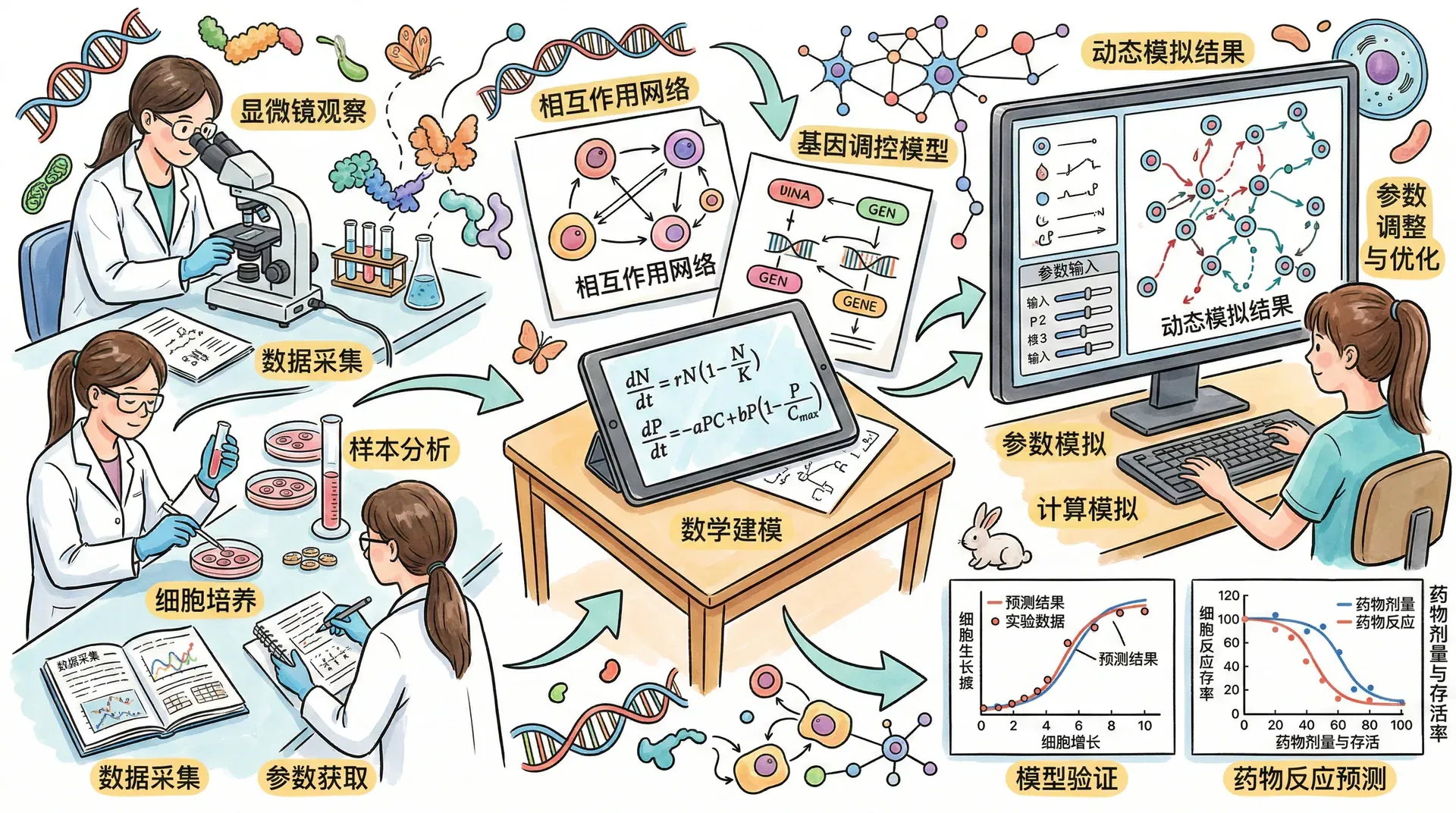
系统建模是系统生物学研究的核心方法之一。通过构建数学模型,研究人员可以定量地描述生物系统的动态行为,并预测系统在不同条件下的响应。生物系统的建模方法多种多样,根据模型的详细程度和应用目的,可以分为不同的类型。
动力学模型是最常用的系统建模方法之一。这类模型使用微分方程来描述系统中各组分浓度随时间的变化规律。例如,在研究基因调控网络时,可以用常微分方程组来描述不同基因的表达水平如何相互影响。上海交通大学系统生物医学研究院的科研团队利用动力学模型研究了肝细胞中脂质代谢的调控机制,发现了多个关键的反馈环路,为理解非酒精性脂肪肝的发病机制提供了新的见解。
约束代谢模型是另一类重要的建模方法,特别适用于研究细胞的代谢网络。这类模型基于质量守恒和热力学约束,通过线性优化方法预测代谢通量的分布。中国科学院天津工业生物技术研究所的研究人员利用约束代谢模型优化了大肠杆菌的代谢途径,成功提高了目标产物的产量,为工业微生物的代谢工程改造提供了理论指导。
随机模型则考虑了生物系统中的随机性因素。在细胞水平上,许多生化反应涉及的分子数量很少,因此随机效应不可忽略。例如,基因表达过程中的随机性会导致即使是遗传背景完全相同的细胞,其基因表达水平也存在显著差异。清华大学的研究团队开发了一种随机模拟算法,能够高效地模拟基因表达的随机动力学,揭示了噪声如何影响细胞的命运决定过程。
计算模拟是系统建模的重要补充。通过数值计算,研究人员可以求解复杂的数学模型,预测系统的行为。现代计算机技术的发展极大地推动了系统生物学的进步。中国的天河二号超级计算机为复杂生物系统的大规模模拟提供了强大的计算支持。例如,研究人员利用超级计算机模拟了包含数千个基因的全基因组调控网络,揭示了细胞如何协调数千个基因的表达来响应环境变化。
系统建模不是简单地用数学公式描述生物现象,而是要抓住系统的本质特征,构建既能反映真实生物学过程又便于分析和计算的模型。
网络生物学与生物网络分析
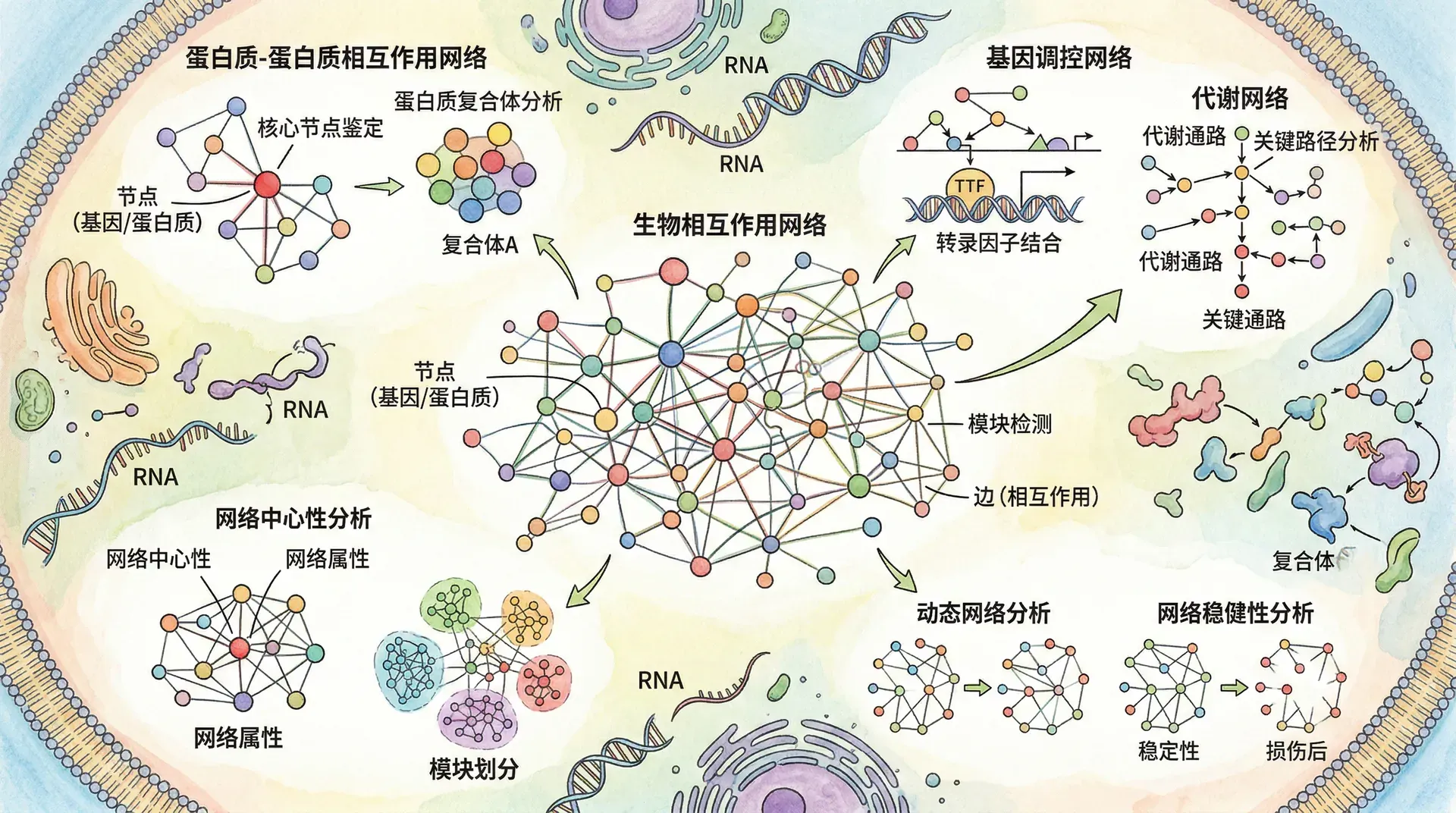
网络生物学是系统生物学的重要分支,通过将生物分子及其相互作用抽象为“网络”,可以揭示生命系统的结构与功能规律。网络中的节点代表基因、蛋白质或代谢物,边表示它们之间的调控、物理作用或代谢转换等关系。对网络结构(如连接方式、拓扑特征)和动态特性的分析,有助于理解生命系统的组织原理。
三大核心网络举例
基因调控网络
节点为基因,边表示转录调控。典型特征是极少数“枢纽基因”拥有大量的调控关系(高连接度),而多数基因只有少数连接。这类无标度特性赋予网络较强鲁棒性。如下图例:
蛋白质相互作用网络(PPI)
北京大学的团队利用高通量技术(如酵母双杂交)构建了上万人类蛋白的PPI网络,展示了蛋白以“复合物/模块”为基础,以小世界方式连接。任意两个蛋白平均可通过不到4个连接建立联系,极大提高信号传递效率。例如:
多数疾病相关蛋白集中于某些功能模块(如信号传递、细胞周期调控)。
代谢网络
节点为细胞内的代谢物,边为酶催化反应。华中科技大学研究发现,大肠杆菌的代谢网络在营养匮乏时能自动激活旁路,维持能量平衡。例如:葡萄糖代谢受阻后,替代碳源(如乳酸、乙醇)相关通路的激活,为工程菌株改造提供理论基础。
常见生物网络类型与应用
网络分析常用方法
网络生物学的研究已证明,生命系统的功能不仅依赖于单一分子,更取决于复杂、层级化的分子关联结构。
系统生物学在疾病研究中的应用
系统生物学以网络整体视角探索疾病成因和治疗方案,不再局限于单基因或通路。以下通过场景和表格结合展示相关主要应用:
典型应用举例
- 癌症分子分型与靶向治疗
复旦大学附属肿瘤医院,整合乳腺癌多组学数据,发现多个驱动基因和异常信号通路,实现根据分子网络特征的个体化分型和治疗。例如,不同患者的癌症虽然病理表现类似,但其分子网络异常各异,需精准“对症下药”。 - 代谢性疾病机制与干预
中国医学科学院通过系统建模分析糖、脂代谢网络,模拟饮食/运动对网络结构的影响。例如,研究发现糖尿病患者在摄入同样热量情况下,如果膳食组分不同,对血糖和脂代谢网络的扰动有本质区别,说明“热量等同≠效果等同”。 - 药物作用机制与多靶点开发
中药往往含多种活性成分,网络药理学研究显示,这些成分可协同作用于多条通路。中国药科大学团队解析了复方连花清瘟中有效成分对COVID-19炎症/免疫通路的作用网络,提高了多靶点药物的筛选效率。 - 传染病防控/新发病原机制探究
新冠疫情中,系统生物学帮助我国科研团队迅速识别病毒与宿主的互作网络,确定ACE2、TMPRSS2等关键分子作为药物和疫苗研发靶标。
各领域应用概览
尽管系统生物学极具潜力,但仍面临数据整合、模型可解释性和实验转化等挑战。例如,如何将异构大数据标准化,以及如何让复杂的网络预测结果为临床医生所用,是当前的难点。
个性化医疗案例
每个人的基因组、生活史、环境暴露各异,因此疾病易感性和最佳治疗方案也需差异化。例如,北京协和医院临床团队整合肺癌患者基因组和转录组信息,建立疾病网络模型—据此精准推荐靶向治疗,显著提升疗效。
个性化精准治疗的流程简图
不同治疗方案对疾病缓解的效果比较
系统生物学与精准医学的结合,使医生能综合患者的遗传、环境及生活习惯信息,更科学地评估风险与选择治疗方案。中国已经建立了大规模生物样本库,为今后的系统医学研究提供坚实基础。
系统生物学方法推动了疾病研究和个性化医疗的变革,但面对的数据整合、模型解释性和转化瓶颈,仍有待技术进步和多学科融合共同突破。
本节练习
1. 系统生物学的核心研究范式是什么?
系统生物学采用“测量-整合-建模-预测-验证”的循环研究范式。首先通过高通量技术获取多层次的组学数据,然后利用生物信息学方法整合分析这些数据,识别关键的调控元件和相互作用关系。在此基础上构建数学模型描述系统的动态行为,通过计算模拟预测系统响应,最后通过实验验证并优化模型。这个循环过程不断深化我们对生物系统的理解。
答案要点:测量多组学数据、数据整合分析、数学建模、计算模拟预测、实验验证与模型优化。这是一个迭代循环的过程,每一轮循环都能加深对系统的理解。
2. 以下关于生物网络拓扑结构的描述,正确的是(多选):
A. 生物调控网络通常具有无标度特征,少数枢纽节点拥有大量连接
B. 随机删除网络中的节点通常会导致网络崩溃
C. 生物网络的小世界特性使得任意两个节点间可通过少数步骤建立联系
D. 网络的模块化结构有助于将复杂系统分解为相对独立的功能单元
答案:ACD
解析: 选项A正确,无标度网络是生物网络的重要特征。选项B错误,正是由于无标度结构,随机删除节点通常不会对网络整体造成重大影响,但删除枢纽节点会导致严重后果。选项C正确,小世界特性使得网络具有高效的信息传递能力。选项D正确,模块性是生物网络的重要组织原理,有助于功能的局部化和系统的鲁棒性。
3. 约束代谢模型(如通量平衡分析)与动力学模型相比,有哪些优势和局限性?请结合具体应用场景说明。
答案要点:
优势: 参数需求少,只需要代谢网络的化学计量信息和反应可逆性,不需要大量动力学参数。适用于大规模代谢网络分析,可以处理包含数千个反应的全基因组代谢模型。计算效率高,基于线性规划的优化算法能快速求解。在预测稳态代谢通量分布方面表现优异,特别适合代谢工程应用。
局限性: 只能分析稳态情况,无法描述代谢物浓度的动态变化过程。需要定义优化目标(如生物量最大化),但真实的细胞目标可能更复杂。不考虑代谢调控机制,如酶活性的变构调节和转录调控。对于涉及快速瞬态变化的过程(如信号转导)不适用。
应用场景: 约束代谢模型特别适合用于工程菌株的设计优化,如提高目标产物的产量、预测基因敲除的表型效应等。而动力学模型更适合研究代谢振荡、瞬态响应等动态过程。
4. 在系统生物学指导的癌症精准治疗中,为什么多靶点治疗策略往往优于单靶点治疗?请从网络鲁棒性的角度解释。
答案: 从网络鲁棒性角度来看,癌细胞的信号网络具有很强的冗余性和适应性,这是多靶点治疗优于单靶点治疗的根本原因。
-
旁路激活机制:当单一靶点被抑制后,癌细胞可以通过激活替代通路来绕过阻断点,维持生存和增殖信号。这种网络的冗余性使得单靶点治疗容易产生耐药性。
-
反馈补偿机制:信号网络中存在大量的负反馈环路,抑制某个节点可能会解除对其上游或其他通路的抑制,反而增强其他促癌信号。
-
网络重构:长期的单靶点治疗会给癌细胞施加选择压力,促使其进化出新的突变或表观遗传改变,重构信号网络结构以逃避治疗。
-
多靶点协同作用:同时作用于网络中的多个关键节点可以更有效地破坏网络的整体功能,减少逃逸途径的可能性。系统生物学方法可以通过网络分析识别出最优的靶点组合,这些靶点在网络中的位置使得它们的联合抑制能够最大程度地破坏癌细胞的生存网络,同时最小化对正常细胞的影响。
因此,基于系统生物学的多靶点治疗策略能够克服网络鲁棒性带来的挑战,提高治疗效果并减少耐药性的产生。