热力学定律
烧水壶里的水从冷变热,铁块在火焰中被加热发红,冰块放在常温下自动融化……这些日常现象中,热量在不同物体之间流动,物体的温度和内部状态随之改变。研究热量与功、内能之间关系的学科,称为热力学。
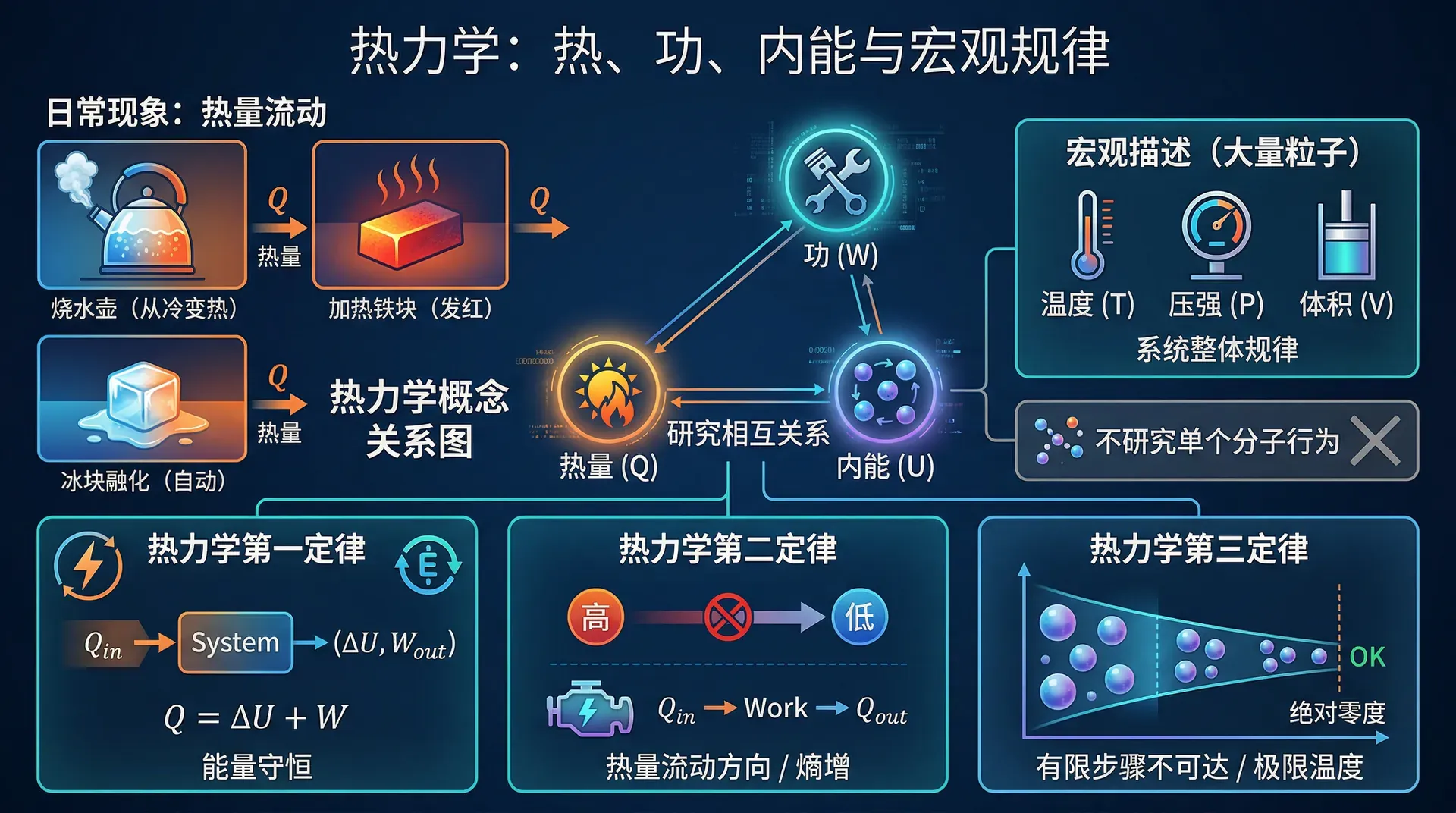
热力学不研究单个分子的行为,而是从宏观角度——温度、压强、体积、热量——描述大量粒子组成的系统的整体规律。它的核心是三条定律,每一条都揭示了自然界中能量转化的基本规则。
热力学基本概念
在正式讨论三条定律之前,需要先明确几个基本概念。
-
热力学系统:研究的对象,例如一瓶气体、一块金属、一杯水。系统以外的一切称为外界(或环境)。
-
内能 :系统中所有分子的动能与势能的总和。内能是状态量——只要系统的状态(温度、体积、组成等)确定,内能就确定,与系统经历何种过程无关。对于理想气体,内能只与温度有关:温度升高,内能增大;温度降低,内能减小。
-
热量 :系统与外界之间因温度差而传递的能量。热量是过程量,只存在于热传递的过程中,不是系统状态的属性。规定:系统吸热时 ,系统放热时 。
-
功 :系统与外界之间因力的作用(如活塞压缩气体)而传递的能量。规定:外界对系统做功时 ,系统对外界做功时 。
热量和功是能量传递的两种方式,两者都是过程量,不能说“物体含有多少热量”或“物体含有多少功”,只能说“传递了多少热量”或“做了多少功”。内能才是状态量,可以说“物体的内能是多少”。
热力学第零定律
两个温度不同的物体接触后,热量会从高温物体流向低温物体,最终两者达到相同的温度,这个最终状态称为热平衡。
- 热力学第零定律(也称热平衡定律):若物体 A 与物体 C 处于热平衡,物体 B 与物体 C 也处于热平衡,则 A 与 B 之间也处于热平衡。
用更直接的方式表达:凡是处于热平衡的物体,都有相同的温度。反过来,温度相同的两个物体,接触后不会发生热量传递。
这条定律看起来简单,却有深刻意义——它为温度的测量提供了逻辑依据。温度计能够测量物体温度,正是因为温度计(物体 C)先后与两个物体达到热平衡,温度计的示数就代表了这些物体的温度。
- 温度的单位:物理学中使用开尔文(K)作为温度的标准单位,称为热力学温标(绝对温标)。与摄氏温度 (℃)的换算关系为:
热力学温度 永远不可能为负值,绝对零度( K)是温度的最低极限,实验上只能无限接近,永远无法真正达到。
例题一:液氮的沸点约为 ℃,干冰(固态二氧化碳)的升华温度约为 ℃,将这两个温度换算为热力学温度。
液氮沸点:
干冰升华温度:
液氮是实验室常用的冷却剂,其温度接近绝对零度,体现了热力学温标的实际意义。
热力学第一定律
系统内能的变化,来自两个途径:热传递(吸热或放热)和做功。热力学第一定律将这两个途径统一起来:
系统内能的增量 ,等于系统从外界吸收的热量 加上外界对系统做的功 。
这条定律本质上是能量守恒定律在热现象中的具体表现——热量和功都是能量,能量总量守恒,不会凭空产生,也不会凭空消失。
例题二:某气体从外界吸收了 J 的热量,同时气体膨胀对外界做了 J 的功,求气体内能的变化量。
按规定,气体对外做功时, J(外界对系统做功为负)。
气体内能增加了 300 J。另外 200 J 的热量转化为气体对外界做的功。
例题三:用打气筒迅速压缩气体时,筒内气体温度明显升高。设压缩过程中外界对气体做功 J,气体向外散热 J,求气体内能的变化量。
气体向外散热,按符号规定: J(系统放热为负)。外界对系统做功: J。
气体内能增加 50 J,表现为温度升高。
热力学第一定律否定了“第一类永动机”的可能性——第一类永动机是指不需要任何能量输入,却能持续对外做功的机器。由 可知,系统对外做功()时,必须有相应的内能减少或从外界吸热,不可能无中生有地产生功。
热力学第二定律
热力学第一定律告诉我们能量守恒,但守恒并不意味着任何过程都能发生。热杯咖啡会自然冷却,冷咖啡不会自动变热——两个过程都符合能量守恒,但只有一个方向在自然界中实际发生。
热力学第二定律描述的正是热过程的方向性。它有两种等价表述:
克劳修斯表述:热量不能自发地从低温物体传向高温物体。 (“自发”是关键词——借助外界做功,可以让热量从低温流向高温,如冰箱和空调,但这需要消耗电能。)
开尔文表述:不可能从单一热源吸取热量,并将这些热量全部转化为功,而不产生其他变化。 (这否定了“第二类永动机”——只从一个热源吸热、完全转化为功、无需向低温热源放热的机器。)
热机(蒸汽机、内燃机)将热量转化为功,但必须有一部分热量流向低温热源(排气、散热),不可能 100% 转化。热机的效率 定义为:
其中 是从高温热源吸收的热量, 是向低温热源放出的热量, 是对外做的功。

卡诺效率是在给定高、低温热源温度下,热机效率的理论上限:
其中温度必须用热力学温度(K)代入。要提高热机效率,需要提高高温热源温度或降低低温热源温度。
例题四:一台热机从温度 K 的高温热源吸收热量 J,向温度 K 的低温热源(环境)放热 J,求该热机的实际效率,并与卡诺效率比较。
实际效率:
卡诺效率:
实际效率(40%)低于卡诺效率(50%),符合热力学第二定律——实际热机由于摩擦、散热等不可逆因素,效率总是低于理论极限。
热力学第二定律否定了“第二类永动机”的可能性。第二类永动机并不违反能量守恒,它试图从海洋、大气等单一热源吸热全部转化为功。热力学第二定律明确指出,这在原理上是不可能实现的,无论设计多么精巧。
熵——无序程度的量度
热力学第二定律说明过程有方向性,但没有给出衡量“方向”的定量工具。为此,物理学引入了熵(entropy,符号 )这个概念。
熵是系统混乱程度(无序程度)的量度。系统越混乱、越无序,熵越大;系统越有序,熵越小。
几个直观的例子可以帮助理解熵的含义:
熵增原理(热力学第二定律的熵表述):在孤立系统中,任何自发过程都向着熵增大的方向进行——即自发过程是不可逆的。
等号对应可逆过程(理想情况),大于零对应实际的自发不可逆过程。
熵增原理并不意味着局部的有序化不可能发生。冰箱内部温度降低,内部熵减小,但冰箱向外界排出更多热量,外界熵增加,整个系统(冰箱 + 外界)的总熵仍然增大。生命体维持高度有序的结构,靠的是不断消耗能量(摄入食物)并向环境排放热量,整个宇宙的总熵依然在增大。
熵增原理赋予了时间一个方向——从过去到未来,孤立系统的熵只增不减。这就是为什么许多自然过程只朝一个方向进行:打碎的鸡蛋不会自动复原,散开的香水不会自动聚回瓶中。熵是区分“时间正向”与“时间逆向”的物理量。
例题五:将 200 g 温度为 ℃ 的水与 200 g 温度为 ℃ 的水混合(不计散热),混合后的温度是多少?这个过程符合热力学第二定律吗?
混合后温度(热量守恒):两份水质量和比热容相同,末温为两者的算术平均:
混合后温度 50 ℃,均匀分布,能量更加分散,系统的熵增大——符合热力学第二定律(孤立系统熵增)。
反向过程(50 ℃ 的水自动分成 20 ℃ 和 80 ℃ 两部分)尽管符合能量守恒,却不符合熵增原理,因此不会自发发生。
例题六:一台冰箱工作时,压缩机消耗电功率 W,冰箱内部(低温热源)每秒从食物中吸热 J,每秒向厨房环境(高温热源)放热多少焦耳?
冰箱是热泵,将热量从低温(冰箱内)泵向高温(室内),需要消耗外界的电能。
由能量守恒:每秒向环境放热 J
冰箱每秒从食物吸热 240 J,消耗电能 120 J,向厨房排放 360 J 的热量。这正是为什么夏天用冰箱降温室内没有效果——排出的热量比吸走的更多。
冰箱和空调并不违反热力学第二定律——它们让热量从低温流向高温,但这个过程依赖外界(压缩机)做功。热力学第二定律禁止的是在不消耗外界能量的前提下,热量自发从低温流向高温。
练习题
1. 关于内能、热量和功,下列说法正确的是( )
A.温度高的物体,内能一定大
B.物体吸收热量,内能一定增大
C.热量是过程量,不能说物体“含有”热量
D.外界对气体做功,气体温度一定升高
答案:C
A 错误:内能与物体的质量、温度、状态都有关。温度高的物体,若质量很小,内能不一定比温度低但质量很大的物体大。B 错误:物体吸热的同时若对外做功,内能可能不变(等温膨胀)甚至减小。C 正确:热量是热传递过程中转移的能量,是过程量,只能说“传递了多少热量”,不能说“含有多少热量”。D 错误:外界对气体做功时,若气体同时向外界放热,且放热量等于外界做的功,内能不变,温度不变()。
2. 某热机从高温热源( K)吸热,向低温热源( K)放热,则该热机的卡诺效率为( )
A. B. C. D.
答案:B
卡诺效率公式(温度需用热力学温度 K):
3. 关于热力学第二定律,下列说法正确的是( )
A.热量可以从低温物体自发传向高温物体,只要总能量守恒
B.热机效率可以达到 100%,前提是工作物质足够好
C.孤立系统中,自发过程总是向熵增大的方向进行
D.熵减小的过程在自然界中绝对不可能发生
答案:C
A 错误:热力学第二定律(克劳修斯表述)明确指出,热量不能自发从低温传向高温,即使总能量守恒也不行。B 错误:热力学第二定律(开尔文表述)明确指出,不可能将从单一热源吸收的热量全部转化为功,热机效率必然小于 100%(卡诺效率是上限,且小于 100%)。C 正确:这是熵增原理的直接表述,孤立系统中自发过程总是沿熵增方向进行。D 错误:局部熵减是可能的(如冰箱内食物降温、生命体维持有序结构),但局部熵减必须以外界更大的熵增为代价,整个孤立系统的总熵仍然增大。
4. 一台冰箱每秒消耗电能 J,冰箱从内部吸热 J/s,则每秒向外界(厨房)排热为( )
A. J B. J C. J D. J
答案:C
冰箱将热量从低温(内部)泵向高温(室内),依赖压缩机消耗电能。由能量守恒:
5.(计算题) 某柴油发动机每循环从高温热源吸收热量 J,向低温热源放热 J。
(1)求该发动机每循环对外做的功 ;
(2)求该发动机的热效率 ;
(3)若该发动机的高温热源温度为 K,低温热源温度为 K,求其卡诺效率,并说明实际效率与卡诺效率的关系。
解题过程
(1)对外做的功
由热力学第一定律(或能量守恒),发动机每循环对外做的功等于吸热与放热之差:
6.(计算题) 一定量气体从外界吸收热量 J,同时气体膨胀对外界做功 J。
(1)求气体内能的变化量 ,并判断内能是增大还是减小;
(2)若该气体随后经历绝热压缩,外界对气体做功 J,求绝热压缩后气体的内能相对于初始状态的变化量。
解题过程
(1)第一步:气体吸热并膨胀
规定:系统吸热 ,外界对系统做功 ,系统对外界做功则 。
气体对外做功 J,即外界对气体做功 J(负号表示气体对外界做功)。