物质的状态
自然界中的物质,绝大多数都以固体、液体或气体三种状态存在。例如,我们常见的水,就是这三种状态变化的经典代表:天气寒冷时,水会结成冰,冰是固体,可以保持固定的形状和体积;当温度升高,冰融化成水,变为液体,可以流动,适应不同容器的形状;继续加热,水会蒸发成看不见的水蒸气,水蒸气是气体,会扩散到空气中,充满整个空间。同一种物质,在不同的温度和压强条件下,可以呈现出完全不同的状态,比如高山上水的沸点就比平原低,而在高压锅里水可以加热到远高于100摄氏度而不沸腾。
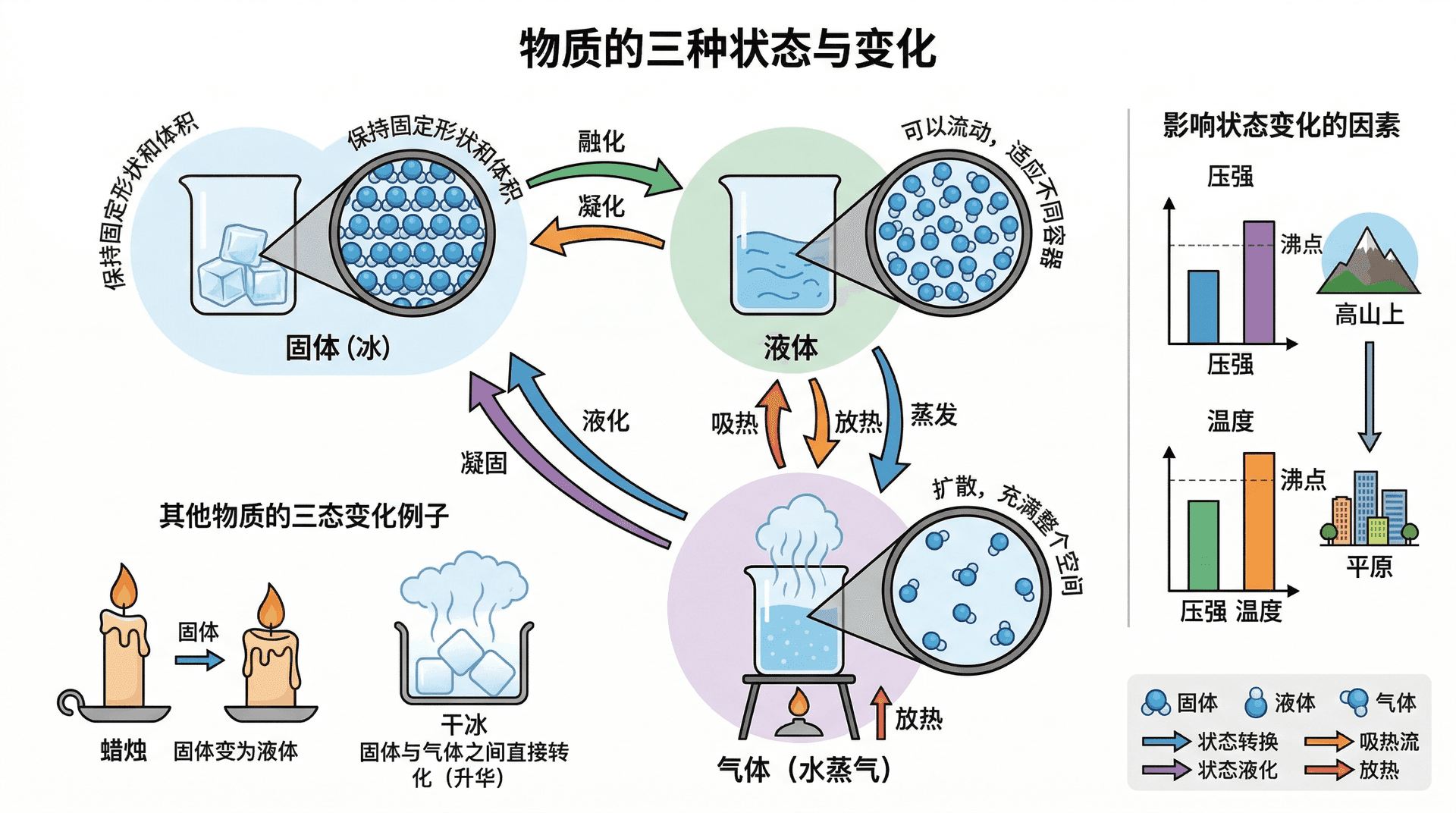
除了水之外,蜡烛的蜡也会在加热时从固体变成液体,而像二氧化碳这样的物质,则可以在干冰(固体)和气体之间直接转化。这些现象在日常生活和自然界中极为常见,充分展现了物质三态变化的丰富和有趣。
固体、液体、气体的特征
物质的三种状态,各有各的特点,从外观和行为上就能区分出来。
三态的对比总结
把三种状态放在一起对比,差别就十分清楚了:
液体和气体都能流动,它们统称为“流体”。工程中的液压系统(如汽车刹车)利用液体传递压力,气压系统(如充气轮胎)则利用气体的可压缩性储存能量。
物质三态的微观解释
物质为什么会有三种不同的状态?答案要从微观层面——分子的排列方式和运动状态来找。
分子的概念
物质是由大量分子组成的,分子是保持物质化学性质的最小微粒。分子的尺寸极其微小,直径大约在 的量级,即大约 。一粒直径 的沙粒,里面大约包含 个分子——这是一个难以直接想象的庞大数字。
分子间的作用力与距离
分子之间同时存在引力和斥力,两者合称为分子力。分子间距离不同,分子力的表现也不同:
分子力的大小与分子间距离密切相关,这一点是理解三态差异的关键。固体不容易被压缩,是因为一旦距离太近,强烈的斥力会阻止进一步靠近;液体不容易被拉开,是因为分子间仍有一定引力。
三种状态的微观图景
-
固体的微观结构:分子(或原子、离子)排列非常规则,像整齐码放的货物一样,每个粒子只在自己的固定位置附近做微小振动,不会离开原来的位置。这种规则排列叫做晶体结构。食盐的晶体、金属中的原子都呈规则排列,这也是固体能保持固定形状的根本原因。
-
液体的微观结构:分子之间的距离比固体稍大,排列不再规则。分子可以在局部范围内移动,就像拥挤的人群——大家挤在一起,但可以互相换位置。液体分子之间仍有足够的引力,所以整体上体积保持不变,但形状可以随容器变化。
-
气体的微观结构:分子之间的距离很大,分子几乎感受不到彼此的引力,各自以极快的速度(常温下约每秒几百米)朝各个方向随机运动,不断碰撞容器壁。气体分子的这种无规则运动,是气体压强的来源,也是气体能充满整个容器的原因。
以下是三种状态微观结构特征的对比:
三态的转化
固体、液体、气体三种状态并不是永远固定不变的,当温度或压强发生变化时,物质可以从一种状态转化为另一种状态。这些转化过程有统一的名称,下面逐一介绍。
熔化与凝固
-
熔化是固体吸收热量,变成液体的过程。冰块放在室温下,吸收了周围环境中的热量,逐渐变成水,这就是熔化。
-
凝固是液体放出热量,变成固体的过程。液态的水放入冰箱,温度降低,失去热量后变成冰,这是凝固。
熔化和凝固互为可逆过程:熔化时吸热,凝固时放热;熔化的温度叫“熔点”,凝固的温度叫“凝固点”,对同一种物质来说,熔点和凝固点相同。
物质分为晶体和非晶体两类,它们在熔化时的表现不同:
晶体熔化时,温度保持在熔点不变,直到全部熔化后温度才继续上升。把冰块放入量筒中加热,会发现一段时间内温度稳定在 ,这段时间内虽然在持续加热,但热量都用于破坏冰的晶体结构,而不是提升温度,这个现象叫做潜热。
以下是一些常见晶体的熔点:
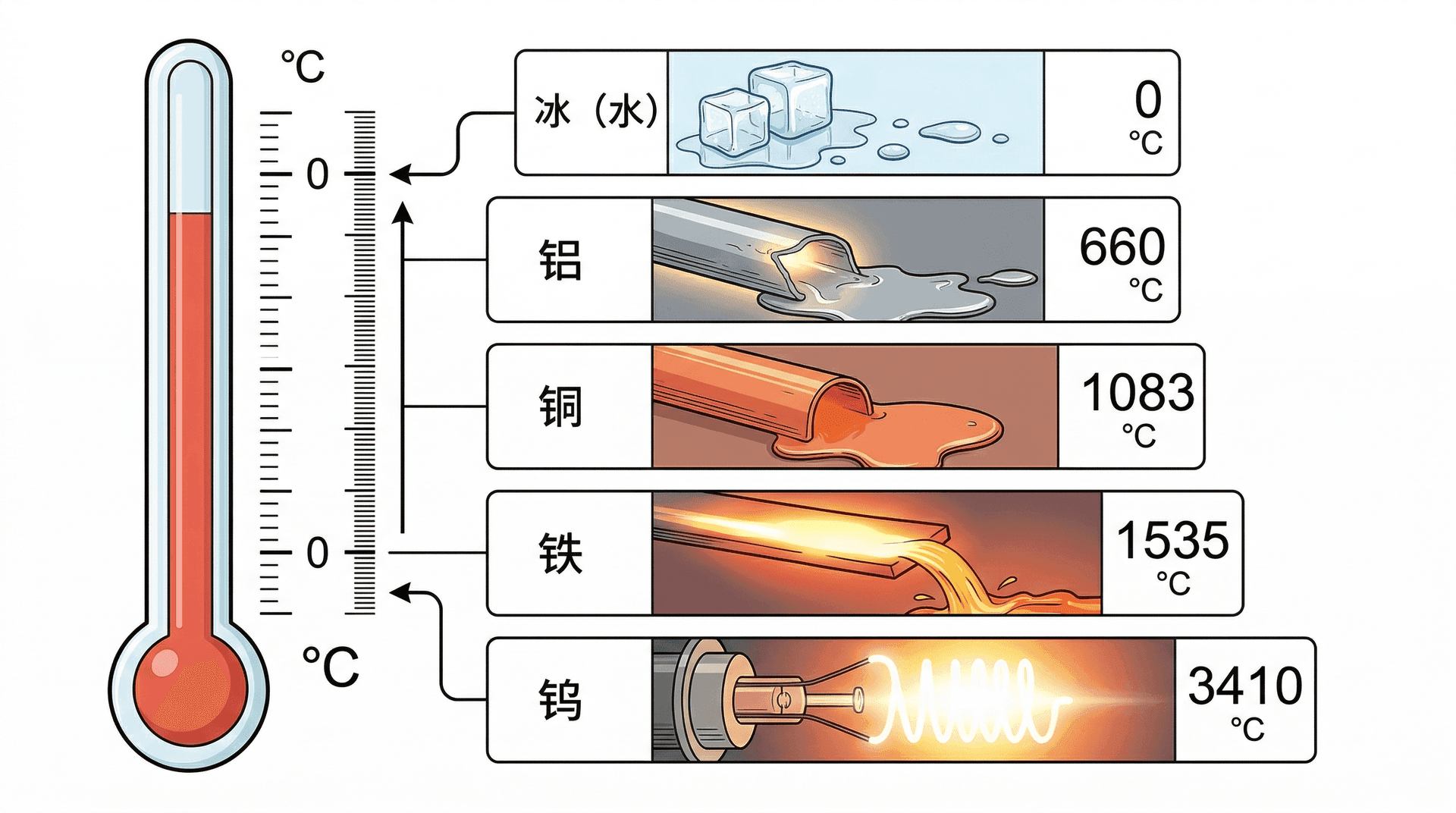
钨的熔点极高,因此被用作灯泡中的灯丝,在高温下仍能保持固体状态发光。
非晶体没有固定熔点,加热时先变软,再慢慢变成液态。玻璃工匠可以在高温下将玻璃塑形成各种形状,利用的正是非晶体这种“软化范围宽”的特性。
蒸发与液化
蒸发是液体表面的分子不断逸出、变成气态的过程。蒸发在任何温度下都能进行,是一个持续发生的缓慢汽化过程。
洗过的衣服晾在通风处,会逐渐变干,这就是水分蒸发的结果。蒸发时,能量较高的分子逃离液体表面,留下的分子平均能量降低,液体温度随之下降——这就是为什么人出汗后吹风会感到凉爽,皮肤表面水分蒸发时会带走热量。
影响蒸发快慢的因素:
-
液化是气态物质放出热量,变成液态的过程,与蒸发正好相反。夏天,冰镇饮料瓶的外壁会出现水珠,这是空气中的水蒸气遇到冰冷的瓶壁降温后液化的结果,而不是水从瓶子里渗出来的。浴室镜子起雾,也是水蒸气液化的典型现象。
-
沸腾是液体在一定温度下,在液体内部和表面同时发生的剧烈汽化现象。沸腾时液体的温度保持在沸点不变,持续吸热。水在标准大气压下的沸点是 ,在高海拔地区(气压低),沸点会低于 ,所以高原上用普通锅煮食物不容易熟透。
沸腾和蒸发都是汽化过程,但二者有明显区别:蒸发在任何温度下都能发生,只发生在液体表面,速度缓慢;沸腾只在达到沸点时发生,液体内部和表面同时进行,速度剧烈。
升华与凝华
- 升华是固体不经过液态,直接变成气态的过程。这个过程需要吸收热量。
干冰(固态二氧化碳)在室温下会直接变成二氧化碳气体,整块干冰慢慢缩小消失,不会留下任何液体,这是典型的升华现象。舞台上制造烟雾效果时,就是利用干冰升华产生大量白色气雾。
碘(紫黑色固体)加热后也会直接升华,变成紫色的碘蒸气,冷却后又直接凝结成固体碘,整个过程都没有液态出现。
- 凝华是气体不经过液态,直接变成固体的过程,与升华相反,凝华时放出热量。
冬天清晨窗户玻璃上出现的冰花,以及树枝上的霜,都是空气中的水蒸气在寒冷表面直接凝华成冰晶的结果。
以下是六种物态变化的汇总:
物态变化的本质是分子间距离的变化。固→液→气的方向,分子间距离增大,需要克服分子引力做功,因此吸热;气→液→固的方向,分子间距离减小,分子势能降低,因此放热。记住“吸热离散,放热聚集”这个规律,六种物态变化的热量方向就不会记错了。
练习题
选择题
第1题 关于固体、液体、气体的微观结构,下列说法正确的是( )
A. 固体分子不运动,液体和气体分子在运动 B. 气体分子间距离最大,分子力最弱,所以气体容易被压缩 C. 液体有固定体积,所以液体分子间距离与固体相同 D. 非晶体内部分子排列和晶体一样规则
答案:B
知识点:物质三态的微观结构。固体分子并非不运动,而是在固定位置附近振动(A 错);气体分子间距离很大,分子间力极弱,外力很容易改变分子间距,所以气体易被压缩(B 正确);液体分子间距比固体稍大,排列不规则(C 错);非晶体内部分子排列无规则,与晶体不同(D 错)。
第2题 下列现象中,属于液化的是( )
A. 冬天哈出的白雾 B. 冰块在室温下变成水 C. 湿衣服在太阳下晾干 D. 冬天窗玻璃上出现冰花
答案:A
知识点:物态变化的判断。冬天哈出的“白雾”是呼出的水蒸气遇冷空气后液化成小水珠(A 正确,液化);冰块变成水是熔化(B 错);湿衣服晾干是蒸发(C 错);窗玻璃上的冰花是水蒸气凝华(D 错)。注意:白雾是小水珠,不是水蒸气,水蒸气是无色透明的。
第3题 将一块冰放入烧杯中,用酒精灯加热,下列关于冰熔化过程的描述,正确的是( )
A. 冰一边熔化,温度一边升高 B. 冰熔化过程中,温度保持在 0 ℃ 不变,但仍在不断吸热 C. 冰是非晶体,没有固定的熔点 D. 冰熔化时不吸收热量,只是温度在升高
答案:B
知识点:晶体熔化的特点。冰是晶体,有固定熔点 0 ℃,熔化过程中温度保持不变(C 错,A 错);虽然温度不变,但酒精灯仍在加热,热量被用于破坏晶体结构(即克服分子间作用力),所以仍在不断吸热(B 正确,D 错)。
第4题 下列四种措施中,能加快液体蒸发的是( )
A. 把湿衣服叠起来放 B. 将液体放入密封容器中 C. 降低液体温度 D. 用电风扇对着湿地板吹风
答案:D
知识点:影响蒸发快慢的因素。加快蒸发需要:提高温度、增大液体表面积、加快液面上方气流速度。叠起来缩小了表面积(A 错);密封后液面气流速度为零(B 错);降温会减慢蒸发(C 错);用电风扇吹风加大了液面上方气流速度,加快蒸发(D 正确)。
计算题
第5题 某工厂需要熔化铝来铸造零件。已知铝的熔点为 ,铁的熔点为 ,钨的熔点为 。
(1)该工厂加热炉的温度至少要达到多少摄氏度,才能将铝熔化?
(2)如果工厂想同时熔化铝和铜(铜的熔点为 ),加热炉温度至少要达到多少摄氏度?
(3)铁制的坩埚(熔化金属用的容器)能否用来熔化铝?铁制坩埚能否用来熔化铁本身?说明原因。
答案:
(1)铝的熔点为 ,加热炉温度至少要达到 才能使铝开始熔化。
(2)铜的熔点为 ,高于铝的熔点 。要同时熔化铝和铜,加热炉温度至少要达到两者中较高的熔点,即 。
(3)铁的熔点为 ,远高于铝的熔点 。当加热炉温度达到 时,铁坩埚仍处于固态,因此铁制坩埚完全可以用来熔化铝。
第6题 在一次物态变化实验中,某同学对一种固体物质(晶体)持续加热,每隔 记录一次温度,数据如下表:
(1)该物质的熔点是多少摄氏度?
(2)该物质的熔化过程持续了多长时间?(从开始熔化到完全熔化)
(3)从第 分钟到第 分钟,该物质平均每分钟升温多少摄氏度?
答案:
(1)从表格中可以看出,在第 、、 分钟时,温度均保持在 不变,说明该物质正在熔化,温度维持在熔点。
(2)熔化过程从第 分钟开始(温度首次达到 ),到第 分钟结束(第 分钟温度开始继续上升),共持续了: