分光光度法检测
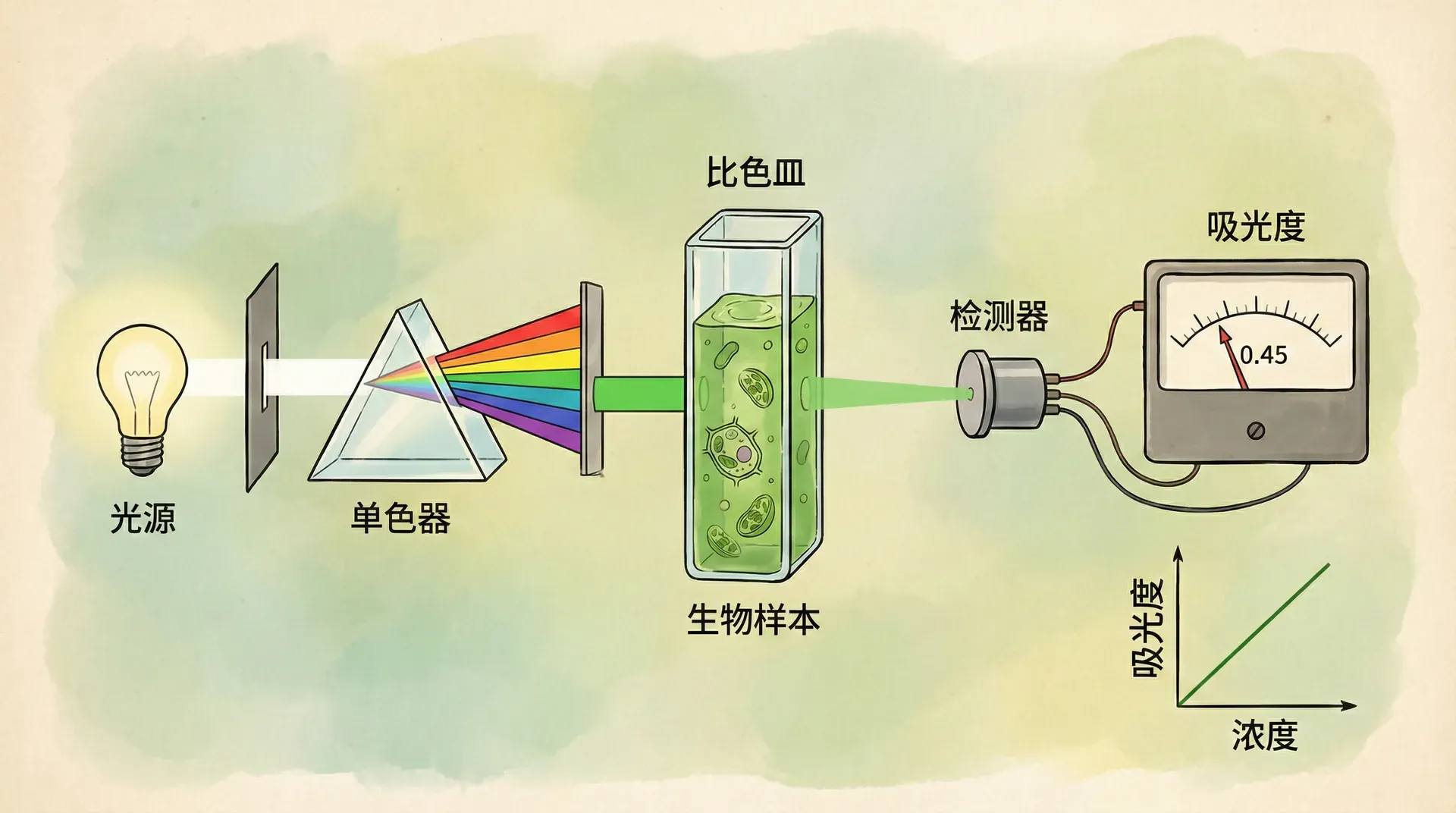
分光光度法作为生物实验室中最常用的分析技术之一,在生物学、化学、医学等多个领域都发挥着极为重要的作用。它利用物质对特定波长光的吸收特性,为我们提供了一种简便、快速且精确的方法来测定溶液中物质的浓度。无论是在日常的蛋白质浓度测定、核酸定量,还是在复杂的酶动力学分析和药物检测中,分光光度法都扮演着不可或缺的角色。举例来说,核酸和蛋白质的定量通常需要测量样品在特定波长(如260 nm和280 nm)下的吸光度,进而推算其浓度,这为分子生物学、基因工程等实验奠定了坚实的基础。
分光光度法不仅广泛应用于科研实验室,也在临床诊断、食品安全检测、环境监测等领域有着广泛用途。例如,在临床检验中,血液中葡萄糖、胆固醇等指标的测定,以及肝功能相关酶活性的检测,均采用分光光度法进行定量分析。此外,随着仪器技术的不断进步,现代分光光度计已经实现了自动化和高通量操作,能够大大提高实验效率,降低人为误差。
学习和掌握分光光度法的基本原理与规范操作,不仅是每一位生物技术工作者的基本功,也是后续开展各种实验和科研工作的基础。我们将从分光光度法的基本原理、仪器结构、测量方法到数据分析,逐步掌握这一重要实验技能,并结合实际案例加深理解,为今后的实验和研究工作打下坚实基础。
透射率与吸光度的数学关系
透射率(Transmittance, )是描述光穿透样品能力的一个基本物理参数。假设入射至样品的光强为 ,穿过样品后的光强为 ,则透射率由下式定义:
实验中常以百分比形式表示透射率,即 。理想纯溶剂中, 接近 ;说明几乎所有光都能通过。
当溶液中有吸光的溶质时, 会因浓度升高而降低,并且这种变化是非线性的。为便于定量分析,引入了吸光度(Absorbance, )的概念。吸光度定义为透射率的倒数的常用(以10为底)对数:
当用百分透射率时,关系式为
这个对数变换将非线性的透射率-浓度关系转变为吸光度与浓度的近似线性关系,这一点对于分光光度法的定量分析非常关键。
吸光度本身是无量纲的,常用“吸光度单位(AU)”表示。在实际操作中,吸光度合理的测量范围为 –,高于时需稀释样品。
下面以几个实际例子说明透射率与吸光度的对应关系:
- 当 ,
- 当 ,
一般建议选择 在 – 之间的数据进行分析,因为光电探测器在此范围响应线性,测量误差最小。例如,若测定蛋白质溶液,吸光度为 时最适合。
朗伯-比尔定律的理论
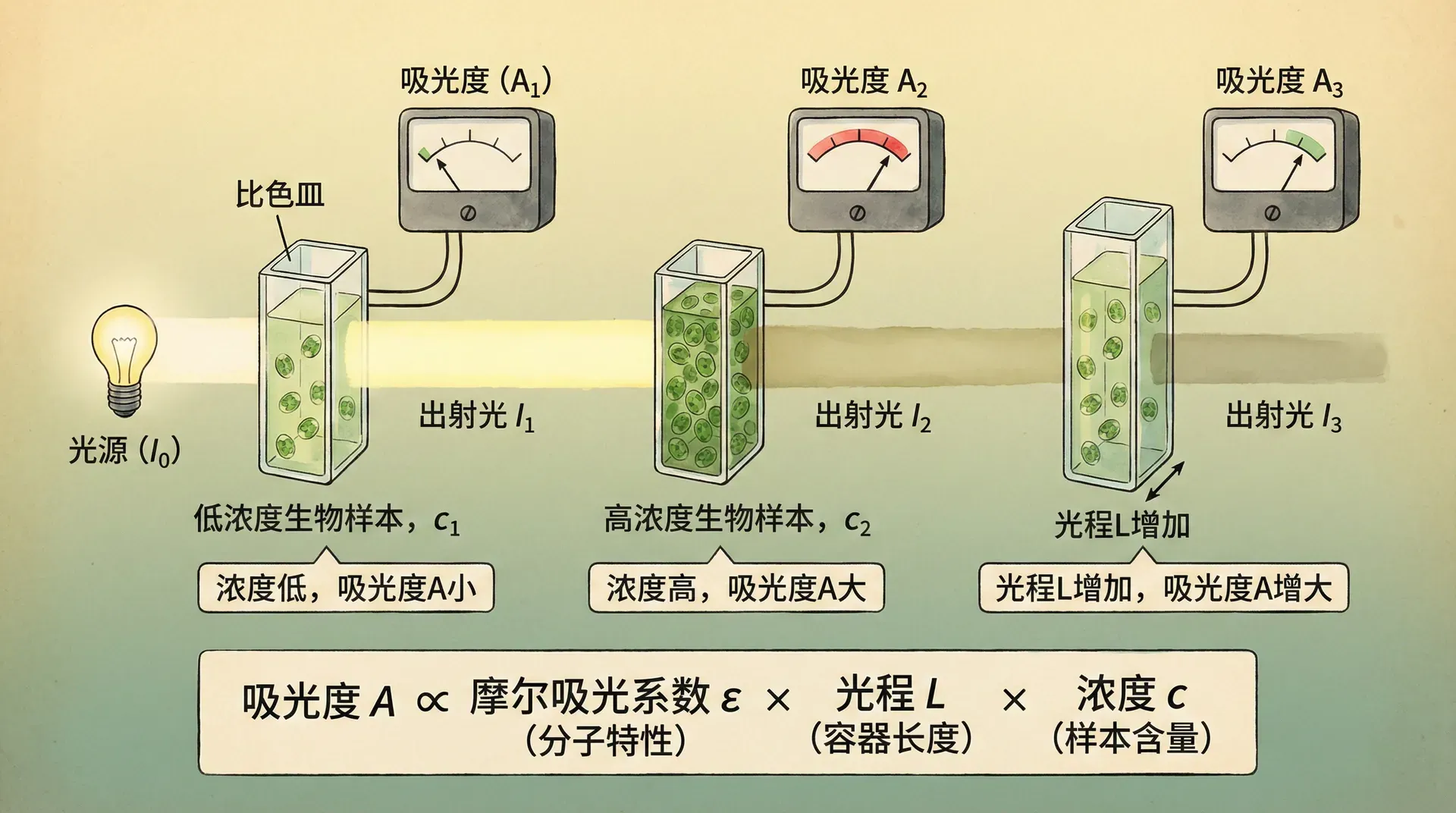
朗伯-比尔定律(Lambert-Beer Law)是分光光度法的核心理论,建立了吸光度、溶质浓度、光程长度之间的定量关系,可表述为:
其中:
- :吸光度
- :摩尔吸光系数(molar absorptivity,),反映某种物质对特定波长光的吸收能力;
- :溶液摩尔浓度()
例如:某染料溶液,假设 ,,,则
说明溶液吸光度为 。
摩尔吸光系数与物质种类、波长有关。以单链DNA为例,在 处 约为 ,而蛋白质在 处差异较大(与氨基酸组成有关)。
实验室常用比色皿光程长度 ,特殊情况下(例如样品浓度较高),可选 cm、 cm等短光程比色皿以保证测量值落在最佳吸光度区间。
朗伯-比尔定律仅在满足一定条件下成立:入射光必须为单色光,溶液要均匀且不产生散射,溶质分子之间不能有相互作用。当溶液浓度过高,可能出现偏离。
在国内如华大基因、诺禾致源等生物技术企业,实验室分光光度计均会定期使用标准溶液严格校准,通常通过配制已知浓度的DNA或蛋白化学品进行校验,以确保仪器数据的准确性、可靠性和溯源性。
下方整理了几种常见生物分子在分光测定中常用的参数,可供快速查阅:
比色法测定的技术要点
比色法是一种基于溶液颜色深浅与物质浓度成正比关系的定量测定方法。许多生物分子本身没有明显颜色,因此需要通过化学反应将其转化为有色产物。选择灵敏、专一且反应条件温和的显色试剂,对于提高方法的准确性和稳定性至关重要。
以蛋白质的比色测定为例,常见的几种方法有各自的优缺点和适用范围:
适当选择比色法,不仅要权衡灵敏度,还要结合样品成分、操作便捷性和检测范围。
例如,下方给出实验室使用场景:
在进行比色测定时,务必设置空白对照。空白管中应包含除待测物外的所有反应成分,用于校正试剂本底与比色皿背景吸收。
核酸的定量分析
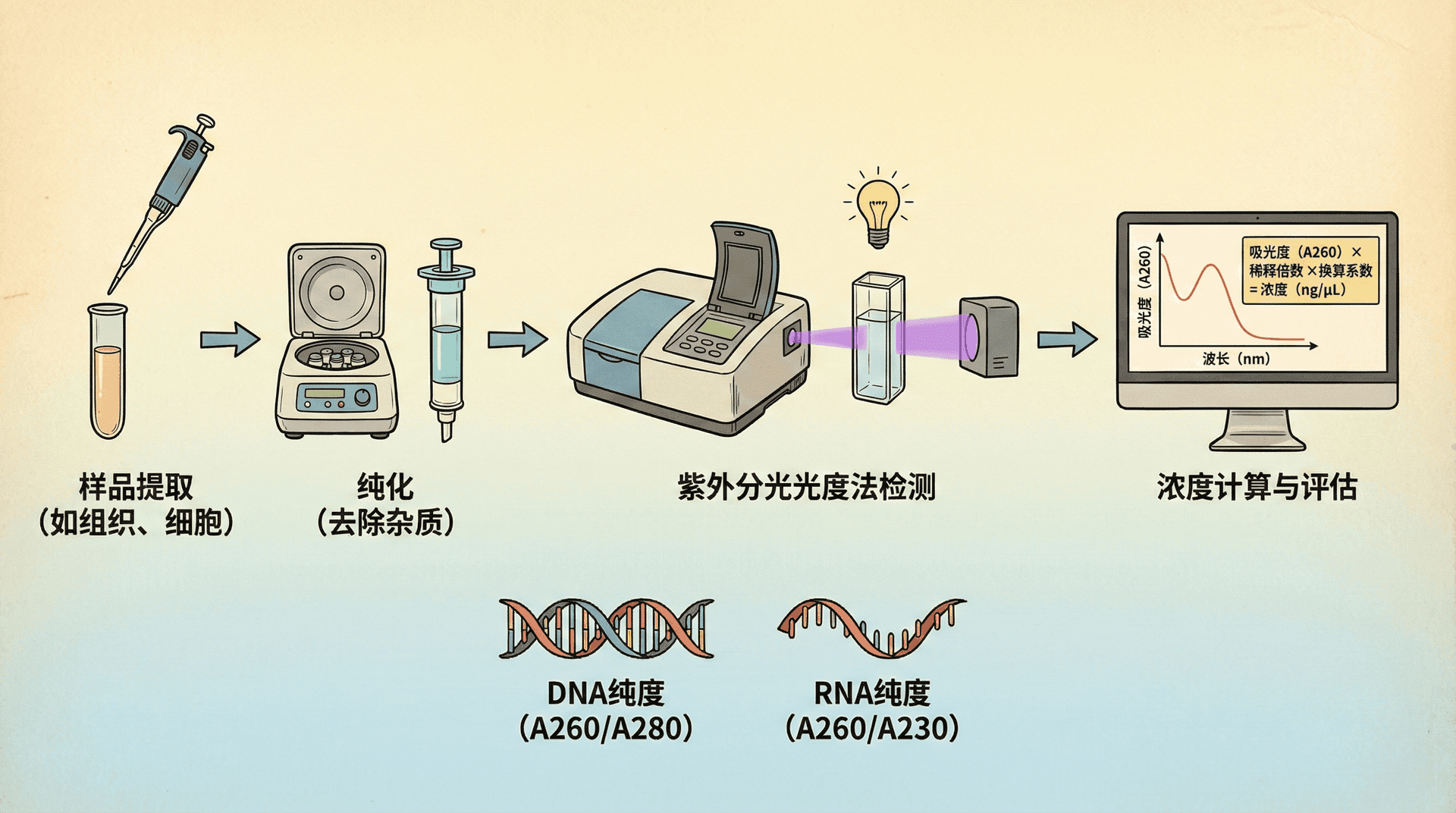
核酸分子拥有大量共轭双键的芳香环结构,因此在紫外波段展现出强吸收峰。DNA和RNA的最大吸收在260 nm附近,这使得紫外分光光度法成为核酸浓度与纯度测定的最常用方式之一。
常见的核酸定量规则如下:
-
DNA:双链DNA溶液在260 nm处吸光度为1时,浓度约50 μg/mL(希尔顿公式)。即:
DNA浓度 (μg/mL) = A₂₆₀ × 50 × 稀释倍数
-
RNA:A₂₆₀为1时,约对应40 μg/mL。
RNA浓度 (μg/mL) = A₂₆₀ × 40 × 稀释倍数
除了浓度,样品纯度同样关键。可通过A₂₆₀/A₂₈₀判断蛋白污染,A₂₆₀/A₂₃₀判断有机残留杂质:
例如,若某DNA样品 A₂₆₀=0.7,A₂₈₀=0.36,稀释倍数为10,则:
- ,说明蛋白污染较少;
如上图所示,纯净DNA在处吸收峰最为显著,处吸收较小;而蛋白质污染后,显著升高,下降。例如,在实验室日常工作中,生物样品的值仅为1.5,通常提示残留蛋白未除净,需进一步提纯。
优质实验室,如北京大学、清华大学的分子生物学实验室,通常要求(DNA)或(RNA),在之间,以保证下游实验数据的可靠性。
需要注意的是,样品缓冲液的组成、测量仪器状态等因素也能对吸光度读数产生影响。因此,经常设定空白对照,并结合标准品进行校准,是保证核酸定量准确的关键。
蛋白质的定量分析
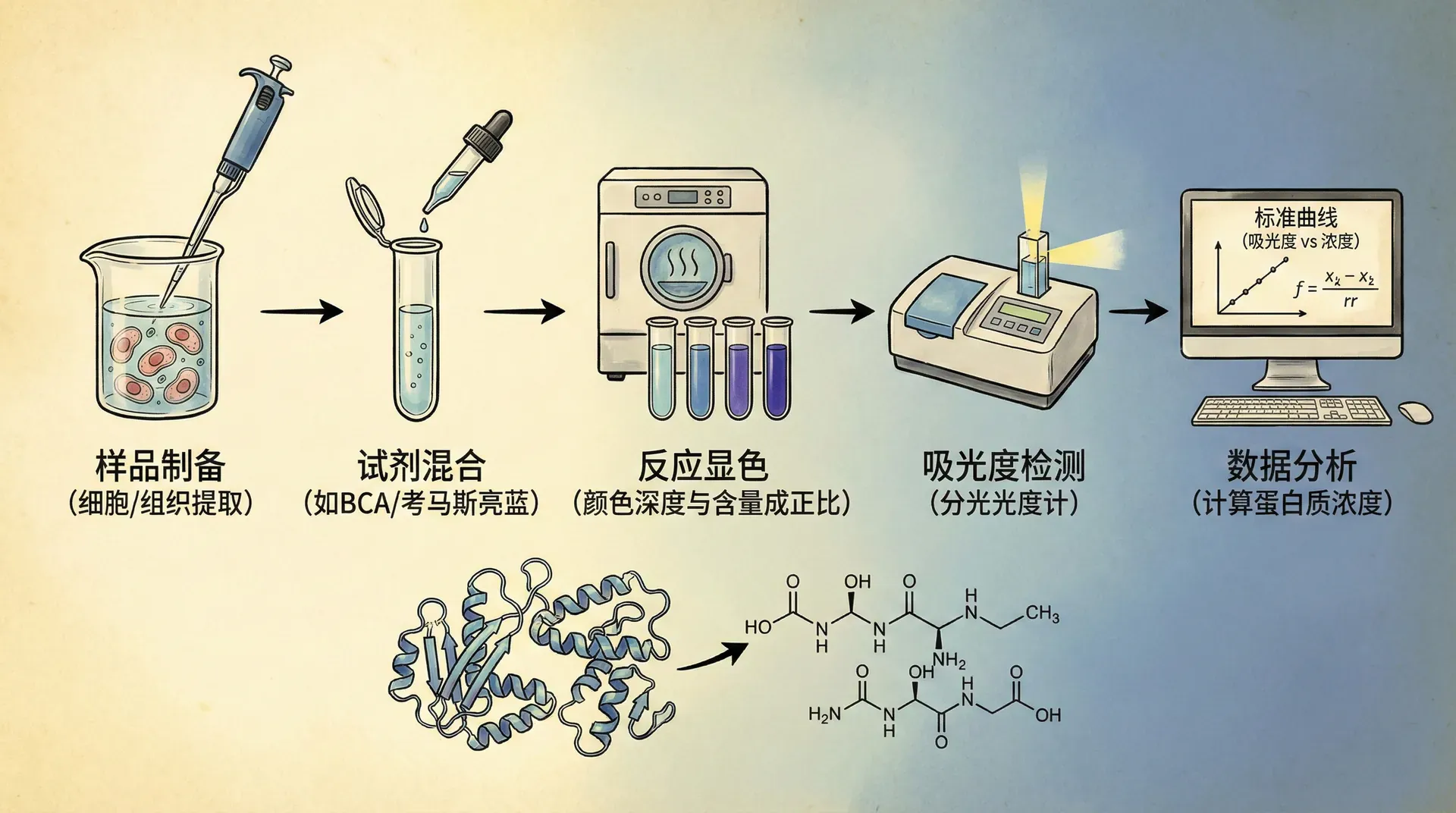
蛋白质在280纳米波长处具有特征吸收,这主要归因于芳香族氨基酸(尤其是色氨酸和酪氨酸)的存在。不像核酸那样摩尔吸光系数比较固定,蛋白质的摩尔吸光系数会随其氨基酸组成和序列显著变化,这导致直接紫外吸收法在各类蛋白测定中灵活性和准确度存在局限。但对于高纯、氨基酸组成明确的蛋白质(如重组蛋白),利用280nm吸收峰快速测定蛋白浓度,仍然是一种高效且无需复杂试剂的常用方法。
下方信息比较了几种常见蛋白定量法的主要特点:
实际上,在生物制药企业如中国生物技术集团的疫苗生产、重组蛋白制备等工业链条上,蛋白质定量检测贯穿原料入库、中间品监测和最终产品质量控制各环节。对于复杂的混合性蛋白样品,单一光吸收法易受核酸、介质等杂质干扰,此时更推荐基于比色反应的BCA或Bradford等方法。
现代实验室通常采取“组合拳”:例如,先用Bradford法快速筛查每批样品大致浓度,然后利用SDS-PAGE考马斯亮蓝染色进行种类和纯度验证,再对目标蛋白用紫外法定量,实现准确性与效率的平衡。例如:在单克隆抗体开发实验中,先用BCA法初筛,再用分光光度法及标准曲线精确定量。
在蛋白定量实验中,建议标准曲线选用与目标样品结构和成分接近的标准蛋白(如牛血清白蛋白BSA),以尽量减小因不同蛋白吸收特性造成的系统性误差。此外注意:实验用缓冲液和空白对照要与样品一致,防止基线偏移影响准确读数。
实验操作的关键细节
尽管分光光度法总体原理直观,但要获得准确可靠的结果,实验操作细节极为关键。以下是常见失误与应对建议:
例如,有实验室采购了新型超微量分光光度计,为节约样品常用“点样微测池”,但发现洗涤不彻底易导致前一份样品残留,进而累积误差。为此,实验室规范要求每测一批样品后,必须用大量纯化水彻底冲洗,比色单元擦干前视检查无挂壁水珠。
如上图所示,理想情况下响应信号与蛋白浓度呈线性关系,但在高浓度时实际测量值出现平台期或偏离直线。其根本原因是朗伯-比尔定律仅适用于低至中等浓度,过量蛋白会导致自我屏蔽或光路饱和。建议当吸光度(A值)超过1.5时及时稀释样本,保证结果真实可靠。
质量控制与误差分析
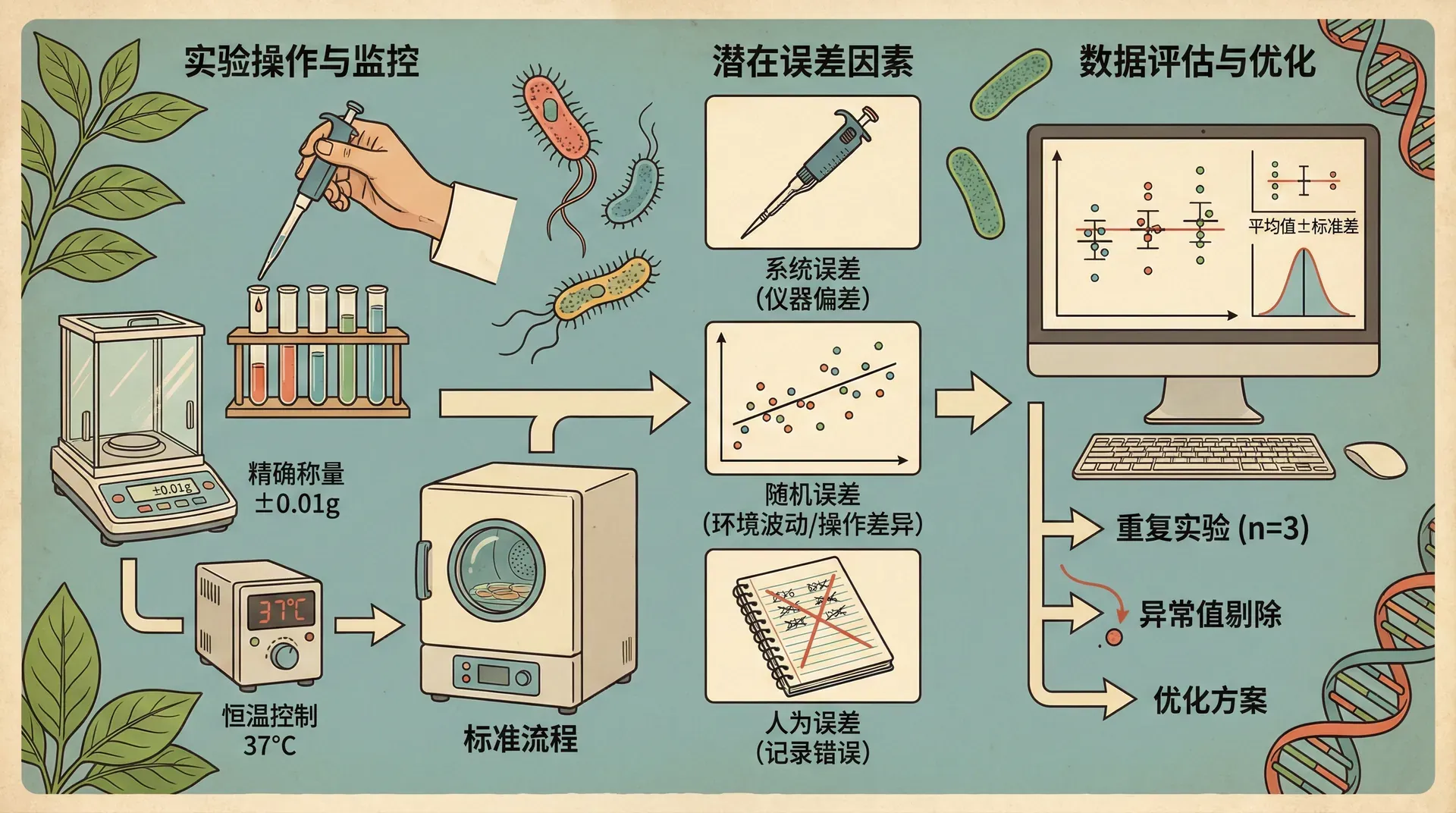
任何生物分析实验都难以做到绝对无误差,因此质量管理体系、误差分析和追踪至关重要。系统误差往往来源于仪器校准、标准溶液配置等实验硬件问题,表现为批次间数据趋势性偏高或偏低。随机误差则多因操作细节(如移液体积微小差异、环境条件)引发。
专业实验室常规流程会设置质控样(如自制蛋白标准品或商业化混合对照)、交叉验证与标准操作流程(SOP)复核。例如进行大型蛋白纯化生产时,批量样品分析会伴随一批质控平行样本,任何测量值明显偏出质控范围都需暂停实验、寻找原因并整改。
常见蛋白定量常规误差因素及调控方法说明如下:
此外,数据处理时应计算平均值、标准差与变异系数(CV),如果CV大于5%,通常说明操作或仪器存在需改进的环节。
在配制标准溶液的过程中,务必采用经过校准的移液器及容量瓶等量器具。哪怕仅有1%的体积偏差,亦会通过标准传播至全部结果,导致系统性误差的积累和实验数据可靠性降低。
总结
分光光度技术正不断迈向微型化、自动化和智能化。如今,便携式分光光度计凭借其内置光电传感器、无线通讯及云平台,已实现现场检测和远程数据共享,在环境监测、食品安全等领域具备广阔应用前景。另外,将分光光度法与色谱等分离分析技术联用,如液相色谱-紫外检测系统,已成为蛋白质组学等领域分析复杂样品的标准方案。
同时,人工智能和机器学习的引入让分光光度数据处理更为智能,通过神经网络等算法挖掘光谱中的深层信息,提升对混合组分的识别能力,特别是在药物质量控制等领域中基于光谱指纹的快速鉴别方法得到越来越多应用。
虽然检测技术不断进步,但分光光度法因其简便、快速、经济等优势,依然是生物技术领域的重要基础工具。只有深入理解原理、严格规范操作,才能充分发挥其价值,为科学研究和生产实践提供可靠数据支持。