分子遗传学基础
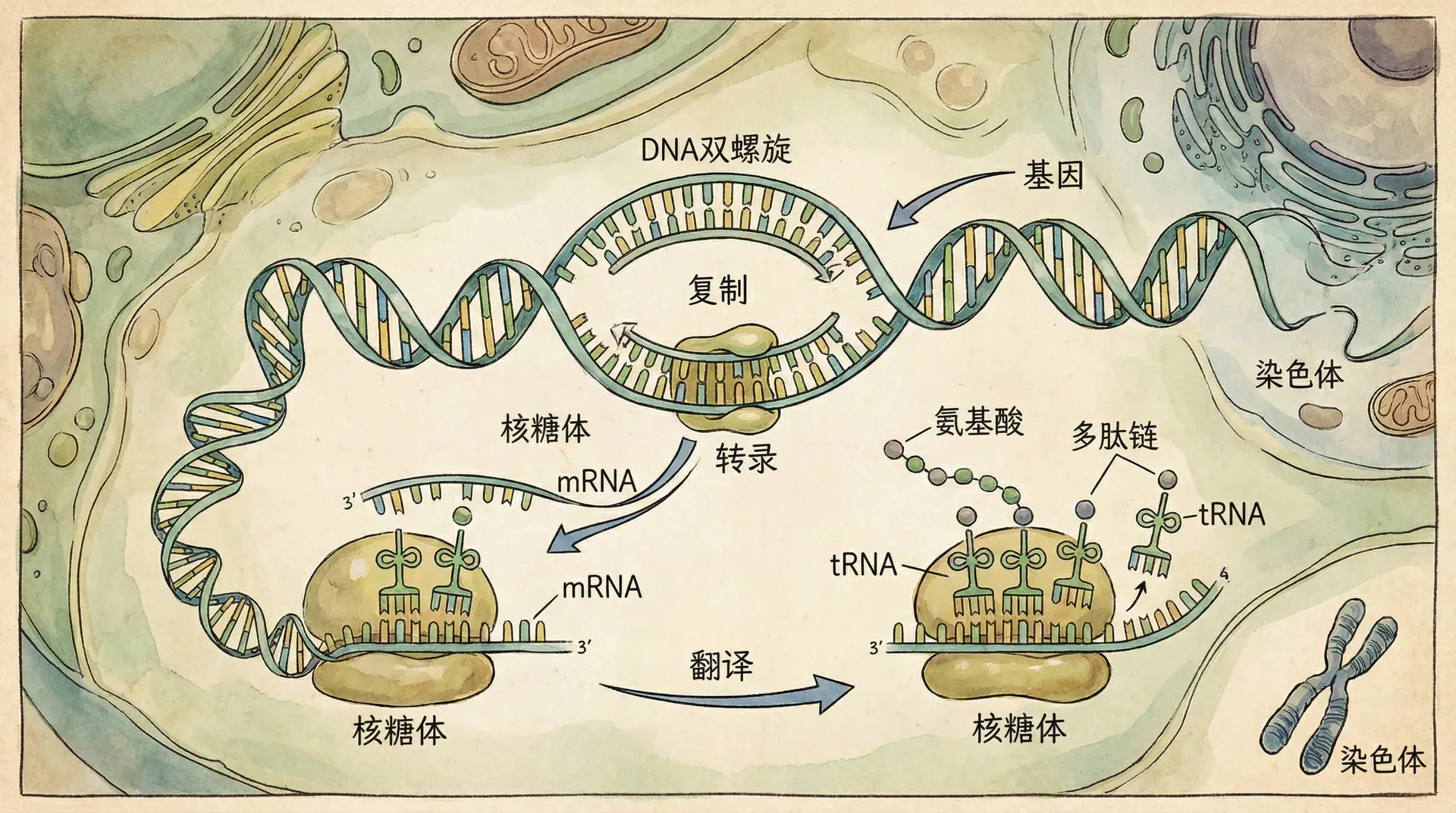
每当我们看到孩子与父母的相似之处时,都会不由自主地感叹遗传的神奇力量。从古人对“种瓜得瓜,种豆得豆”的朴素认知,到现代科学对遗传规律的精确描述,人类对遗传现象的理解经历了一个漫长而曲折的历程。在这个过程中,一个分子的发现彻底改变了我们对生命的认知——它就是脱氧核糖核酸,简称DNA。
DNA的发现不仅解开了遗传的分子机制,更为现代生物技术的发展奠定了基础。从袁隆平院士利用杂交水稻技术提高粮食产量,到屠呦呦教授从青蒿中提取抗疟药物,再到当下火热的基因治疗和精准医学,这些科学成就的背后都离不开对DNA分子机制的深入理解。
DNA承担遗传功能的证据积累
对遗传根源的追寻
上世纪初,学者们已经明确基因在染色体之上,可基因真正的物质基础仍然笼罩在迷雾里。染色体中既包含蛋白质,也含有核酸。从分子构造的复杂性考虑,许多研究者最初更看好蛋白质担当遗传载体角色,觉得其多样性足以胜任复杂遗传指令,而当时的核酸被视作结构简单,没有引起足够重视。直到一系列试验证据逐步积累,科学界才逐渐转变看法。
在这转折过程中,弗雷德里克·格里菲斯于1928年的一项实验成为了分水岭。他并未直接找到遗传物质是什么,但揭示了遗传性质可以在细胞间转移,为后续研究指明方向。
格里菲斯实验
当格里菲斯研究肺炎链球菌时,他发现有可以致病的“光滑型(S)”和无害的“粗糙型(R)”。他混合了被高温杀死的S型菌与活的R型菌,并将混合物注射到小鼠体内。结果不但小鼠死亡,而且这些小鼠血液中分离出的竟然是活的S型菌。
他提出,有某种物质能让R型转变成S型。这种现象后来称作“转化”,意味着细胞可吸收外源遗传因子并出现表型变化。
值得注意的是,这项发现仅证明了传递存在,却没有解释具体是何物质实现的“转化”。直到后来的研究工作者艾弗里等人通过分离纯化实验,才证实发挥作用的关键物质正是DNA。
噬菌体作用实验
虽然“转化实验”有力支持了DNA的重要性,但学界仍有不少异议。直到1952年,赫尔希和蔡斯通过噬菌体实验彻底解决了争议。
他们选择构造单纯的T2噬菌体,它既包含蛋白质外壳又有内部的DNA。研究者们利用同位素为这两种成分分别作标签:给蛋白壳贴上带放射性的³⁵S、让DNA携带带放射性的³²P。噬菌体感染细菌后,科学家分离了被感染后的细胞和外部壳体,检测放射性分布。
实验组别如下所示:
研究结果表明,只有DNA顺利进入细菌并指导后续新噬菌体的合成。蛋白质留在了外面,没有遗传信息的转移。这项实验证明了DNA才是真正承载生命遗传信息的分子。
赫尔希-蔡斯的设计精妙且说服力极强,被认为是现代分子生物学的奠基之作。
查加夫规律
DNA的遗传角色确定后,其内部结构更受到关注。化学家查加夫梳理了不同物种的DNA组成,意外发现重要规律:
- 物种间多样性:不同生物体内,四种碱基的比例呈现各异
- 配对对等性:每一物种内,腺嘌呤(A)与胸腺嘧啶(T)数量极为相近,鸟嘌呤(G)和胞嘧啶(C)之间也几乎等量
来看看具体测量数据对比:
图表中各物种四种碱基的配比一目了然。虽然A、T与G、C的总比例随物种不同而变化,但同一物种内部A对T、G对C的关系始终保持一致。这个规律后来成为解释DNA结构的关键线索。 查加夫的规律为破译DNA分子的排列模式提供了坚实的数据,为双螺旋模型的建立奠定了化学基础。
DNA双螺旋
20世纪50年代初,破解DNA空间结构成为国际科学界关注的核心问题。多个研究组分别展开攻关:鲍林专注于利用化学方法解析分子结构,威尔金斯和富兰克林所在的伦敦国王学院举重若轻地推进X射线衍射实验,而在剑桥大学,沃森与克里克凭借敏锐洞察力和模型构建能力,逐渐厘清思路。相较名声在外的同行,剑桥组并非最被看好,但正是他们善于整合他人实验数据、灵活创新,最终抢先提出了令人信服的结构模型。这场科学突破不仅体现了团队合作和跨领域信息融合的重要,更展示了坚持与科学直觉的价值。
X射线衍射
DNA结构的突破离不开物理化学的前沿利器——X射线衍射。富兰克林精于此道,她拍摄的“照片51”是科学史上极具传奇色彩的一页。通过衍射图样,她观察到栅格状X形斑点,直观反映了DNA分子的螺旋性。科学家由此测算出:
- 双螺旋每转有大约10个碱基对,
- 螺旋直径约是2纳米,
- 紧邻碱基之间的距离在0.34纳米左右。
这为后续模型建立提供了不可替代的数据支撑。
分子层面的对接
深入研究后,沃森和克里克认识到,DNA分子的稳定结构源自碱基之间极其特定的配对方式。
- 嘌呤(腺嘌呤A、鸟嘌呤G) 个头更大,拥有两个环;
- 嘧啶(胸腺嘧啶T、胞嘧啶C) 体积更小,只含单环。
如果仅让两个嘌呤或两个嘧啶结合,DNA链宽度会变得不均匀。只有一条链上的嘌呤正好对应另一链的嘧啶,才能确保螺旋外径恒定。 A总是与T结合,两者之间形成2个氢键;G则与C配对,有3个氢键牵引。这种高度“对等性”正好与查加夫法则所揭示的碱基比例关系不谋而合。
1953年,沃森与克里克仅凭一页论文在《Nature》上发布了他们的假设——DNA为双螺旋结构。短短篇幅中,他们不仅揭示了遗传物质的微观构型,更大胆提出了复制机制的可能模型,为分子生物学开辟新纪元。
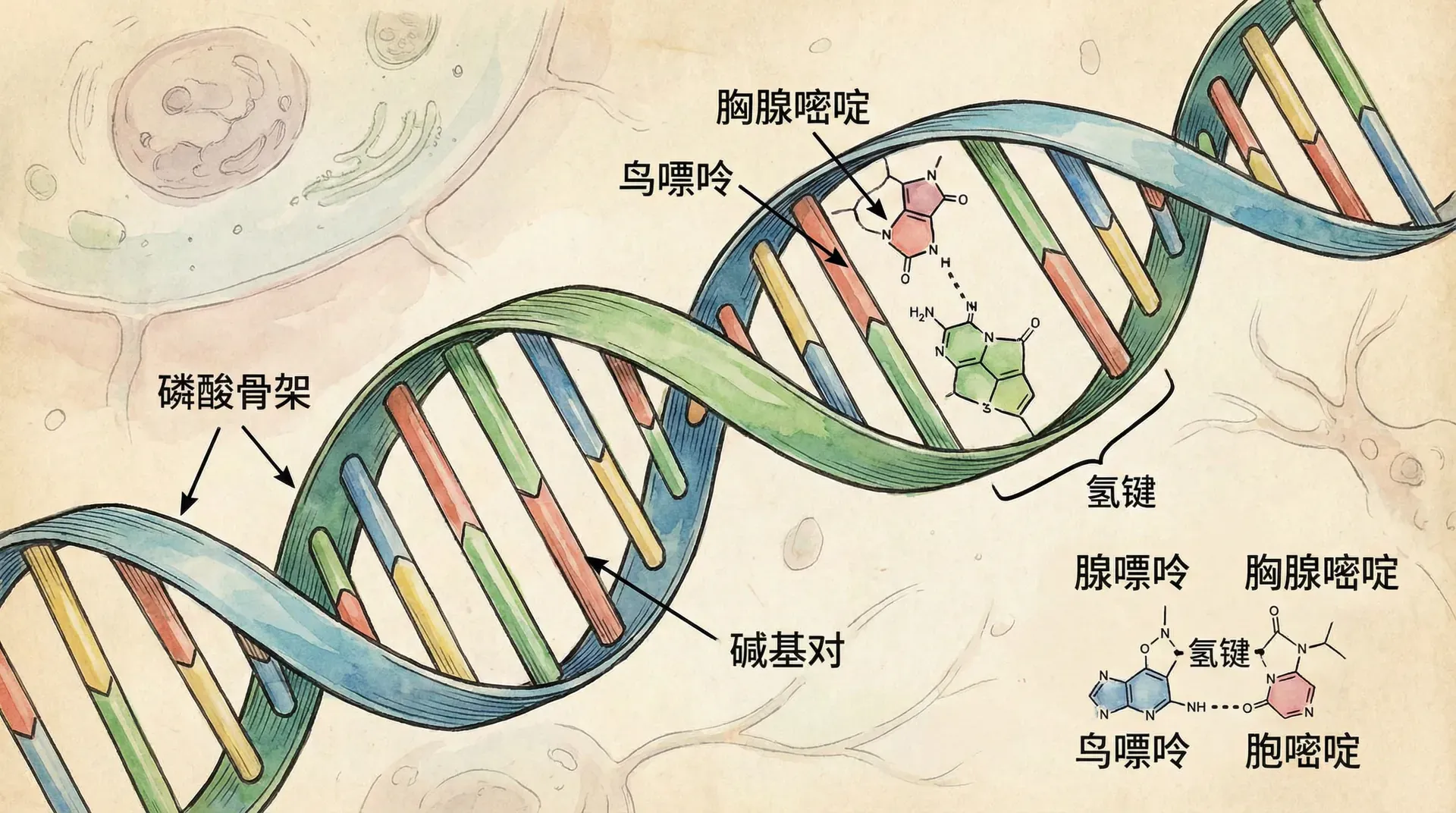
双螺旋
DNA这座“分子阶梯”,拥有如下结构亮点:
DNA复制的分子机制
不同复制模型的构想
DNA的复制机制并非一开始就明朗无疑。当沃森和克里克提出双螺旋结构后,科学界开始思考:遗传信息究竟如何在分子层面无误地传递?最初存在三种主要假设:
这些假说往往只停留在理论层面,难以通过传统实验区分。直到1958年,梅塞尔森和斯塔尔利用15N与14N两种氮同位素,创造性地验证了半保守复制。他们的实验思路堪称分子生物学的典范:
- 让大肠杆菌在15N重氮环境中连续生长,使其DNA均为重型。
- 再转入14N轻氮培养基,观察复制后的DNA密度变化。
- 每一代提取DNA,用密度梯度离心法分析结果。
事实证明,DNA复制后第一代的密度居于两者之间,第二代则出现一半中间型、一半轻型,完美验证了半保守复制原理。这一实验不仅解决了复制机制的问题,更让全世界见证了理论与实验的结合威力。
DNA复制的分步剖析
复制起始点的奥秘
DNA复制的启动有着严格的时空控制。复制的“起点”叫做起始子(origin),就像一部小说的序章。原核生物(如大肠杆菌)整条环状DNA只需一个起点,而真核细胞因染色体体积庞大,设置了成千上万个起始点。每当细胞准备分裂时,专业蛋白复合物会识别这些位置,精确激活复制过程,从而保证整个基因组及时精确地复制完成。
关键分子角色包括:
- DNA解旋酶:主动劈开双螺旋,为复制开路。
- 单链结合蛋白(SSB):迅速缠绕在暴露的单链上,防止其回弹重组。
- 拓扑异构酶:缓解因解旋而产生的DNA过度缠绕现象,确保前行顺畅。
DNA链的合成逻辑
复制的核心由一系列酶密切分工协作完成:
RNA引物的奠基作用
DNA聚合酶“挑剔”地拒绝从零开始,新链合成必须借助引物酶先制造一小段RNA“起点”。随后,DNA聚合酶才能执笔继续书写遗传信息。
前导链与滞后链的策略
由DNA双螺旋的反向平行特性,复制存在不同的“进度通道”:
- 前导链(Leading strand):顺着解旋方向,平稳、连续地拓展新链。
- 滞后链(Lagging strand):逆行而作,只能断续生成短小的“冈崎片段(Okazaki fragments)”,最后由连接酶(ligase)拼接成完整链条。
不同生物体内,DNA复制速度差异显著:
这种速度上的悬殊,并非进化的偶然,而是与遗传物质的总长度、细胞生命周期和生物复杂性密切相关。细菌追求极速繁殖,而复杂多细胞生物则更注重准确性与调控。
复制过程的“质检”
DNA复制中,精确性至关重要。倘若复制频繁出错,生命将陷入信息混乱乃至疾病状态。幸运的是,生物进化出多重校对与修复机制:
DNA聚合酶的校对
许多DNA聚合酶配备3'→5'外切酶“橡皮擦”,能识别并切除新合成链中的错误碱基,这一过程中类似人工智能文本校正工具,高效又可靠。
错配修复系统的补救
即使校对环节漏网之鱼,专门的错配修复蛋白还会巡逻纠偏。这一领域中国科学家如施一公等人的研究为解析修复机制奠定了结构基础。不幸的是,一旦修复系统失灵,就可能导致肿瘤、早衰等严重问题。
DNA的自我修复是维持生命稳定的关键。如果相关基因遭受突变,修复机制失效,极易诱发遗传性疾病和癌症。了解其分子机制对精准医学意义重大。
DNA复制与健康、科技的深层联系
DNA复制研究的意义已远超基础科学:
抗菌“武器”之源
不少抗生素本质上就是靶向细菌DNA复制环节,如环丙沙星抑制细菌拓扑异构酶,结果细菌无法繁殖,被人体免疫消灭。这也提醒我们——过度使用抗生素会促进耐药性进化。
肿瘤治疗靶点
与正常细胞相比,肿瘤细胞有着惊人的增殖速度,对DNA复制过程的依赖性极高。很多抗癌药物正是“趁虚而入”,阻断DNA复制,抑制肿瘤扩展。副作用的出现则推动针对性更强的靶向治疗和免疫疗法不断发展。
分子生物学新工具:PCR技术的崛起
聚合酶链式反应(PCR)模拟体内DNA复制,短时间内扩增出大量特定DNA片段。PCR的出现带动了医学诊断、司法鉴定、传染病检测、动植物基因改良等诸多领域的革命。新冠疫情期间,PCR检测成为全球抗疫的技术“基石”。
总之,DNA复制既是生命最基础的自我继承之道,也是现代生物学、医学、甚至法医领域创新的源泉。走进分子复制的世界,我们能更深刻地理解生命本身之所以精准有序、生生不息的根本原因。
染色体中的DNA包装
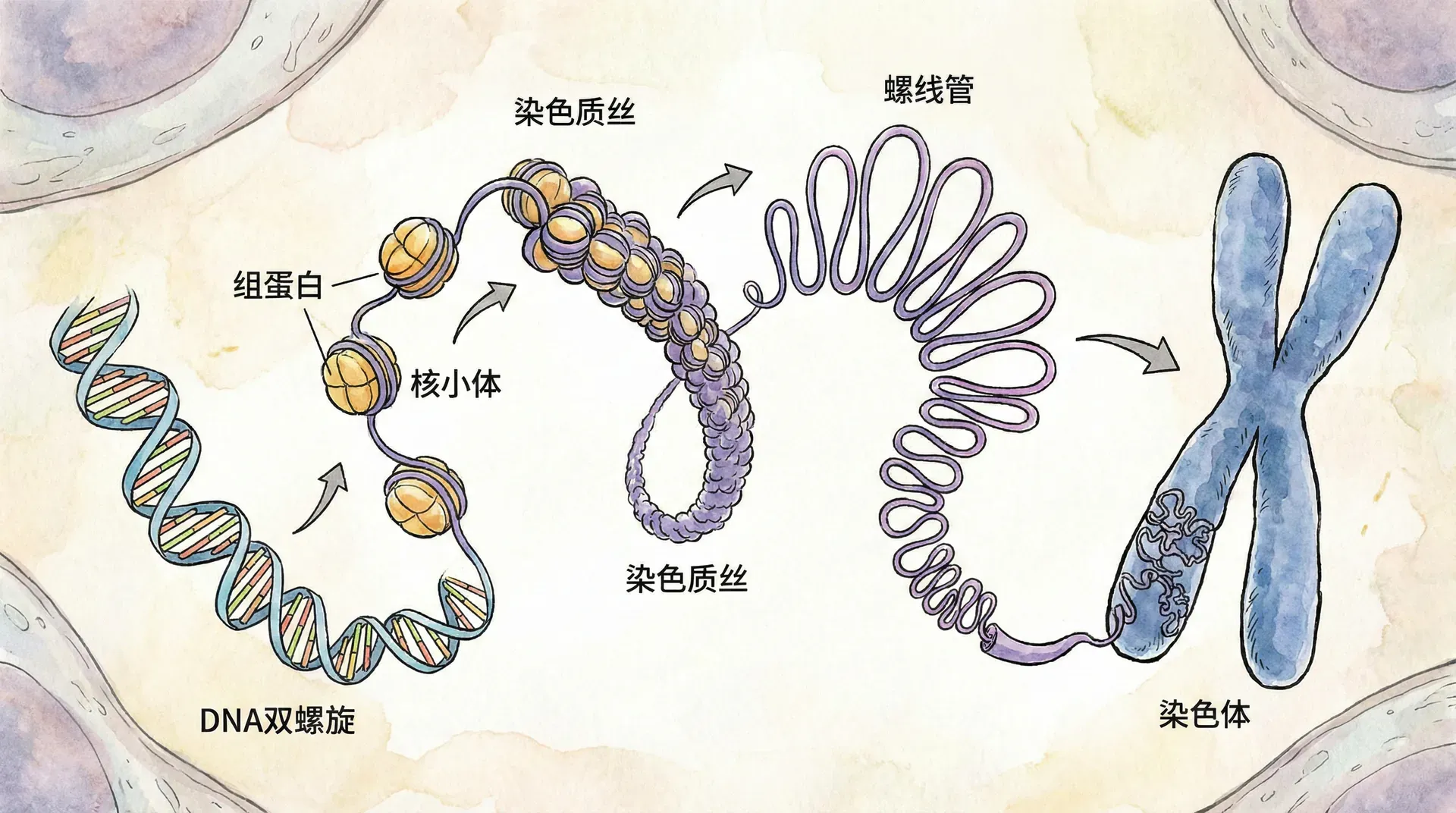
从分子到染色体的层级包装
如果把人类细胞中所有的DNA拉成一条直线,总长度约为2米,而细胞核的直径只有几微米。这就像要把2000公里长的细线塞进一个乒乓球里,这是怎么实现的呢?答案就在于DNA的精密包装系统。
组蛋白
真核细胞中的DNA并不是裸露存在的,而是与一类特殊的蛋白质——组蛋白——紧密结合。组蛋白具有以下特点:
高度保守性:牛和豌豆的同类组蛋白仅相差2个氨基酸,这种保守性反映了其重要的生物学功能。
碱性特征:组蛋白富含赖氨酸和精氨酸等带正电的氨基酸,能够与带负电的DNA磷酸基团紧密结合。
DNA包装的层级结构
DNA的包装遵循严格的层级结构:
第一级:核小体结构(10纳米纤维)
DNA双螺旋缠绕在由8个组蛋白分子组成的蛋白质核心上,形成核小体。这种结构在电子显微镜下看起来像“串珠”,每个“珠子”就是一个核小体,“线”就是连接DNA。
第二级:30纳米纤维
核小体进一步压缩形成直径约30纳米的纤维结构。虽然这种结构很常见,但其确切的组织方式仍然是研究的热点。
第三级:环状结构域(300纳米纤维)
30纳米纤维形成环状结构域,附着在由蛋白质组成的染色体支架上。
第四级:凝缩的染色体
在细胞分裂时,环状结构域进一步卷曲和折叠,最终形成我们在显微镜下看到的高度凝缩的染色体。
让我们用图表来展示DNA包装的压缩比例:
异染色质与常染色质
在细胞核中,并不是所有的DNA都处于相同的包装状态。根据凝缩程度和转录活性,染色质可以分为两类:
这种染色质状态的调节对基因表达控制具有重要意义。许多疾病都与染色质结构的异常有关,比如某些智力发育障碍就与组蛋白修饰异常相关。
端粒
线性染色体面临一个特殊问题:每次DNA复制都会导致末端的一些DNA丢失。为了保护重要基因不被“吃掉”,真核细胞进化出了巧妙的解决方案——端粒。
端粒位于染色体末端,由重复的DNA序列组成。在人类中,这个序列是TTAGGG,重复100-1000次。端粒就像鞋带两端的塑料套,保护染色体不会“散架”。
端粒与衰老:随着细胞分裂次数的增加,端粒逐渐缩短。当端粒缩短到一定程度时,细胞就会停止分裂或死亡。这被认为是细胞衰老的重要机制之一。
端粒酶的作用:在生殖细胞和某些干细胞中,端粒酶能够延长端粒,使这些细胞保持无限分裂的能力。有趣的是,许多癌细胞也会激活端粒酶,这可能是它们获得“永生”能力的原因之一。
让我们来看看不同年龄段人群的平均端粒长度变化:
端粒长度的研究为抗衰老医学提供了新的方向,但同时也要谨慎,因为无限激活端粒酶可能增加癌症风险。
总结
DNA分子的研究历程展现了科学探索的魅力——从最初对遗传现象的好奇,到今天对分子机制的精确理解,每一步都凝聚着科学家们的智慧和努力。这些基础研究不仅帮助我们理解了生命的本质,更为现代生物技术的发展奠定了坚实基础。
在中国,DNA相关技术的应用也取得了举世瞩目的成就。从华大基因在基因组测序领域的突破,到张锋等华人科学家在基因编辑技术方面的贡献,再到新冠疫情期间mRNA疫苗技术的快速应用,这些都离不开对DNA分子机制的深入理解。
随着技术的不断进步,我们对DNA的理解将会更加深入,这必将为人类健康、农业发展和环境保护带来更多的机遇和挑战。
基于DNA的技术还将在更多领域发挥作用:精准医学将根据个体的基因特点制定治疗方案;基因治疗将为遗传病患者带来希望;合成生物学将创造出全新的生物系统为人类服务。这些激动人心的前景,都建立在我们今天所学习的这些基础知识之上。生命科学的发展永无止境,每一个新发现都可能改写我们对生命的认知。正如沃森和克里克当年的发现改变了整个生物学一样,未来的突破也将继续推动人类文明的进步。