物质的微观结构
物质世界的多样性令人叹为观止:金属能导电,木材可以燃烧,食盐溶于水,钻石坚硬无比。这些截然不同的性质,根源究竟在哪里?当我们把宏观物质不断细分,最终会来到肉眼无法看见的世界——原子的尺度。原子是构成物质的基本单元,它的内部结构决定了物质的一切化学性质和大部分物理性质。
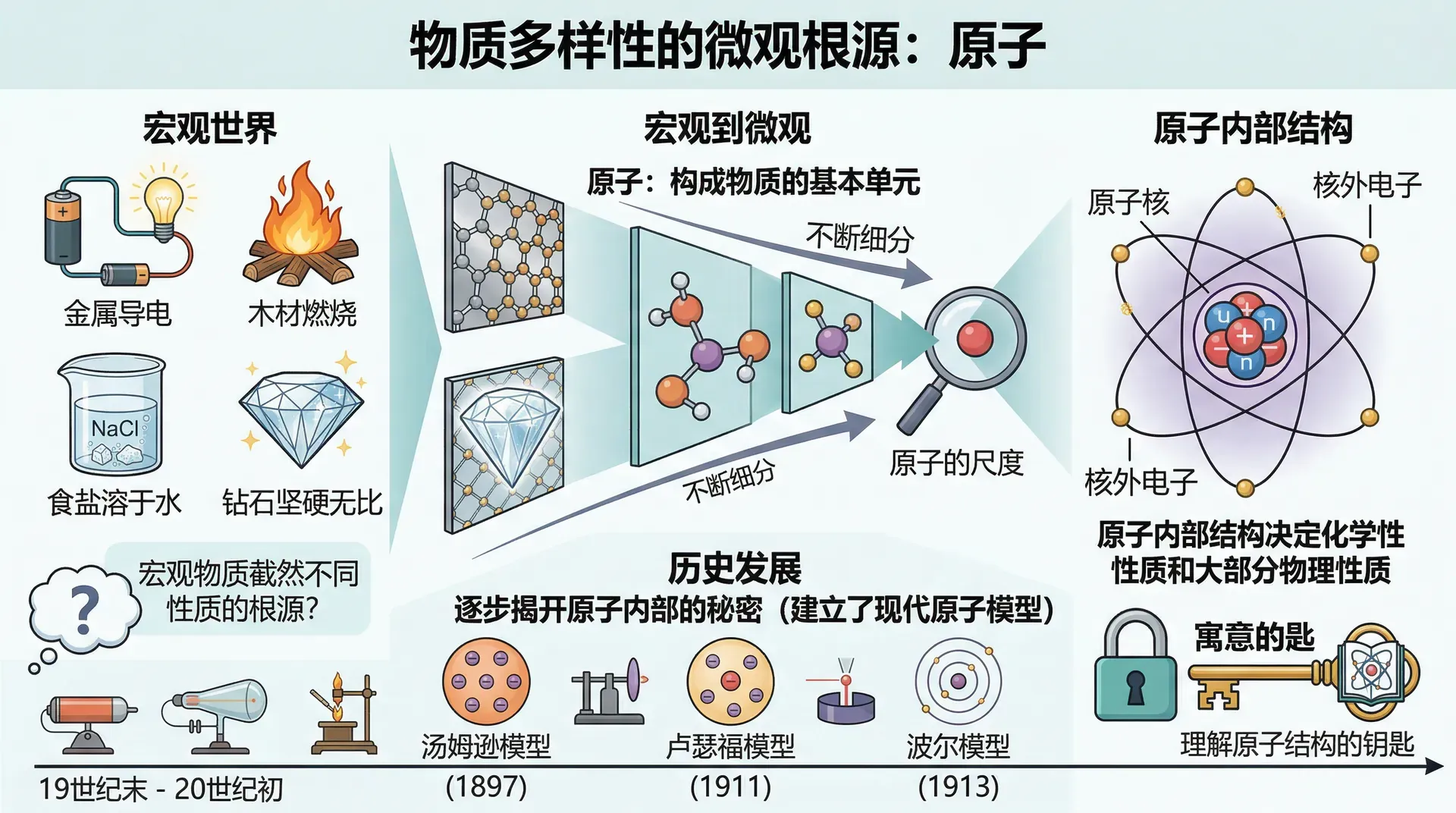
理解原子的结构,是读懂整个物质世界的钥匙。从19世纪末到20世纪初,物理学家经过一系列精密实验,逐步揭开了原子内部的秘密,建立了我们今天所熟知的原子模型。
原子的基本结构
原子的直径约为 数量级,远远小于头发丝的直径。在这样微小的空间里,原子并不是一个实心的小球,而是有着精细的内部构造。
1911年,英国物理学家卢瑟福通过著名的 粒子散射实验,得出结论:原子中心存在一个极小但质量集中的区域,称为原子核;原子核外围存在着带负电的电子,在核外空间中运动。原子核的直径约为 ,仅为原子直径的万分之一,但却集中了原子几乎全部的质量。
原子核由两种粒子组成:质子和中子。
其中 ,是元电荷,质子所带的正电荷量与电子所带的负电荷量大小相等。
整个原子对外表现为电中性,是因为原子核中质子数等于核外电子数。质子数用 表示,称为原子序数,它决定了该原子属于哪种元素。
例1 碳原子的质子数为 ,中子数为 ,核外有 个电子。整个碳原子不带电,因为 个质子的正电荷与 个电子的负电荷完全抵消。
例2 氧原子的质子数为 ,核外有 个电子,通常含有 个中子。原子核中共有 个核子(质子和中子统称核子)。
原子的质量主要集中在原子核上,电子质量极小,可以忽略不计。原子的体积几乎都是空的——如果把原子核放大到一个足球那么大,整个原子的范围则相当于一座大型体育场。
核外电子并非杂乱无章地分布,而是按照能量高低分层排列,称为电子层(也叫电子壳层)。离原子核最近的第一层最多容纳 个电子,第二层最多容纳 个电子,第三层最多容纳 个电子。原子最外层的电子数决定了该元素的化学性质。
最外层有 个电子(第一层有 个时满足稳定)的原子,化学性质最为稳定,不易与其他物质发生反应。氦、氖、氩等稀有气体就属于这种情况。
相对原子质量
原子的实际质量极其微小。例如,一个氢原子的质量约为 ,一个碳原子的质量约为 。直接使用这些数值进行计算非常不便,因此物理学和化学中引入了相对原子质量的概念。
以碳-12原子质量的 作为标准单位,其他原子的质量与这个标准单位的比值,就是该原子的相对原子质量,用符号 表示:
相对原子质量是一个纯数,没有单位。碳-12原子质量的 约为 ,这个数值称为原子质量单位,符号为 (或 )。
由于质子和中子的质量都约等于 ,电子质量远小于 ,所以原子的相对原子质量在数值上约等于该原子核中质子数与中子数之和,即质量数:
其中 为质子数, 为中子数, 为质量数。
例3 铁原子含有 个质子和 个中子,其质量数为:
铁的相对原子质量约为 ,与质量数一致。
例4 铝原子含有 个质子和 个中子,质量数为 ,相对原子质量约为 。
常见元素的相对原子质量:
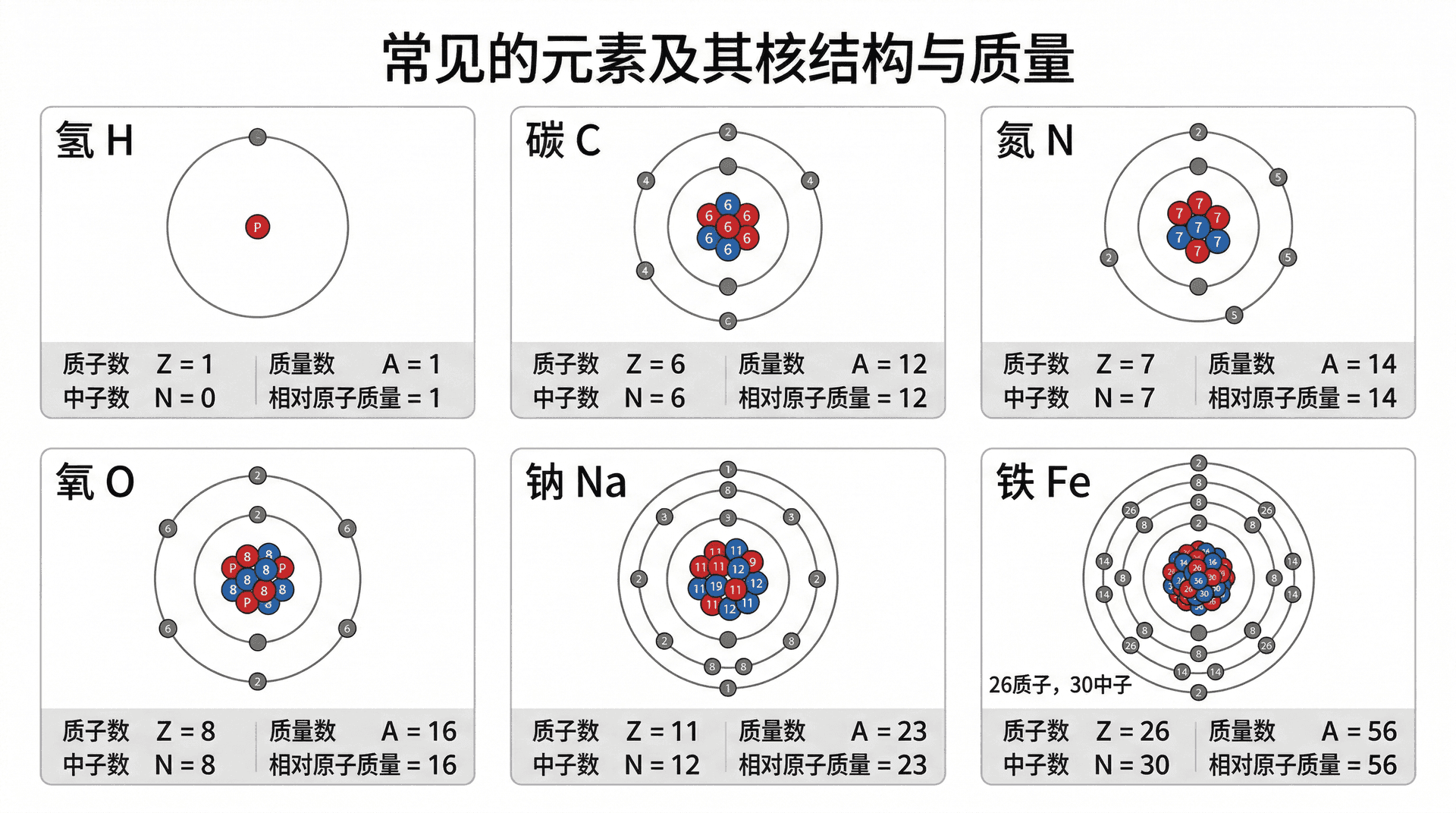
质量数 与相对原子质量在数值上非常接近,但两者并不完全相同。质量数是整数,而相对原子质量可以是小数(天然元素往往由多种同位素混合,相对原子质量是各同位素按丰度加权平均的结果)。
元素与同位素
元素是具有相同质子数的一类原子的总称。质子数决定了原子的化学性质——质子数相同的原子,化学性质基本相同,归为同一种元素。例如,所有质子数为 的原子都是碳元素,不论其中子数是多少。
然而,同一种元素的原子,中子数可以不同。质子数相同、中子数不同的原子,称为该元素的同位素。
碳元素有三种天然同位素:
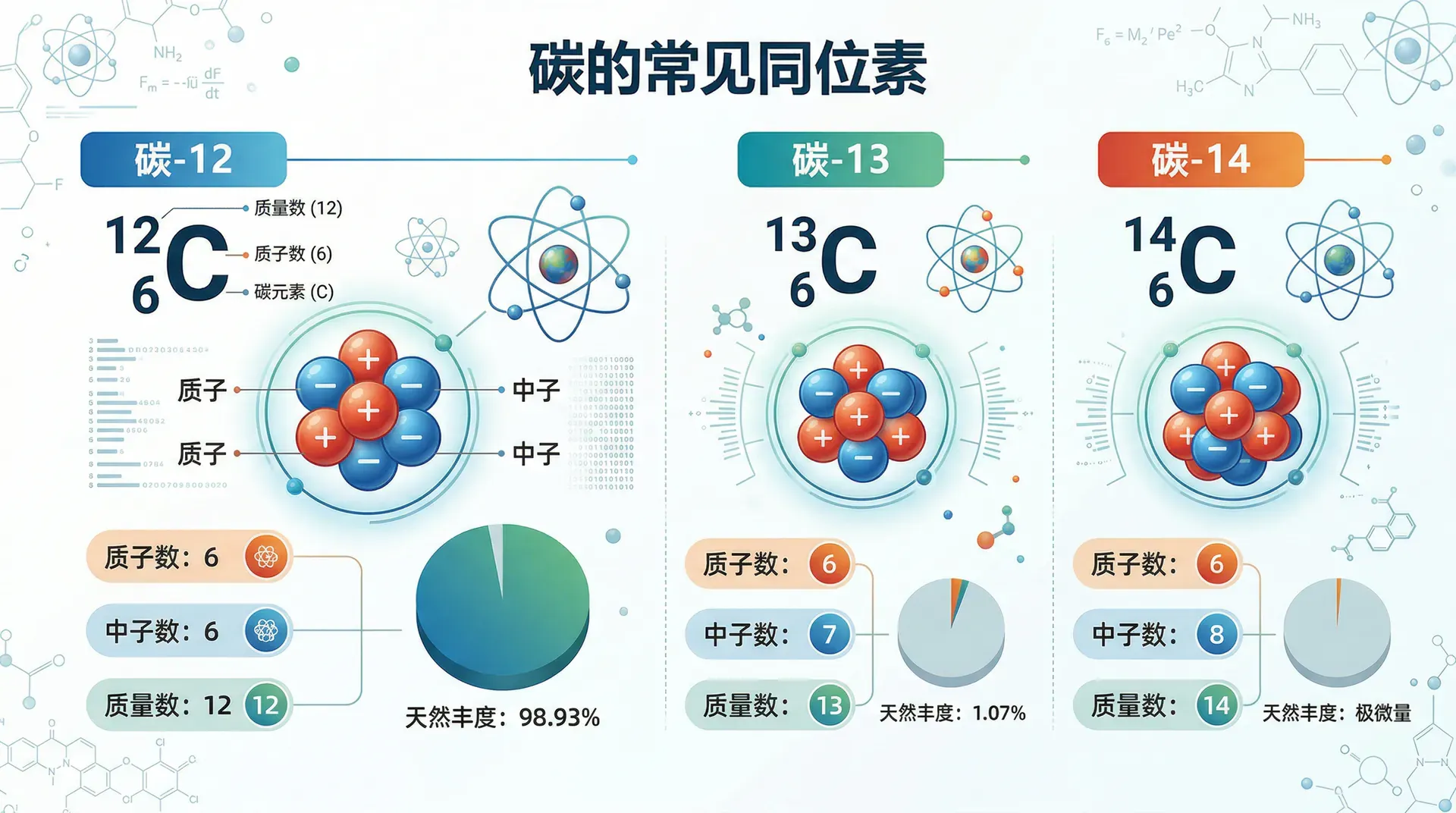
同位素的表示方法为 ,左上角为质量数,左下角为质子数, 为元素符号。
同位素有以下特点:质子数相同,因此化学性质几乎完全相同;中子数不同,因此质量数不同,物理性质(如密度、沸点)略有差异;有些同位素是稳定的,有些则具有放射性。
氢元素有三种同位素,常用名称和性质对比如下:
碳-14是考古学中的重要工具。由于生物体在生存期间不断与环境交换碳元素,体内碳-14含量保持恒定;生物死亡后,碳-14持续衰变减少。通过测量遗存物中碳-14的含量,可以推算出其距今的年代,这种方法称为放射性碳定年法。
同位素在工业、医学、科研中有广泛应用。铀-235和铀-238是铀元素的两种同位素,前者可以发生链式反应,是核电站的燃料;碘-131是放射性同位素,用于甲状腺疾病的诊断和治疗。
放射性与核衰变
某些原子核不稳定,会自发地从内部发射出射线,同时转变为其他原子核,这种现象称为放射性,这类原子核称为放射性核素。这一过程称为核衰变。
放射性现象由法国物理学家贝可勒尔于1896年发现,随后居里夫人对此进行了深入研究,发现了钋和镭两种放射性元素。
核衰变过程中发出的射线主要分为三种:
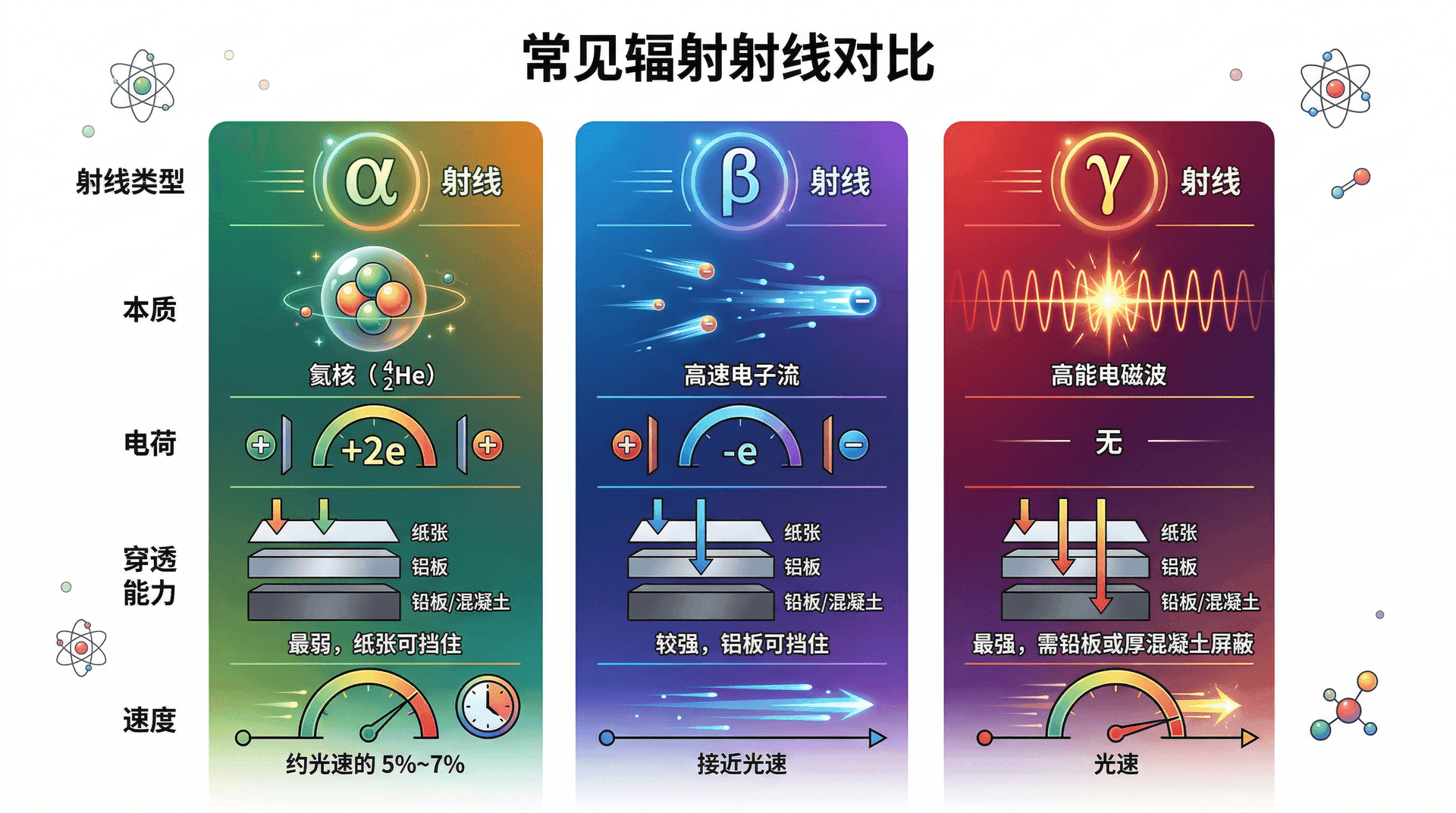
衰变:原子核放出一个 粒子(即氦核 ),质量数减少 ,质子数减少 :
例5 铀-238发生 衰变,生成钍-234:
核反应前后,质量数(上标)守恒:;质子数(下标)守恒:。
衰变:原子核中一个中子转变为质子,同时放出一个电子(即 粒子),质量数不变,质子数增加 :
例6 钍-234发生 衰变,生成镤-234:
质量数不变:;质子数守恒:。
射线通常伴随 衰变或 衰变一起发射,是原子核从高能态跃迁到低能态时释放的能量,本身不改变原子核的质量数和质子数。
放射性物质对人体有害。 射线虽然穿透力弱,但若放射性物质进入人体内部, 射线会对周围组织造成严重损伤; 射线穿透力极强,外照射危险性最高。在接触放射性物质时,必须做好防护措施。
描述放射性衰变速率的重要物理量是半衰期,符号 。半衰期是指放射性核素数量减少到原来一半所需的时间。经过 个半衰期后,剩余的放射性核素数量为:
其中 为初始数量。
不同放射性核素的半衰期差异极大:
半衰期是放射性核素的固有特性,不受温度、压力、化学状态等外部条件的影响。
例7 某放射性物质的半衰期为 天,初始时有 ,求 天后剩余的质量。
经过的半衰期个数:
天后剩余质量为 。
核衰变遵守两个重要守恒定律:质量数守恒(反应前后各粒子质量数之和相等)和电荷数守恒(反应前后各粒子质子数之和相等)。利用这两个守恒定律,可以判断核反应产物的种类。
练习题
选择题
第1题 关于原子的结构,下列说法正确的是( )
A. 原子核占据了原子的大部分体积
B. 电子的质量与质子的质量相近
C. 原子核由质子和电子构成
D. 原子对外呈电中性,是因为质子数等于核外电子数
答案:D
原子核只占原子体积的极小部分,A 错误;电子质量约为质子质量的 ,B 错误;原子核由质子和中子构成,不含电子,C 错误;原子呈电中性是因为核内质子数与核外电子数相等,正负电荷抵消,D 正确。
第2题 某原子的符号为 ,则该原子核内的中子数为( )
A. B. C. D.
答案:B
原子符号 中,左上角 为质量数,左下角 为质子数。中子数 ,答案为 B。
第3题 碳-12和碳-14是碳元素的两种同位素,下列关于它们的描述正确的是( )
A. 质子数不同,中子数相同
B. 质子数相同,中子数不同,化学性质不同
C. 质子数相同,中子数不同,化学性质几乎相同
D. 质量数相同,化学性质完全不同
答案:C
同位素的定义是质子数相同、中子数不同的同一元素的原子。碳-12和碳-14质子数均为 ,中子数分别为 和 ,质量数不同。由于质子数(原子序数)相同,两者化学性质几乎完全相同,C 正确。
第4题 一种放射性核素经过两次 衰变和一次 衰变后,其质量数和质子数的变化为( )
A. 质量数减少 ,质子数减少
B. 质量数减少 ,质子数减少
C. 质量数减少 ,质子数减少
D. 质量数减少 ,质子数减少
答案:A
每次 衰变:质量数减少 ,质子数减少 ;每次 衰变:质量数不变,质子数增加 。
两次 衰变:质量数减少 ,质子数减少 ;
计算题
第5题 某放射性物质的半衰期为 天,实验室中现有该物质 。
(1) 天后,剩余的放射性物质有多少克?
(2)若要使该物质减少到 ,需要经过多少天?
解:
(1)经过15天:
半衰期个数:
第6题 已知一个 原子核经过一系列衰变,最终变为 (铅-207)。
(1)在整个衰变过程中,共发生了多少次 衰变?
(2)共发生了多少次 衰变?
解:
设共发生 次 衰变和 次 衰变。
根据质量数守恒:
每次 衰变质量数减少 , 衰变质量数不变,因此: